
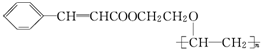
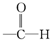 +
+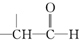 $→_{△}^{稀OH-}$
$→_{△}^{稀OH-}$ +H2O
+H2O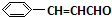 +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2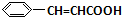 +H2O;③C与F的反应:
+H2O;③C与F的反应: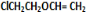 +
+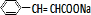 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$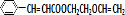 +NaCl.
+NaCl.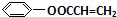 .
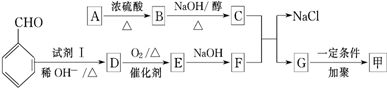
. 分析 G通过加聚反应生成高分子化合物甲,由甲的结构可知,G为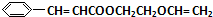 ,试剂Ⅰ可由相对分子质量为26的烃与水,该烃为乙炔,乙炔与水发生加成反应生成乙醛,故试剂Ⅰ是CH3CHO,苯甲醛与乙醛,在稀OH-、加热条件下生成D,由反应信息②可知,D为
,试剂Ⅰ可由相对分子质量为26的烃与水,该烃为乙炔,乙炔与水发生加成反应生成乙醛,故试剂Ⅰ是CH3CHO,苯甲醛与乙醛,在稀OH-、加热条件下生成D,由反应信息②可知,D为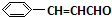 ,D催化氧化生成E,故E为
,D催化氧化生成E,故E为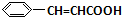 ,E与氢氧化钠反应生成F,故F为
,E与氢氧化钠反应生成F,故F为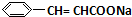 ,F与C反应生成G与NaCl,根据G的结构可知,C为
,F与C反应生成G与NaCl,根据G的结构可知,C为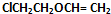 ,A的相对分子质量是80.5,A分子中氧元素的质量分数为19.88%,氧原子数目为$\frac{80.5×19.88%}{16}$=1,碳元素的质量分数为29.81%,碳原子的数目为$\frac{80.5×29.81%}{12}$=2,碳原子与氧原子的相对原子质量为12+16=28,故A含有1个Cl原子,A分子H原子数目为$\frac{80.5-35.5-16-12×2}{1}$=5,故A的分子式为C2H5OCl,A的核磁共振氢谱上有三个吸收峰,峰面积的比例为2:2:1,则A的结构简式为ClCH2CH2OH,由反应信息①可知,B为ClCH2CH2OCH2CH2Cl,B在氢氧化钠醇溶液、加热条件下,发生部分消去反应生成
,A的相对分子质量是80.5,A分子中氧元素的质量分数为19.88%,氧原子数目为$\frac{80.5×19.88%}{16}$=1,碳元素的质量分数为29.81%,碳原子的数目为$\frac{80.5×29.81%}{12}$=2,碳原子与氧原子的相对原子质量为12+16=28,故A含有1个Cl原子,A分子H原子数目为$\frac{80.5-35.5-16-12×2}{1}$=5,故A的分子式为C2H5OCl,A的核磁共振氢谱上有三个吸收峰,峰面积的比例为2:2:1,则A的结构简式为ClCH2CH2OH,由反应信息①可知,B为ClCH2CH2OCH2CH2Cl,B在氢氧化钠醇溶液、加热条件下,发生部分消去反应生成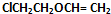 ,据此解答.
,据此解答.
解答 解:G通过加聚反应生成高分子化合物甲,由甲的结构可知,G为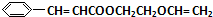 ,试剂Ⅰ可由相对分子质量为26的烃与水,该烃为乙炔,乙炔与水发生加成反应生成乙醛,故试剂Ⅰ是CH3CHO,苯甲醛与乙醛,在稀OH-、加热条件下生成D,由反应信息②可知,D为
,试剂Ⅰ可由相对分子质量为26的烃与水,该烃为乙炔,乙炔与水发生加成反应生成乙醛,故试剂Ⅰ是CH3CHO,苯甲醛与乙醛,在稀OH-、加热条件下生成D,由反应信息②可知,D为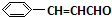 ,D催化氧化生成E,故E为
,D催化氧化生成E,故E为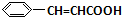 ,E与氢氧化钠反应生成F,故F为
,E与氢氧化钠反应生成F,故F为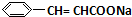 ,F与C反应生成G与NaCl,根据G的结构可知,C为
,F与C反应生成G与NaCl,根据G的结构可知,C为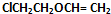 ,A的相对分子质量是80.5,A分子中氧元素的质量分数为19.88%,氧原子数目为$\frac{80.5×19.88%}{16}$=1,碳元素的质量分数为29.81%,碳原子的数目为$\frac{80.5×29.81%}{12}$=2,碳原子与氧原子的相对原子质量为12+16=28,故A含有1个Cl原子,A分子H原子数目为$\frac{80.5-35.5-16-12×2}{1}$=5,故A的分子式为C2H5OCl,A的核磁共振氢谱上有三个吸收峰,峰面积的比例为2:2:1,则A的结构简式为ClCH2CH2OH,由反应信息①可知,B为ClCH2CH2OCH2CH2Cl,B在氢氧化钠醇溶液、加热条件下,发生部分消去反应生成
,A的相对分子质量是80.5,A分子中氧元素的质量分数为19.88%,氧原子数目为$\frac{80.5×19.88%}{16}$=1,碳元素的质量分数为29.81%,碳原子的数目为$\frac{80.5×29.81%}{12}$=2,碳原子与氧原子的相对原子质量为12+16=28,故A含有1个Cl原子,A分子H原子数目为$\frac{80.5-35.5-16-12×2}{1}$=5,故A的分子式为C2H5OCl,A的核磁共振氢谱上有三个吸收峰,峰面积的比例为2:2:1,则A的结构简式为ClCH2CH2OH,由反应信息①可知,B为ClCH2CH2OCH2CH2Cl,B在氢氧化钠醇溶液、加热条件下,发生部分消去反应生成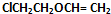 ,
,
(1)由上述分析可知,A为ClCH2CH2OH,
故答案为:ClCH2CH2OH;
(2)试剂Ⅰ可由相对分子质量为26的烃与水,该烃为乙炔,乙炔与水发生加成反应生成乙醛,故试剂Ⅰ是CH3CHO,
B→C是ClCH2CH2OCH2CH2Cl氢氧化钠醇溶液、加热条件下,发生部分消去反应生成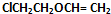 ,
,
故答案为:乙醛,消去反应;
(3)①A→B是ClCH2CH2OH在浓硫酸作用下发生取代反应生成ClCH2CH2OCH2CH2Cl,反应的方程式为2ClCH2CH2OH $→_{△}^{浓H_{2}SO_{4}}$ClCH2CH2OCH2CH2Cl+H2O;
②D→E是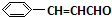 催化氧化生成
催化氧化生成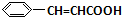 ,反应方程式为:2
,反应方程式为:2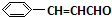 +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2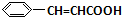 +H2O,
+H2O,
③C与F的反应是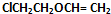 与
与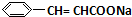 生成
生成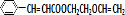 与NaCl,反应方程式为:
与NaCl,反应方程式为: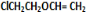 +
+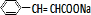 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$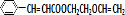 +NaCl,
+NaCl,
故答案为:2ClCH2CH2OH $→_{△}^{浓H_{2}SO_{4}}$ClCH2CH2OCH2CH2Cl+H2O;2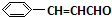 +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2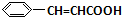 +H2O;
+H2O;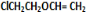 +
+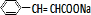 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$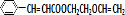 +NaCl;
+NaCl;
(4)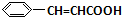 的一种同分异构体,水解产物有两种,说明该异构体含有酯基,一种水解产物能使溴水褪色,故该异构体中含有C=C双键,另一种水解产物在滴加饱和溴水后,有白色沉淀生成,该产物中含有酚羟基,故该异构体含有羧酸酚酯,故该物质的结构简式为
的一种同分异构体,水解产物有两种,说明该异构体含有酯基,一种水解产物能使溴水褪色,故该异构体中含有C=C双键,另一种水解产物在滴加饱和溴水后,有白色沉淀生成,该产物中含有酚羟基,故该异构体含有羧酸酚酯,故该物质的结构简式为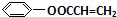 ,
,
故答案为: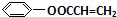 .
.
点评 本题考查有机物的推断,是对有机知识的综合运用,注意根据甲的结构推断其单体,再结合反应信息,利用正、逆推法结合推断,能较好的考查考生的阅读、自学能力和思维能力,难度中等,是热点题型.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 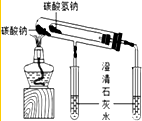 比较碳酸钠与碳酸氢钠的热稳定性 | B. |  称取NaOH | ||
| C. | 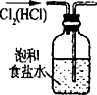 除去Cl2中HCl | D. | 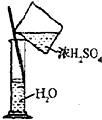 稀释浓H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 鉴定蔗糖水解产物中有葡萄糖:直接在水解液中加入新制Cu(OH)2悬浊液 | |
| B. | 鉴别某白色纺织品的成分是蚕丝还是“人造丝”,可用灼烧的方法 | |
| C. | 乙醇可以被酸性高锰酸钾溶液或酸性重铬酸钾溶液直接氧化成乙酸 | |
| D. | 醇CH3CHOHCH3能在铜或银作催化剂的条件下发生催化氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
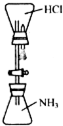 某同学受喷泉实验原理的启发,设计如图所示装置进行“喷烟”实验.下列对实验的有关说法错误的是( )
某同学受喷泉实验原理的启发,设计如图所示装置进行“喷烟”实验.下列对实验的有关说法错误的是( )| A. | 由于NH3的密度比HCl小,实验中二者的位置不能调换 | |
| B. | “白烟”是由于生成NH4Cl固体小颗粒的缘故 | |
| C. | 若用HBr代替HCl进行相同的操作,可得到相同的现象 | |
| D. | 实验时,打开活塞并挤出胶头滴管中的水即可看到白烟 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
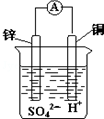
| A. | 电子从锌片经导线流向铜片 | B. | 氢离子在铜表面被还原,产生气泡 | ||
| C. | 锌是负极,其质量逐渐减小 | D. | 溶液由无色变为蓝色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定有SO${\;}_{4}^{2-}$- | B. | 一定有CO32- | ||
| C. | 不能确定Cl-是否存在 | D. | 不能确定HCO3-是否存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容器内气体压强不再改变 | |
| B. | 有2mol NH3生成的同时有3mol H2反应 | |
| C. | 生成NH3的量与反应掉N2的量之比为2:1 | |
| D. | N2、H2、NH3的物质的量之比为1:3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com