
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
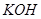 溶液中,得到含有次氯酸钾、氯酸钾和氯化钾的混合溶液。若反应过程中转移
溶液中,得到含有次氯酸钾、氯酸钾和氯化钾的混合溶液。若反应过程中转移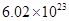 个电子,所得溶液中
个电子,所得溶液中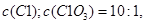 则参与反应的
则参与反应的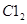 的物质的量为( )
的物质的量为( )A.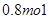 | B.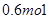 | C.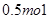 | D.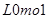 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.85 | B.0.75 | C.0.65 | D.0.60 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
| V(Cl2)(标况,L) | 2.8 | 5.6 | 11.2 |
| n(Cl—) /mol | 1.5 | 1.75 | 2.25 |
| n(Br—) /mol | 1.5 | 1.4 | 0.9 |
| n(I—)/mol | a | 0 | 0 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 N2 + NH4Cl
N2 + NH4Cl 查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A. +3 | B.+2 | C.+1 | D.+6 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.5∶3 | B.5∶4 | C.1∶1 | D.3∶5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com