
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
下列实验可实现鉴别目的的是( )
A.用KOH溶液鉴别SO3(g)和SO2
B.用湿润碘化钾淀粉试纸鉴别Br2(g)和NO2
C.用CO2鉴别NaAlO2溶液和CH3COONa溶液
D.用BaCl2溶液鉴别AgNO3溶液和K2SO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
NA表示阿伏加德罗常数,下列叙述正确的是 ( )
A.1 mol Fel2与足量氯气反应时转移的电子数为2NA
B.2 L 0.5 mol/l硫酸钾溶液中阴离子所带电荷数为NA
C.1 mol Na202固体中含离子总数为4NA
D.丙烯和环丙烷组成的42 g混合气体中氢原子的个数为6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是
A.熵变小于零而焓变大于零的反应肯定不能发生
B.热化学方程式中ΔH的值与反应物的用量有关
C.化学反应中旧键断裂吸收能量,新键形成释放能量,所以化学反应伴随能量变化,
但反应前后物质的总能量不变
D.用蒸馏水稀释0.1mol/L的醋酸至0.01mol/L,稀释过程中温度维持25℃不变,溶
液中各离子浓度均减小
查看答案和解析>>
科目:高中化学 来源: 题型:
已知可逆反应X(g)+2Y(g) 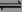 Z(g) ΔH<0,一定温度下,在体积为2 L的密闭容器中加入4 mol Y和一定量的X后,X的浓度随时间的变化情况如右图所示,则下列说法正确的是
Z(g) ΔH<0,一定温度下,在体积为2 L的密闭容器中加入4 mol Y和一定量的X后,X的浓度随时间的变化情况如右图所示,则下列说法正确的是
A.a点正反应速率大于逆反应速率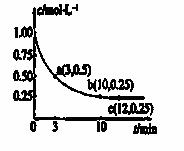
B.增大X的浓度,X的转化率增大
C.容器中压强恒定时,不能说明反应已达平衡状态
D.保持温度和密闭容器的压强不变,再充入1 mol X和
2 mol Y,再次达到平衡时n(Z)/n(X)的值会变小
查看答案和解析>>
科目:高中化学 来源: 题型:
过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用来消
毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,欲准确测定过氧化
氢的含量。请填写下列空白:
(1)取10.00 mL密度为ρg/mL的过氧化氢溶液稀释至250mL。移取稀释后的过氧化
氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式为 。
(3)滴定时,将高锰酸钾标准溶液注入 (填“酸式”或“碱式”)滴定管
中,滴定到达终点的现象是 。
(4)重复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中
过氧化氢的质量分数为 。
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果 (填
“偏高”或“偏低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验方案合理的是
A.配制50g质量分数为5%NaCl溶液:将45mL水加入到盛有5g NaCl的烧杯中,搅拌溶解
B.制备乙酸乙酯:用如图所示的实验装置
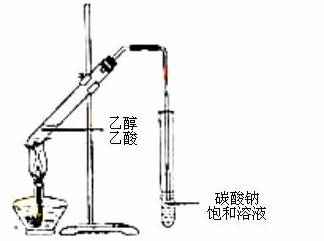
C.鉴定SO42—:向溶液中加入盐酸酸化的氯化钡溶液
D.鉴别环己烯和苯:将溴的四氯化碳溶液分别滴加到少量环己烯和苯中
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH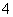 )=c(Cl-),则溶液显________性(填“酸”“碱”或“中”);用含a的代数式表示NH3·H2O的电离常数Kb=________。
)=c(Cl-),则溶液显________性(填“酸”“碱”或“中”);用含a的代数式表示NH3·H2O的电离常数Kb=________。
(2)常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,
c(H2CO3)=1.5×10-5mol·L-1。若忽略水的电离及H2CO3的第二级电离,则H2CO3 HCO
HCO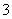 +H+的平衡常数K1=________(已知10-5.60=2.5×10-6)。
+H+的平衡常数K1=________(已知10-5.60=2.5×10-6)。
(3)沉淀物并非绝对不溶,其在水及各种不同溶液中的溶解度有所不同,同离子效应、络合物的形成等都会使沉淀物的溶解度有所改变。下图是AgCl在NaCl、AgNO3溶液中的溶解情况。
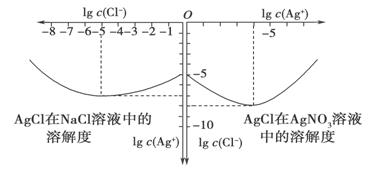
由以上信息可知:
①AgCl的溶度积常数的表达式为____________________________,
由图知AgCl的溶度积常数为________________________________。
②向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,c(Br-)/c(Cl-)=________。[Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10]
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com