
【题目】有关元素X、Y、Z、D、E的信息如下:
元素 | 有关信息 |
X | 元素主要化合价-2,原子半径为0.0074 nm |
Y | 所在主族序数与所在周期序数之差为4 |
Z | 单质在X的单质中燃烧,产物是造成酸雨的罪魁祸首之一 |
D | 最高价氧化物对应的水化物能电离出电子数相等的阴、阳离子 |
E | 单质是生活中的常见金属,其制品在潮湿空气中易被腐蚀或损坏 |
请回答下列问题(用化学用语表示):
(1)X的一种氢化物可用于实验室制取X的单质,其反应的化学方程式为____________。
(2)比较Y与Z的氢化物的稳定性________(用化学式表示)。
(3)E元素与Y元素可形成EY2和EY3两种化合物,则下列说法中正确的是________(填序号)
①通常实验室配制EY3溶液时,可直接用水溶解EY3固体
②EY2不能通过单质直接化合产生
③铜片、碳棒和EY3溶液组成原电池,电子由铜片沿导线流向碳棒
④Y、Z、D的离子半径大小依次减小
(4)Y的最高价氧化物为无色液体,当0.25 mol该物质与一定量的水混合得到一种稀溶液时,放出Q kJ的热量,写出该反应的热化学方程式_______________________________。
(5)写出E在潮湿的空气中发生腐蚀时正极上的电极反应式_____________________。
【答案】(1)2H2O2![]() 2H2O+O2↑ (2)HCl>H2S (3)②③
2H2O+O2↑ (2)HCl>H2S (3)②③
(4)Cl2O7(l)+H2O(l)===2HClO4(aq)ΔH=-4 QkJ/mol (5)O2+2H2O+4e-=4OH-
【解析】试题分析:X 元素主要化合价-2,原子半径为0.0074 nm,因此X为氧元素;Y所在主族序数与所在周期序数之差为4 ,因此Y为氯元素;Z 单质在X的单质中燃烧,产物是造成酸雨的罪魁祸首之一,则Z为硫元素;D 最高价氧化物对应的水化物能电离出电子数相等的阴、阳离子,则D为钠元素;E单质是生活中的常见金属,其制品在潮湿空气中易被腐蚀或损坏,所以E是铁元素。
(1)X的一种氢化物可用于实验室制取X的单质,该物质是双氧水,其反应的化学方程式为2H2O2![]() 2H2O+O2↑。
2H2O+O2↑。
(2)氯元素的非金属性强于硫元素,非金属性越强,氢化物越稳定,则氢化物的稳定性HCl>H2S。
(3)①铁离子水解,因此通常实验室配制FeCl3溶液时,先将氯化铁溶解在浓盐酸中,然后再稀释,①错误;②铁与氯气发生化合反应生成氯化铁,得不到FeCl2,②正确;③铜片、碳棒和EY3溶液组成原电池,铜是负极,则电子由铜片沿导线流向碳棒,③正确;④D、Y、Z的离子半径大小依次增大,④错误,答案选②③。
(4)Y的最高价氧化物为无色液体,当0.25 mol该物质与一定量的水混合得到一种稀溶液时,放出Q kJ的热量,则该反应的热化学方程式为Cl2O7(l)+H2O(l)===2HClO4(aq)ΔH=-4 QkJ/mol。
(5)铁在潮湿的空气中发生腐蚀时正极上的电极反应式为O2+2H2O+4e-=4OH-。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】化学在生产和日常生活中有着重要的应用。下列说法正确的是( )
A.汽车的排气管上装有“催化转化器”,使有毒的CO和NO反应生成N2和CO2
B.氢氟酸保存在细口玻璃瓶中。
C.高纯度的硅单质广泛用于制作光导纤维
D.大量燃烧化石燃料排放的废气中含CO2、SO2,从而使雨水的pH=5.6形成酸雨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧气(O2)和臭氧(O3)是氧元素的两种同素异形体,已知热化学方程式:
4Al(s)+3O2(g)===2Al2O3(s) ΔH1
4Al(s)+2O3(g)===2Al2O3(s) ΔH2
3O2(g)===2O3(g) ΔH3则( )
A.ΔH1-ΔH2=ΔH3
B.ΔH1+ΔH2=ΔH3
C.ΔH2-ΔH1=ΔH3
D.ΔH2+ΔH1+ΔH3=0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图表示4个碳原子相互结合的几种方式。小圆球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢结合,则下列说法正确的是 ( )
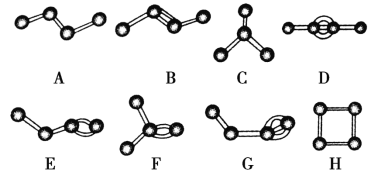
A.图中属于烷烃的是A、C、H
B.图中C和F分子中氢原子数相同
C.图中物质碳元素的质量分数最大的是C
D.图中与B互为同分异构体的有E、F、H
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z是短周期三种元素,它们在周期表中的位置如图所示。试回答:
X | ||
Y | ||
Z |
(1)X元素单质的化学式是__________________________________。
(2)Z元素的原子结构示意图为________________________________。
(3)Y在元素周期表中的位置是______________________。
(4)与Z同主族的下一周期元素的原子序数是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D是四种常见的有机物,其中A是一种气态烃,在标准状况下的密度为1.25 g/L;B与C在浓硫酸和加热条件下发生反应,生成的有机物有特殊香味;A、B、C、D在一定条件下的转化关系如图所示(反应条件已省略):
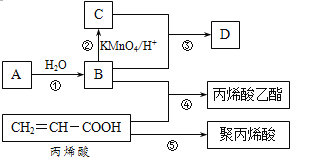
(1)A的电子式为___________,C中官能团的名称为__________。
(2)丙烯酸(CH2=CH-COOH)的性质可能有_______________。
A.加成反应
B.取代反应
C.加聚反应
D.中和反应
E.氧化反应
(3)用两种方法鉴别B和C,所用试剂分别是___________、___________。
(4)丙烯酸乙酯的结构简式为 。
(5)写出下列反应方程式和有机反应基本类型:
①____________________ _ _______,_________反应;
④____________________ _ _______,_________反应;
⑤____________________ _ _______,_________反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分子晶体中如果不是由于分子本身形状的影响,它的晶体将取密堆积结构,原因是分子晶体中( )
A.分子间作用力无一定方向性
B.占据晶格结点的微粒是原子
C.化学键是共价键
D.三者都是
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com