
【题目】含有砒霜(As2O3)的试样和锌、盐酸混合反应,生成的砷化氢(AsH3)在热玻璃管中完全分解成单质砷和氢气。若砷的质量为1.50 mg,则( )
A.被氧化的砒霜为1.98 mg
B.分解产生的氢气为 0.672 mL
C.和砒霜反应的锌为3.90 mg
D.生成砷化氢时,转移的电子总数为6×10-5NA
【答案】C
【解析】
试题分析:A.反应中As元素化合价由As2O3中+3价降低为AsH3中-3价,砒霜发生还原反应,故A错误;B.生成As的物质的量=![]() =2×10-5mol,根据原子守恒可知分解的AsH3为2×10-5mol,由H原子守恒可知生成氢气为
=2×10-5mol,根据原子守恒可知分解的AsH3为2×10-5mol,由H原子守恒可知生成氢气为![]() =3×10-5mol,故标况下,分解产生氢气体积为3×10-5mol×22.4L/mol=6.72×10-4L=0.672 mL,但氢气所处的状态不一定是标准状况,故其体积不一定是0.672 mL,故B错误;C.根据电子转移守恒,可知参加反应Zn的物质的量=2×10-5mol×[3-(-3)]÷2=6×10-5mol,故参加反应Zn的质量=6×10-5mol×65g/mol=3.9×10-3g=3.9mg,故C正确;D.整个过程中,As元素化合价由As2O3中+3价降低为AsH3中-3价,AsH3中-3价升高为As中0价,故整个过程转移电子总数为2×10-5mol×(6+3)×NAmol-1=1.8×10-4NA,故D错误;故选C。
=3×10-5mol,故标况下,分解产生氢气体积为3×10-5mol×22.4L/mol=6.72×10-4L=0.672 mL,但氢气所处的状态不一定是标准状况,故其体积不一定是0.672 mL,故B错误;C.根据电子转移守恒,可知参加反应Zn的物质的量=2×10-5mol×[3-(-3)]÷2=6×10-5mol,故参加反应Zn的质量=6×10-5mol×65g/mol=3.9×10-3g=3.9mg,故C正确;D.整个过程中,As元素化合价由As2O3中+3价降低为AsH3中-3价,AsH3中-3价升高为As中0价,故整个过程转移电子总数为2×10-5mol×(6+3)×NAmol-1=1.8×10-4NA,故D错误;故选C。


 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案科目:高中化学 来源: 题型:
【题目】某芳香烃A,分子式为C8H10,B、C的混合物在NaOH乙醇溶液中加热可以生成同一种有机物Y,以Y为单体可以合成高分子化合物。某烃类衍生物X,分子式为C15H14O3,遇FeCl3溶液显紫色;J分子内有两个互为对位的取代基。在一定条件下有如下的转化关系(无机物略去):

(1)一种属于芳香烃类的A的同分异构体,其苯环上的一氯代物仅有一种,其结构简式为 。
(2)J中所含的含氧官能团的名称为__________________。
(3)E与H反应的化学方程式是_______________,反应类型是_____________。
(4)已知J有多种同分异构体,写出一种符合下列性质的J的同分异构体的结构简式:_________________________。
① 与FeCl3溶液作用显紫色
② ②与新制Cu(OH)2悬浊液作用产生红色沉淀
③ ③苯环上的一卤代物有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,同种规格的铝片分别与下列物质混合,产生氢气速率最大的是
A. 0.1 mol/L的盐酸15mL B. 0.15 mol/L的硫酸溶液8mL
C. 0.4 mol/L的硝酸12mL D. 18 mol/L的浓硫酸15mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用电镀污泥(主要含有Fe2O3、CuO、Cr2O3及部分难溶杂质)回收铜和铬等金属,回收流程如下:
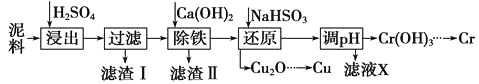
已知部分物质沉淀的pH及CaSO4的溶解度曲线如下:
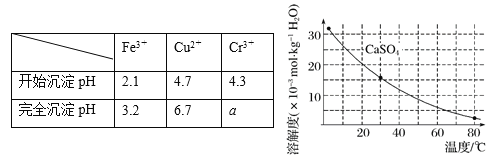
(1)在浸出过程中除了生成Fe2(SO4)3、Cr2(SO4)3外,主要还有 。
(2)在除铁操作中,需要除去Fe3+和CaSO4,请完成相关操作:
①加入石灰乳调节pH范围 ,检验Fe3+已经除尽的操作是 ;
②将浊液加热到80℃, 。
(3)写出还原步骤中加入NaHSO3生成Cu2O固体反应的离子方程式: ,此步骤中加入NaHSO3得到Cu2O的产率为95%,若NaHSO3过量,除了浪费试剂外,还会出现的问题是 。
(4)当离子浓度小于或等于1×10-5 mol·L-1时可认为沉淀完全,若要使Cr3+完全沉淀则要保持c(OH-)≥ 。[已知:Ksp[Cr(OH)3] = 6.3×10-31,![]() ≈4.0]。
≈4.0]。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分。
碳 | 氮 | Y | ||
铝 | X | 硫 | Z |
请回答下列问题:
(1)Z元素在周期表中的位置为_______________。
(2)表中元素原子半径最大的非金属是(元素符号)_______________。
(3)下列事实能说明Y元素的非金属性比S元素的非金属性强的是_______________;
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1 mol Y单质比1 mol S得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(4)碳与镁形成的1 mol 化合物Q与水反应,生成2 mol Mg(OH)2和1 mol烃,该烃分子中碳氢质量比为9:1。Q的化学式为_____________________。
(5)向氯化铝溶液中加入过量氨水,离子方程式为 。
(6)将SO2通入稀硝酸中,反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2和I2在一定条件下能发生反应:H2(g) + I2(g)![]() 2HI(g) ΔH=-a kJ·mol-1
2HI(g) ΔH=-a kJ·mol-1
已知: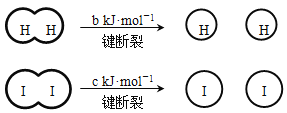 (a、b、c均大于零)
(a、b、c均大于零)
下列说法不正确的是( )
A.反应物的总能量高于生成物的总能量
B.断开1 mol H-H键和1 mol I-I键所需能量大于断开2 mol H-I键所需能量
C.断开2 mol H-I键所需能量约为(c+b+a) kJ
D.向密闭容器中加入2 mol H2和2 mol I2,充分反应后放出的热量小于2a kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铬铁矿的主要成分可表示为FeO·Cr2O3,还含有MgO、Al2O3、Fe2O3等杂质,以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的工艺如下(部分操作和条件略):
Ⅰ.将铬铁矿和碳酸钠混合在空气中充分焙烧。
Ⅱ.焙烧后的固体加水浸取,分离得到溶液A和固体A。
Ⅲ.向溶液A中加入醋酸调pH约7~8,分离得到溶液B和固体B。
Ⅳ.再向溶液B中继续加醋酸酸化,使溶液pH小于5。
Ⅴ.向上述溶液中加入氯化钾,得到重铬酸钾晶体。
(1)Ⅰ中焙烧发生的反应如下,配平并填写空缺:
① FeOCr2O3 + Na2CO3 + □ = Na2CrO4 + Fe2O3 + CO2↑
② Na2CO3+Al2O3=2NaAlO2+CO2↑
(2)固体A中主要含有 (填写化学式)。
(3)Ⅴ中发生反应的化学方程式是:Na2Cr2O7+2KCl=K2Cr2O7↓+2NaCl,已知下表数据
物质 | KCl | NaCl | K2Cr2O7 | Na2Cr2O7 | |
溶解度 (g/100g水) | 0℃ | 28 | 35.7 | 4.7 | 163 |
40℃ | 40.1 | 36.4 | 26.3 | 215 | |
80℃ | 51.3 | 38 | 73 | 376 | |
获得K2Cr2O7晶体的操作由多步组成,依次是:加入KCl固体、 、过滤、洗涤、干燥得到晶体。洗涤沉淀的操作为 。
(4)Ⅲ中固体B中主要含氢氧化铝,还含少量镁、铁的难溶化合物及可溶性杂质,精确分析固体B中氢氧化铝含量的方法是:称取n g样品,加入过量 (填写试剂名称)、溶解、过滤、再通入过量的CO2、灼烧、冷却、称量,得干燥固体m g。计算样品中氢氧化铝的质量分数为 (用含m、n的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com