
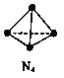
【题目】N4分子结构为正四面体(如图所示)。已知:断裂N4(g)中1 molN-N键吸收193kJ能量,形成N2(g)中1 mol N![]() N放出941 kJ能量。下列说法正确的是
N放出941 kJ能量。下列说法正确的是
A. N4(g)比N2(g)更稳定
B. N4(g)=2N2(g) △H=+724kJmol-1
C. 形成1 mol N4(g)中的化学键放出193 kJ的能量
D. lmolN2(g)完全转化为N4(g),体系的能量增加362kJ
【答案】D
【解析】从结构图中可看出,一个N4分子中含有6个N-N键,根据N4(g)=2N2(g)△H,有△H=6×193 kJmol-1-2×941 kJmol-1=-724 kJmol-1。A.根据上述分析,N4比N2的能量高,没有N2的稳定,故A错误;B.根据上述分析,N4(g)=2N2(g)△H=-724 kJmol-1,故B错误;C.一个N4分子中含有6个N-N键,形成1 mol N4(g)中的化学键放出6×193 kJ的能量,故C错误;D.根据上述分析,lmolN2(g)完全转化为N4(g),需要吸收362kJ的热量,体系的能量增加362kJ,故D正确;故选D。
点晴:本题考查反应热与化学键键能的关系。注意从物质能量、键能角度理解反应热,明确反应热的焓变△H=反应物总键能-生成物总键能以及焓变的正负与吸收、放出热量的关系是解答的关键。本题的易错点为C,要注意一个N4分子中含有6个N-N键。


科目:高中化学 来源: 题型:
【题目】实验室用密度为1.25g/mL,质量分数为36.5%的浓盐酸配置240mL 0.1mol/L的盐酸.浓盐酸的物质量浓度为多少?配置稀盐酸应取用的浓盐酸的体积为多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚铁氰化钾(K4[Fe(CN)6])俗称黄血盐,易溶于水和丙酮,是食盐的一种抗结剂,用含NaCN(N显-3价)的废液合成黄血盐的主要工艺流程如图:

(1)实验室用NaCN固体配制NaCN溶液时,应先将其溶于____溶液,再用蒸馏水稀释。
(2)在流程图“反应器”中发生的主要反应的方程式为_______________。
(3)流程中加入碳酸钠溶液主要目的是除去__________;
(4)相同温度下溶解度:Na4[Fe(CN)6]____K4[Fe(CN)6](选填>、<、=)。
(5)我国卫生部规定食盐中黄血盐最大使用量为10 mg/kg,黄血盐可与酸性高锰酸钾溶液反应:K4[Fe(CN)6]+KMnO4+H2SO4—KHSO4+Fe2(SO4)3+MnSO4+HNO3+CO2+H2O(未配平),若有1molK4[Fe(CN)6]被氧化,则消耗高锰酸钾的物质的量为____。
(6)电镀银时,电镀液不能直接用硝酸银溶液,可将其转变为K4[Ag2(CN)6]溶液,写出AgCl与黄血盐溶液制取电镀液的离子方程式_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,pH=l 的某溶液 A 中除H+外,还含有NH4+、K+、Na+、Fe3+、Al3+、Fe2+、CO32-、NO3-、 Cl-、I-、SO42-中的4种,且溶液中各离子的物质的量浓度均为0.1mol·L-1。现取该溶液进行有关实验,实验结果如下图所示,下列有关说法正确的是

A. 该溶液中一定有上述离子中的NO3-、Al3+、SO42-、Cl-四种离子
B. 实物消耗Cu14.4g,则生成气体丁的体积为3.36L
C. 该溶液一定没有Fe3+,但是无法确定是否含有I-
D. 沉淀乙一定有BaCO3,可能有BaSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用KMnO4氧化一定体积密度为1.19g/cm3 , 溶质质量分数为36.5%的 盐酸.反应方程式如下:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
(1)用双线桥法分析该反应(只需标出电子得失的方向和数目)
(2)15.8g KMnO4参加反应能消耗多少摩尔HCl?
(3)产生的Cl2在标准状况下的体积为多少升?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分析下列反应回答相应问题.
①3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
未被还原的硝酸与参加反应的总硝酸的质量比为 .
②S+2KNO3+3C ![]() K2S+N2↑+3CO2↑ 还原剂是还原产物是
K2S+N2↑+3CO2↑ 还原剂是还原产物是
③3Cl2+6NaOH ![]() 5NaCl+NaClO3+3H2O 反应中若消耗3molCl2共转移mol电子.
5NaCl+NaClO3+3H2O 反应中若消耗3molCl2共转移mol电子.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在细胞内含量极少,但对维持生命活动必不可少的元素有( )
A. Fe Mn Zn Mg B. Zn Cu Mg Ca
C. Zn Cu B Mn D. Mg Mn Cu Mo
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为硬脂酸甘油酯在碱性条件下水解的装置图。进行皂化反应时的步骤如下:

(1)在圆底烧瓶中装入7~8 g硬脂酸甘油酯,然后加入2~3 g氢氧化钠、5 mL 水和10 mL酒精,加入酒精的作用是________________________。
(2)隔着石棉网给反应混合物加热约10 min,皂化反应基本完成,所得到的混合物为________(填“悬浊液”、“乳浊液”、“溶液”或“胶体”)。
(3)向所得混合物中加入________,静置一段时间后,液体分为上下两层,肥皂在________层,这个操作称为________。
(4)图中长玻璃导管的作用为________________________。
(5)写出该反应的化学方程式:________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com