
【题目】(1)下列物质能导电的是___,属于电解质的是___。
①NaCl晶体 ②液态SO2 ③液态醋酸 ④铜 ⑤BaSO4固体 ⑥纯蔗糖(C12H22O11) ⑦氨水 ⑧熔化的KNO3
(2)0.5molCH4的质量是___g,在标准状况下的体积为___L;
(3)8.4g氮气和9.6g某单质Rx所含原子个数相同,且分子个数之比为3:2,则x的值是___,R的摩尔质量是___。
【答案】④⑦⑧ ①③⑤⑧ 8 11.2 3 16g/mol
【解析】
(1)①NaCl晶体不含自由移动的离子,不能导电,其溶于水可电离,水溶液可导电,是电解质;②液态SO2不含自由移动的离子,不能导电,其于水反应生成亚硫酸可电离,水溶液可导电,但不是自身导电,是非电解质;③液态醋酸不含自由移动的离子,不能导电,其溶于水可电离,水溶液可导电,是电解质; ④铜含有自由移动的电子可以导电,但属于单质,不是化合物,既不是电解质也不是非电解质;⑤BaSO4固体不含自由移动的离子,不能导电,熔融状态下电离生成离子可以导电,属于电解质; ⑥纯蔗糖(C12H22O11) 不含自由移动的离子,不能导电,在水溶液里和熔融状态下都不能导电,是非电解质; ⑦氨水含有自由移动的离子可以导电,是混合物,既不是电解质也不是非电解质; ⑧熔化的KNO3含有自由移动的离子,可以导电,属于电解质;
(2)根据n=![]() 可得,m=nM,V= nVm,进行计算;
可得,m=nM,V= nVm,进行计算;
(1)①NaCl晶体不含自由移动的离子,不能导电,其溶于水可电离,水溶液可导电,是电解质;②液态SO2不含自由移动的离子,不能导电,其于水反应生成亚硫酸可电离,水溶液可导电,但不是自身导电,是非电解质;③液态醋酸不含自由移动的离子,不能导电,其溶于水可电离,水溶液可导电,是电解质; ④铜含有自由移动的电子可以导电,但属于单质,不是化合物,既不是电解质也不是非电解质;⑤BaSO4固体不含自由移动的离子,不能导电,熔融状态下电离生成离子可以导电,属于电解质; ⑥纯蔗糖(C12H22O11) 不含自由移动的离子,不能导电,在水溶液里和熔融状态下都不能导电,是非电解质; ⑦氨水含有自由移动的离子可以导电,是混合物,既不是电解质也不是非电解质; ⑧熔化的KNO3含有自由移动的离子,可以导电,属于电解质;
下列物质能导电的是④⑦⑧,属于电解质的是①③⑤⑧,
答案为:④⑦⑧;①③⑤⑧;
(2)根据n=![]() 可得,m=nM,0.5molCH4的质量=0.5mol×16g/mol=8g;在标准状况下的体积为=nVm=0.5mol×22.4L/mol=11.2L,
可得,m=nM,0.5molCH4的质量=0.5mol×16g/mol=8g;在标准状况下的体积为=nVm=0.5mol×22.4L/mol=11.2L,
答案为:8;11.2;
(3)8.4g氮气的物质的量=![]() =
=![]() =0.3mol,则氮原子的物质的量=0.3mol×2=0.6mol,物质的量之比等于粒子数目之比,根据题意9.6g某单质Rx所含原子物质的量也为0.6mol,则Rx所含分子物质的量为
=0.3mol,则氮原子的物质的量=0.3mol×2=0.6mol,物质的量之比等于粒子数目之比,根据题意9.6g某单质Rx所含原子物质的量也为0.6mol,则Rx所含分子物质的量为![]() ,则0.3mol:
,则0.3mol:![]() =3:2,解得x=3,R3的物质的量为
=3:2,解得x=3,R3的物质的量为![]() =0.2mol,R3的摩尔质量=
=0.2mol,R3的摩尔质量=![]() =
=![]() =48g/mol,则R的摩尔质量=
=48g/mol,则R的摩尔质量=![]() =16g/mol,
=16g/mol,
答案为:3;16g/mol。


科目:高中化学 来源: 题型:
【题目】一学生设计了如下实验方法分离NaCl和CaCl2两种固体混合物
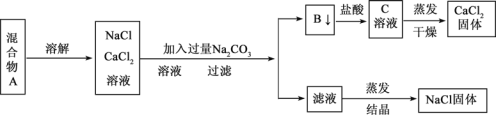
回答下列问题
(1)方案中反应的离子方程式是 __________、________________。
(2)按此实验方案分离得到的NaCl,经分析含有杂质,是因为上述方案中某一设计有毛病,这一步的正确设计方案应是____________________________。
(3)若要测定该样品中NaCl和CaCl2的质量比,可称量干燥的B 物质和另一物质的质量,这种物质是__________________。(填物质对应的字母)
(4)实验过程中检验洗涤 B 物质是否洗净的方法是___________________。
(5)该实验过程中需要0.1mol/L的Na2CO3溶液450 mL,实验老师用碳酸钠晶体(Na2CO3·10H2O)配制该浓度的溶液。请你协助老师完成下列问题:
① 配制Na2CO3溶液时需要的主要玻璃仪器有烧杯、玻璃棒、___________________。
② 该实验的第一步是计算,称取_________g碳酸钠晶体。
③ 若定容时仰视刻度线,则所配制的溶液浓度_____________(填“偏高”“偏低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.由CH4、O2和KOH溶液组成的燃料电池,负极反应为CH4+8OH--8e-=CO2+6H2O
B.常温下,反应2Na2O2(s)+2CO2(g)=2Na2CO3(s)+O2(g)能自发进行,该反应ΔH<0
C.反应C(s)+H2O(g)![]() CO(g)+H2(g)达平衡后,缩小容器体积,H2O(g)平衡转化率不变
CO(g)+H2(g)达平衡后,缩小容器体积,H2O(g)平衡转化率不变
D.0.1 mol·L-1 NH4Cl溶液加水稀释,![]() 的值减小
的值减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2 ,则下列说法中正确的是( )
2KClO3 + H2C2O4 + H2SO4 ![]() 2ClO2↑ + K2SO4 + 2CO2↑ + 2H2O
2ClO2↑ + K2SO4 + 2CO2↑ + 2H2O
A. KClO3在反应中是还原剂
B. 1molKClO3参加反应,在标准状况下能得到22.4L气体
C. 在反应中H2C2O4 既不是氧化剂也不是还原剂
D. 1molKClO3参加反应有1mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1-溴丙烷是一种重要的有机合成中间体,沸点为71℃,密度为1.36gcm-3.实验室制备少量1-溴丙烷的主要步骤如下:
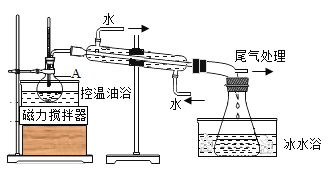
步骤1:在仪器A中加入搅拌磁子、12g正丙醇及20mL水,冰水冷却下缓慢加入28mL浓H2SO4;冷却至室温,搅拌下加入24gNaBr。
步骤2:如图所示搭建实验装置,缓慢加热,直到无油状物馏出为止。
步骤3:将馏出液转入分液漏斗,分出有机相。
步骤4:将分出的有机相转入分液漏斗,依次用12mLH2O、12mL5%Na2CO3溶液和12mLH2O洗涤,分液,得粗产品,进一步提纯得1-溴丙烷。
(1)步骤1发生反应的方程式为______
(2)仪器A的名称是______;加入搅拌磁子的目的是搅拌和______。
(3)反应时生成的主要有机副产物有______。
(4)反应过程中可以观察到A的上方出现红棕色气体,其电子式为______。
(5)步骤2中需向接受瓶内加入少量冰水并置于冰水浴中的目的是______。同时可以观察到的现象是______。
(6)步骤4中三次洗涤分别洗去的主要杂质是①______②______③______。
(5)步骤4中②的Na2CO3溶液还可以用下列哪个试剂代替______
A. NaOH溶液 B. NaI溶液 C. Na2SO3溶液 D. CCl4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示中,A为一种常见的单质,B、C、D、E是含有A元素的常见化合物。它们的焰色试验均为黄色。
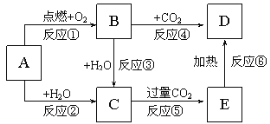
回答下列问题:
(1)写出化学式:A___,D___。
(2)以上反应中不属于氧化还原反应的有___(填序号)。
(3)反应③的离子方程式:___。氧化剂为___;氧化产物为___。
(4)向D溶液中通入CO2反应的化学方程式:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国化学侯德榜改革国外的纯碱生产工艺,生产流程如图所示,下列说法不正确的是( )

A. 在沉淀池中应先通入氨气,再通入二氧化碳气体
B. 该反应原理: NH3+CO2+H2O=HCO3-+NH4+
C. 循环1中X是二氧化碳
D. 在过滤后的母液中加入氯化钠粉末、通入氨气,搅拌,经冷却结晶后可得氯化铵晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 天然气和沼气的主要成分都是甲烷,它们都属于不可再生能源
B. 煤的气化和液化均属于物理变化
C. 石油裂解的目的是为了得到更多的汽油
D. 用含糖类、淀粉比较多的农作物为原料,在催化剂作用下,经水解和细菌发酵制乙醇的过程属于生物质能的利用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校学生课外活动小组的同学设计下图所示实验装置,用来验证一氧化碳具有还原性。回答下列问题。
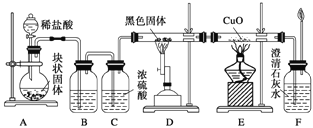
(1)写出装置A中发生反应的化学反应方程式:_______________________。
(2)装置B中最适宜的试剂是:_________________________。
(3)装置D中黑色固体为_____________(填名称),反应的化学方程式为:_____________________________。
(4)若实验中没有装置C,使装置B与装置D直接相连,会对实验造成的影响是: ___________________________________。
(5)按照如图装置进行实验时,首先进行的操作名称是_____________。
(6)根据实验中的_________________现象,可证明CO具有还原性,有关反应的化学方程式是___________________________。
(7)若要根据装置F中澄清石灰水变浑浊的现象确认一氧化碳具有还原性,应在上图装置________与________之间连接下图中的___________装置(填序号)。
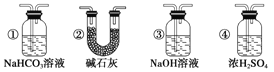
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com