
【题目】下列说法正确的是
A.由CH4、O2和KOH溶液组成的燃料电池,负极反应为CH4+8OH--8e-=CO2+6H2O
B.常温下,反应2Na2O2(s)+2CO2(g)=2Na2CO3(s)+O2(g)能自发进行,该反应ΔH<0
C.反应C(s)+H2O(g)![]() CO(g)+H2(g)达平衡后,缩小容器体积,H2O(g)平衡转化率不变
CO(g)+H2(g)达平衡后,缩小容器体积,H2O(g)平衡转化率不变
D.0.1 mol·L-1 NH4Cl溶液加水稀释,![]() 的值减小
的值减小
【答案】B
【解析】
A.在CH4、O2和KOH溶液组成的燃料电池中,负极反应式为:CH4+10OH--8e-=CO32-+7H2O,选项A错误;
B.常温下,反应2Na2O2(s)+2CO2(g)=2Na2CO3(s)+O2(g)是熵减的反应,ΔS<0,能自发进行,则ΔG=ΔH-TΔS<0,故该反应ΔH<0,选项B正确;
C.反应C(s)+H2O(g)![]() CO(g)+H2(g)为气体体积增大的反应,达平衡后,缩小容器体积,平衡逆向移动,H2O(g)平衡转化率减小,选项C错误;
CO(g)+H2(g)为气体体积增大的反应,达平衡后,缩小容器体积,平衡逆向移动,H2O(g)平衡转化率减小,选项C错误;
D.0.1 mol·L-1 NH4Cl溶液加水稀释,温度不变,电离平衡常数Kb=![]() 不变,故
不变,故![]() 的值不变,选项D错误;
的值不变,选项D错误;
答案选B。


科目:高中化学 来源: 题型:
【题目】(NH4)2SO4是常见的化肥和化工原料,受热易分解。某兴趣小组拟探究其分解产物。
[查阅资料](NH4)2SO4在260℃和400℃时分解产物不同。
[实验探究]该小组拟选用下图所示装置进行实验(夹持和加热装置略)

实验1:连接装置A-B-C-D,检查气密性,按图示加入试剂(装置B盛0.5000mol/L盐酸70.00mL)。通入N2排尽空气后,于260℃加热装置A一段时间,停止加热,冷却,停止通入N2。品红溶液不褪色,取下装置B,加入指示剂,用0.2000mol/L NaOH溶液滴定剩余盐酸,终点时消耗NaOH溶液25.00 mL。经检验滴定后的溶液中无SO42-。
(1)仪器X的名称是________________;
(2)滴定前,下列操作的正确顺序是_________(填字母编号);
a.盛装0.2000mol/L NaOH溶液
b.用0.2000mol/L NaOH溶液润洗
c.读数、记录
d.查漏、清洗
e.排尽滴定管尖嘴的气泡并调整液面
(3)装置B内溶液吸收气体的物质的量是__________mol,
实验2:连接装置A-D-B,检查气密性,按图示重新加入试剂。通入N2排尽空气后,于400℃加热装置A至(NH4)2SO4完全分解无残留物,停止加热,冷却,停止通入N2。观察到装置A、D之间的导气管内有少量白色固体。经检验,该白色固体和装置D内溶液中有SO32-,无SO42-。进一步研究发现,气体产物中无氮氧化物。
(4)检验装置D内溶液中有SO32-,无SO42-的实验操作和现象是__________;
(5)装置B内溶液吸收的气体是____________;
(6)(NH4)2SO4在400℃分解的化学方程式是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 石油分馏、硝基苯的制备和乙烯的制取中温度计的位置都不相同
B. 向苯溴代实验后的溶液中加水,可观察到溶液分三层为有苯层、水层和溴苯层
C. 卤代烃中卤原子的检验,可以向卤代烃水解后的产物中直接滴加![]() 溶液
溶液
D. 乙醇与浓硫酸反应所制得的气体通入到溴水中,若溴水褪色即可证明有乙烯产生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用适量MnO2和10mol/L的盐酸100mL(过量)反应制取Cl2,若反应过程中有0.2mol电子发生转移,求:
(1)生成标准状况下Cl2的体积是多少?
(2)被氧化的HCl占原有HCl的物质的量百分数是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度为T时,在三个容积均为1L的恒容密闭容器中仅发生反应:2SO2(g)+O2(g)![]() 2SO3(g) ΔH<0,达到平衡时,下列说法不正确的是
2SO3(g) ΔH<0,达到平衡时,下列说法不正确的是
容器 编号 | 容器类型 | 起始物质的量 / mol | 平衡时SO3的物质的量 / mol | ||
SO2 | O2 | SO3 | |||
I | 恒温恒容 | 2 | 1 | 0 | 1.8 |
II | 恒温恒压 | 2 | 1 | 0 | a |
III | 绝热恒容 | 0 | 0 | 2 | b |
A. 容器I中SO2的转化率小于容器II中SO2的转化率
B. 容器II的平衡常数大于容器III中的平衡常数
C. 平衡时SO3的物质的量:a>1.8、b>1.8
D. 若起始时向容器I中充入0.10 mol SO2(g)、0.20mol O2(g)和2.0 mol SO3(g),则此时v正<v逆
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KClO3和浓HCl在一定温度下反应会生成黄绿色的易爆物二氧化氯。其反应可表述为:
________KClO3+________HCl(浓) ===________KCl+________ClO2↑+________Cl2↑+________H2O
(1)配平以上化学方程式(写出各物质的化学计量数)。
(2)ClO2是反应的_________(填“氧化”或“还原”)产物。浓盐酸在反应中显示出来的性质是________(填字母)。
a.还原性 b.氧化性 c.酸性 d.碱性
(3)反应产生0.1 mol Cl2,则转移的电子的物质的量为________ mol。
(4)ClO2具有很强的氧化性,因此可被用来做消毒剂,若ClO2作消毒剂后其自身转化为Cl,则其消毒的效率(以单位质量得到电子数表示)是Cl2的________倍(保留2位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】EPR橡胶(![]() )和PC塑料的合成路线如下:
)和PC塑料的合成路线如下:
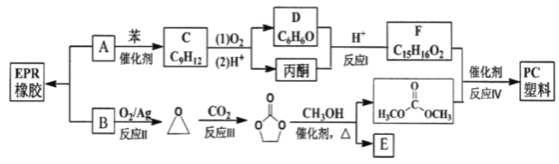
已知:
①![]() +
+![]() +
+![]()
②化合物F能与FeCl3溶液发生显色反应,分子中含有两个化学环境完全相同的甲基,其苯环上的一硝基取代物只有两种。
(1)下列说法正确的是______
A C不能使酸性高锰酸钾溶液褪色
B 反应Ⅱ、Ⅲ的原子利用率为100%
C 1molE与足量的金属钠反应,最多可生成22.4L的H2
D 塑料PC的合成中CH3OH可以循环使用
(2)反应Ⅳ的反应类型为______,F的结构简式为______
(3)反应Ⅳ的化学方程式是______
(4)写出同时满足下列条件的![]() 的所有同分异构体的结构简式(不考虑立体异构)______
的所有同分异构体的结构简式(不考虑立体异构)______
a 属于酯类 b 能发生银镜反应
(5)已知:![]() 以D与乙酸为其实原料合成
以D与乙酸为其实原料合成![]() ,无机试剂任选,写出合成路线(注:合成路线示意图:CH3CHO
,无机试剂任选,写出合成路线(注:合成路线示意图:CH3CHO![]() CH3COOH
CH3COOH![]() CH3COOHCH2CH3)______
CH3COOHCH2CH3)______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列物质能导电的是___,属于电解质的是___。
①NaCl晶体 ②液态SO2 ③液态醋酸 ④铜 ⑤BaSO4固体 ⑥纯蔗糖(C12H22O11) ⑦氨水 ⑧熔化的KNO3
(2)0.5molCH4的质量是___g,在标准状况下的体积为___L;
(3)8.4g氮气和9.6g某单质Rx所含原子个数相同,且分子个数之比为3:2,则x的值是___,R的摩尔质量是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含amol NH4Fe(SO4)2和amol NH4HSO4溶液中逐滴加入bmol Ba(OH)2溶液,请计算
⑴当b=1,a=2时,溶液中产生沉淀的质量是___________g
⑵当b=2.5a时,溶液中产生沉淀的质量是__________________g(用a或b的表达式表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com