
【题目】在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如下图所示,下列表述不正确的是

A. 反应的化学方程式为:3N ![]() 2M
2M
B. t2时,正、逆反应速率不相等
C. t3时,正反应速率等于逆反应速率,达到平衡
D. t1时,N的浓度是M浓度的2倍
【答案】A
【解析】
A、由图像可知:N是反应物、M是生成物,同一时间内物质的量的变化量比为系数比;B、t2时M、N的物质的量相等,但此时M、N的物质的量仍在变化,所以t2时没有达到平衡状态;C、t3后M、N的物质的量不再变化,说明达到平衡状态;D、根据![]() 分析。
分析。
A、由图像可知:N是反应物、M是生成物,同一时间内物质的量的变化量比为系数比,所以反应方程式是2N ![]() M,故A错误;B、t2时M、N的物质的量相等,但此时M、N的物质的量仍在变化,所以t2时没有达到平衡状态,正、逆反应速率不相等,故B正确;C、t3后M、N的物质的量不再变化,说明达到平衡状态,正反应速率等于逆反应速率,故C正确;D、t1时,N、M的物质的量分别是6mol、3mol,根据
M,故A错误;B、t2时M、N的物质的量相等,但此时M、N的物质的量仍在变化,所以t2时没有达到平衡状态,正、逆反应速率不相等,故B正确;C、t3后M、N的物质的量不再变化,说明达到平衡状态,正反应速率等于逆反应速率,故C正确;D、t1时,N、M的物质的量分别是6mol、3mol,根据![]() ,N的浓度是M浓度的2倍,故D正确。
,N的浓度是M浓度的2倍,故D正确。


科目:高中化学 来源: 题型:
【题目】(1)反应3Fe(s)+4H2O(g)![]() Fe3O4(s)+4H2(g)在一容积可变的密闭容器中进行,试回答:
Fe3O4(s)+4H2(g)在一容积可变的密闭容器中进行,试回答:
①增加Fe的量,其反应速率____(填“增大”、“不变”或“减小”,下同)。
②将容器的体积缩小一半,其反应速率____。
③保持体积不变,充入He,其反应速率____。
④保持压强不变,充入He,其反应速率_____。
(2)氨气可作为脱硝剂,在恒温恒容密闭容器中充入一定量的NO和NH3,在一定条件下发生反应:6NO(g)+4NH3(g)![]() 5N2(g)+6H2O(g)。
5N2(g)+6H2O(g)。
①能说明该反应已达到平衡状态的标志是____(填字母序号)
a.反应速率5v(NH3)=4v(N2)
b.单位时间里每生成5mol N2,同时生成4mol NH3
c.容器内N2的物质的量分数不再随时间而发生变化
d.容器内n(NO):n(NH3):n(N2):n(H2O)=6:4:5:6
②某次实验中测得容器内NO及N2的物质的量随时间变化如图所示,图中v(正)与v(逆)相等的点为_____(选填字母)。

(3)298K时,若已知生成标准状况下2.24LNH3时放出热量为4.62kJ。写出合成氨反应的热化学方程式____。
(4)一定条件下,在2L密闭容器内,反应2NO2(g)=N2O4(g)△H=-180kJ·mol-1,n(NO2)随时间变化如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO2)/mol | 0.040 | 0.020 | 0.010 | 0.005 | 0.005 | 0.005 |
用NO2表示0~2s内该反应的平均速度____。在第5s时,NO2的转化率为____。根据上表可以看出,随着反应进行,反应速率逐渐减小,其原因是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】AOH为弱碱,已知:2AOH(aq)+H2SO4(aq)===A2SO4(aq)+2H2O(l) ΔH1=-24.2 kJ·mol-1;H+(aq)+OH-(aq)===H2O(l) ΔH2=-57.3 kJ·mol-1。则AOH在水溶液中电离的ΔH为( )
A. +33.1 kJ·mol-1 B. +45.2 kJ·mol-1 C. -81.5 kJ·mol-1 D. -33.1 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向体积为2 L的固定密闭容器中通入2mol X气体,在一定温度下发生如下反应:2X(g) ![]() Y(g)+3Z(g)ΔH=+92.0kJ· mol-1。经5 min 后反应达到平衡,此时测得容器内的压强为起始时的1.5倍。
Y(g)+3Z(g)ΔH=+92.0kJ· mol-1。经5 min 后反应达到平衡,此时测得容器内的压强为起始时的1.5倍。
(1)用Y表示的化学反应速率为_____,X的转化率为______,平衡时反应吸收的热量为_________。
(2)在定温,定容的条件下向平衡体系中再充入1mol X(g)气体,平衡______(填“正向”“不”“逆向”)移动, X(g)的转化率______(填“增大”“减小”“不变”),Y(g)的质量分数______(填“增大”“减小”“不变”)。
(3)在相同温度,相同容积的密闭容器中起始时充入0.8molX(g),0.6molY(g),1.8molZ(g),此时V正______V逆(填“大于”、“小于”或“等于”);平衡时X(g)的百分含量______ (填“大于”、“小于”或“等于”)原平衡。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,下列溶液的离子浓度关系式正确的是
A. pH=5的H2S溶液中,c(H+)= c(HS-)=1×10—5 mol·L—1
B. pH=a的氨水溶液,稀释10倍后,其pH=b,则a﹤b+1
C. pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+ c(H+)= c(OH-)+c( HC2O4-)+ c( C2O42-)
D. pH相同的①CH3COONa②NaHCO3③NaClO三种溶液的c(Na+):③>②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电镀废水沉泥中含Cu、Ni、Ag和Fe等多种元素的有机金属盐,采用焙烧一浸出—分离回收的工艺流程可有效分离电镀废水沉泥中的金属,其流程如下:
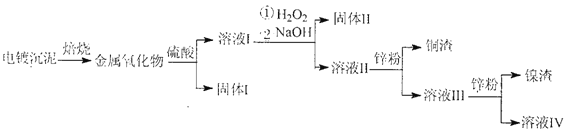
下列叙述错误的是
A. 上述流程中硫酸可以用稀盐酸代替
B. “固体Ⅱ”为Fe(OH)2
C. 溶液III中含有Na+、Ni2+、Zn2+等金属离子
D. 合理处理电镀废沉泥可实现资源的回收与可持续利用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一定条件下N2与H2反应过程中能量变化的曲线图。下列叙述正确的是

A. 该反应的热化学方程式为:N2+3H2![]() 2NH3 △H=-92kJ·mol-1
2NH3 △H=-92kJ·mol-1
B. a曲线是加入催化剂时的能量变化曲线
C. 加入催化剂,该化学反应的反应热将发生改变
D. 在相同温度的条件下,在体积相同I、II两个容器中分别通入1mol N2和3 mol H2,容器I体积恒定,容器II体积可变保持恒压,则反应过程中两容器内的反应速率v(I)<v(II)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、M的原子序数依次增大,其中X、Y、Z 三种元素中,可形成含二种元素的10电子微粒m、n、p、q,且有反应m+n![]() p
p![]() +q;M的最高价氧化物对应的水化物为最强酸。则下列说法正确是
+q;M的最高价氧化物对应的水化物为最强酸。则下列说法正确是
A. 原子半径X<M<Z<Y B. 非金属性X <M<Z<Y
C. X、Y、Z三种元素组成的化合物的水溶液一定呈酸性 D. MZ2可用于自来水的杀菌消毒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列有关叙述正确的是( )
A. 乙烯和丙烯组成的42g混合气体中碳氢键数目为6NA
B. 标准状兄下,22.4L二氯甲烷的分子数约为NA
C. 常温常压下,1mol甲醇完全燃烧生成CO2和H2O,转移的电子数目为12NA
D. 将1molCH3COONa溶于稀醋酸中使溶液呈中性,溶液中CH3COO-数目小于NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com