
【题目】下列物质不是因为发生水解而呈碱性的是( )
A. 醋酸钠B. 苯酚钠C. 草酸钠D. 氢氧化钠
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】一定条件下,可逆反应C(s) + CO2(g) ![]() 2 CO(g) ΔH > 0,达到平衡状态,现进行如下操作:① 升高反应体系的温度;② 增加反应物C的用量;③ 缩小反应体系的体积;④ 减少体系中CO的量。上述措施中一定能使反应的正反应速率显著加快的( )
2 CO(g) ΔH > 0,达到平衡状态,现进行如下操作:① 升高反应体系的温度;② 增加反应物C的用量;③ 缩小反应体系的体积;④ 减少体系中CO的量。上述措施中一定能使反应的正反应速率显著加快的( )
A.①②③④ B.①③ C.④② D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锰元素在溶液中主要以Mn2+(很浅的肉色,近乎无色)、MnO42-(绿色)、MnO4-(紫色)形式存在。MnO2不溶于稀硫酸。
(1)将8 mL 0.1 mol·L-1的酸性高锰酸钾溶液和2 mL l.0mol/L的草酸(H2C2O4)溶液在试管中混合,然后将试管置于25℃水浴中,KMnO4溶液浓度随时间变化关系如下图所示。
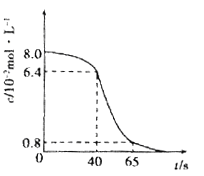
① 写出发生反应的离子方程式:____________
② 计算前40秒用草酸表示的平均反应速率v(草酸)=________________.
③ 40s-65s的反应速率比前40s快,解释原因___________
(2)已知反应3MnO42-+2H2O![]() MnO2+2MnO4-+4OH-。
MnO2+2MnO4-+4OH-。
① 向MnO4-溶液中加入足量稀硫酸,可观察到的现象是__________.
② 常温下,在0.512 mol/L K2MnO4溶液中,当pH=14时K2MnO4的转化率为4/9,则该反应的平衡常数的值为__________
③ 在其他条件不变的条件下,适当升温有利于降低K2MnO4的转化率,则该反应的△H___0(填“大于” “小于”或“等于”)。
(3)碳酸锰是一种重要的工业原料。工业生产中常用复分解法生产MnCO3:
MnSO4+2NH4HCO3=MnCO3↓+(NH4)2SO4+CO2↑+H2O。反应中通常需加入稍过量的NH4HCO3,且控制溶液的pH为6.8-7.4. 溶液的pH不能过低也不能过高,原因是_______。设MnSO4溶液为0.19mol/L,则溶液的pH 最高不能超过_________。
[己知MnCO3、Mn(OH)2的Ksp分别为l.8×10-11和1.9×10-13]
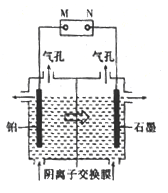
(4)制备单质锰的实验装置如图,阳极以稀硫酸为电解液,阴极以硫酸锰和硫酸混合液为电解液,电解装置中“![]() ”表示溶液中阴离子移动的方向。铂电极的电极反应式为______。
”表示溶液中阴离子移动的方向。铂电极的电极反应式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用1 L 1 molL-1 NaOH溶液吸收0.8 mol CO2,所得溶液中Na2CO3和NaHCO3的物质的量之比约为
A. 1∶3 B. 1∶2 C. 2∶3 D. 3∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将6.48g含有C、H、O的有机物M,装入元素分析装置,通入足量的O2使它完全燃烧,将生成的气体依次通过氯化钙干燥管A和碱石灰干燥管B.测得A管质量增加了4.32g,B管增加了18.48g,已知该有机物的相对分子质量为108。
(1) 燃烧此化合物6.48g,须消耗氧气的质量是多少?
(2) 求此化合物M的分子式?
(3) 该有机物1分子中有1个苯环,试写出一种满足条件的M的结构简式。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系)。
实验步骤 | 实验现象 |
①将镁条用砂纸打磨后,放入沸水中;再向溶液中滴加酚酞溶液 | A. 有气体产生,溶液变成浅红色 |
②向新制得的Na2S溶液中滴加新制的氯水 | B. 生成淡黄色沉淀 |
③将一小块金属钠放入滴有酚酞溶液的冷水中 | C. 浮在水面上,熔成小球,做不定向移动,随之消失,溶液变成红色 |
④将镁条投入稀盐酸中 | D. 剧烈反应,迅速产生大量无色气体 |
⑤将铝条投入稀盐酸中 | E. 反应不十分剧烈,产生无色气体 |
请你帮助该同学整理并完成实验报告。
(1)实验目的:认识同周期元素性质的递变规律
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlCl3溶液,NaOH溶液等。
仪器:试管,滴管,酒精灯,试管夹,镊子,小刀,玻璃片,砂纸等。
(3)实验内容:(填写与实验步骤对应的实验现象的标号和化学方程式)
实验内容 | 化学方程式 |
____________________ | |
____________________ | |
____________________ | |
____________________ | |
____________________ |
(4)实验结论:__________________________________________________
(5)请用原子结构的知识简单解释上述结论:__________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于原电池的电极名称,叙述错误的是( )
A. 发生氧化反应的一极为负极B. 正极为电子流入的一极
C. 比较不活泼的金属为负极D. 电流流出的一极为正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,可逆反应X(g) + 3Y(g) ![]() 2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0,单位mol/L),当达平衡时X、Y、Z的浓度分别为0.1mol/L,0.3mol/L,0.08mol/L,则下列判断不合理的是
2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0,单位mol/L),当达平衡时X、Y、Z的浓度分别为0.1mol/L,0.3mol/L,0.08mol/L,则下列判断不合理的是
A.c1:c2 = 1:3 B.平衡时,Y和Z的生成速率之比为3:2
C.X、Y的转化率不相等 D.c1的取值范围为0 < c1 < 0.14mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com