
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ |
分析 (1)由元素在周期表中位置,可知①为N、②为F、③为Na、④为Mg、⑤为Al、⑥为Si、⑦为S、⑧为Cl、⑨为Ar,⑩为K,⑪为Br;
(2)最活泼的金属为K,与水反应生成氢氧化钾与氢气;
(3)最高价氧化物的水化物酸性最强的是高氯酸,碱性最强的是氢氧化钾;
(4)同周期自左而右原子半径减小,同主族自上而下原子半径增大;
(5)F2与氢氧化钠反应生成OF2,由电荷守恒可知生成NaF,同时生成水;
(6)二氧化硫通入硝酸钡溶液中,酸性条件下硝酸根具有强氧化性,反应生成硫酸钡沉淀与NO.
解答 解:(1)由元素在周期表中位置,可知①为N、②为F、③为Na、④为Mg、⑤为Al、⑥为Si、⑦为S、⑧为Cl、⑨为Ar,⑩为K,⑪为Br,
故答案为:Mg;
(2)最活泼的金属为K,与水反应生成氢氧化钾与氢气,反应离子方程式为:2K+2H2O=2K ++2OH-+H2↑,
故答案为:2K+2H2O=2K ++2OH-+H2↑;
(3)最高价氧化物的水化物酸性最强的是HClO4,K的金属性最强,故碱性最强的是KOH,
故答案为:HClO4;KOH;
(4)同周期自左而右原子半径减小,同主族自上而下原子半径增大,故F原子半径最小,K原子半径最大,
故答案为:F;K;
(5)F2与氢氧化钠反应生成OF2,由电荷守恒可知生成NaF,同时生成水,反应方程式为:2F2+2OH-=OF2+2F-+H2O,
故答案为:2F2+2OH-=OF2+2F-+H2O;
(6)二氧化硫通入硝酸钡溶液中,酸性条件下硝酸根具有强氧化性,反应生成硫酸钡沉淀与NO,反应离子方程式为:3SO2+2NO3-+3Ba2++2H2O=3BaSO4↓+2NO↑+4H+,
故答案为:3SO2+2NO3-+3Ba2++2H2O=3BaSO4↓+2NO↑+4H+.
点评 本题考查元素周期表与元素周期律综合运用,熟练掌握周期表的结构,侧重常用化学用语、元素周期律以及学生分析解决问题的能力的考查.


科目:高中化学 来源: 题型:解答题
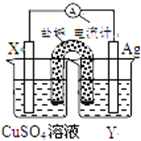 依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.
依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH═CH(OH2)2CH3 | B. | CH2═CH(CH2)2CH3 | ||
| C. | CH3CH═CH-CH═CHCH3 | D. | CH3CH2═CHCH2CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O2分子中含有极性键和非极性键 | |
| B. | 向其溶液加入少量MnO2和FeCl3等能加快反应 | |
| C. | H2O2分子中所有原子都达8电子结构 | |
| D. | 该反应中H2O2是氧化剂也是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不粘锅的原料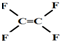 为烃类化合物 为烃类化合物 | |
| B. | 分子组成相差1个或若干个“CH2”原子团的有机物,互称为同系物 | |
| C. | 石油分馏是物理变化,煤的气化、液化是化学变化 | |
| D. | 油脂在酸性或碱性条件下都能发生水解反应制取肥皂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO3-、OH-、Na+ | B. | Fe2+、OH-、NO3- | C. | Fe2+、H+、Cl- | D. | Fe2+、H+、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ① | ⑦ | ④ | ||||
| 3 | ③ | ⑤ | ⑧ | ⑩ | ||||
| 4 | ② | ⑨ |
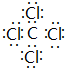 .
.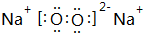 ;④⑧⑨元素的离子的还原性由强到弱顺序为Br->Cl->F-(用离子符号).
;④⑧⑨元素的离子的还原性由强到弱顺序为Br->Cl->F-(用离子符号).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C21H33COOC2H5 | B. | C21H31COOC2H5 | C. | C22H33COOC2H5 | D. | C22H39COOC2H5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com