
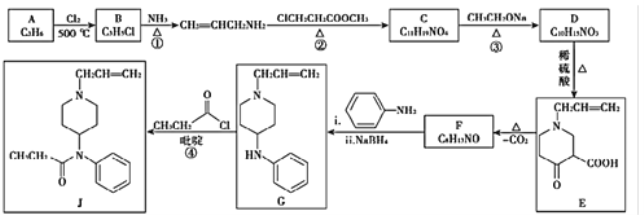
【题目】新合成的药物J的合成方法如图所示:
已知:R1—NH—R2+Cl—R3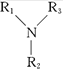
![]() +HCl
+HCl
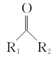
R1COOR2+R3CH2COOR4![]()
![]() +R2OH
+R2OH
![]()
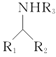 (R1、R2、R3、R4为氢或烃基)
(R1、R2、R3、R4为氢或烃基)
回答下列问题:
(1)B的化学名称为______________,F的结构简式为_____________
(2)有机物CH2=CHCH2NH2中的官能团名称是_______,由A生成B的反应类型为_____
(3)③的化学方程式为__________。
(4)已知④有一定的反应限度,反应进行时加入吡啶(C5H5N,属于有机碱)能提高J的产率,原因是________。
(5)有机物K分子组成比F少两个氢原子,符合下列要求的K的同分异构体有_________种(不考虑立体异构)。
①遇FeCl3溶液显紫色
②苯环上有两个取代基
(6)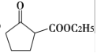 是一种重要的化工中间体。以环已醇(
是一种重要的化工中间体。以环已醇(![]() )和乙醇为起始原料,结合已知信息选择必要的无机试剂,写出制备
)和乙醇为起始原料,结合已知信息选择必要的无机试剂,写出制备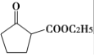 的合成路线:_________________。(已知:RHC=CHR'
的合成路线:_________________。(已知:RHC=CHR'![]() RCOOH+R'COOH,R、R'为烃基。用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
RCOOH+R'COOH,R、R'为烃基。用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
【答案】3-氯-1-丙烯 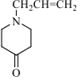 碳碳双键和氨基 取代反应
碳碳双键和氨基 取代反应 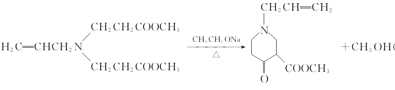 吡啶显碱性,能与反应④的产物HCl发生中和反应,使平衡正向移动,提高J产率 15
吡啶显碱性,能与反应④的产物HCl发生中和反应,使平衡正向移动,提高J产率 15 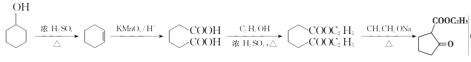
【解析】
由A、B的分子式,C的结构简式,可知A为CH3CH=CH2,A发生取代反应生成B为ClCH2CH=CH2;B中氯原子被氨基取代得到![]() , 根据C的分子式既反应条件,可知反应②发生题给信息中的取代反应,可知C为
, 根据C的分子式既反应条件,可知反应②发生题给信息中的取代反应,可知C为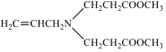 ;比较C、D分子式,结合E的结构简式分析,反应③为题给信息中的成环反应,可知D为
;比较C、D分子式,结合E的结构简式分析,反应③为题给信息中的成环反应,可知D为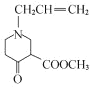 ;D发生酯的水解反应生成E,比较E和G的结构,结合反应条件分析中间产物F的结构为
;D发生酯的水解反应生成E,比较E和G的结构,结合反应条件分析中间产物F的结构为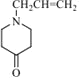 ;对比G、J的结构,G与
;对比G、J的结构,G与![]() 发生取代反应生成J,据此分析解答。
发生取代反应生成J,据此分析解答。
(1)B为ClCH2CH=CH2,化学名称为3-氯-1-丙烯,比较E和G的结构,结合反应条件分析中间产物F的结构为 故答案为:3-氯-1-丙烯;
故答案为:3-氯-1-丙烯; ;
;
(2)根据官能团的结构分析,有机物CH2=CHCH2NH2中的官能团有碳碳双键和氨基;比较A和B的结构变化可知该反应为取代反应,故答案为:碳碳双键和氨基;取代反应;
(3)根据上述分析,反应③的化学方程式为 ,故答案为:
,故答案为: ;
;
(4)反应④为取代反应,生成有机物的同时可生成HCl,而吡啶呈碱性,可与HCl发生中和反应,使平衡正向移动,提高J的产率,故答案为:吡啶显碱性,能与反应④的产物HCl发生中和反应,使平衡正向移动,提高J产率;
(5)F为 ,分子式为C8H13NO,则K的分子式为C8H11NO,①遇FeCl3溶液显紫色,则结构中含有酚羟基;②苯环上有两个取代基,一个为OH,则另一个为由2个C原子6个H原子1个N原子构成的取代基,其结构有-CH2CH2NH2、-CH2NHCH3、-CH(CH3)NH2、-NHCH2CH3、-N(CH3)2共5种,两取代基的位置共有邻、间、对三种情况,所以K的同分异构体有3×5=15种,故答案为:15;
,分子式为C8H13NO,则K的分子式为C8H11NO,①遇FeCl3溶液显紫色,则结构中含有酚羟基;②苯环上有两个取代基,一个为OH,则另一个为由2个C原子6个H原子1个N原子构成的取代基,其结构有-CH2CH2NH2、-CH2NHCH3、-CH(CH3)NH2、-NHCH2CH3、-N(CH3)2共5种,两取代基的位置共有邻、间、对三种情况,所以K的同分异构体有3×5=15种,故答案为:15;
(6)由题给信息可知,由![]() 反应得到
反应得到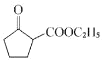
![]() 用酸性高锰酸钾溶液氧化的己二酸,己二酸与乙醇发生酯化反应得到
用酸性高锰酸钾溶液氧化的己二酸,己二酸与乙醇发生酯化反应得到![]() ,
,![]() 可由原料
可由原料![]() 发生消去反应获取,则合成路线流程图为:
发生消去反应获取,则合成路线流程图为: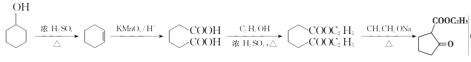 ,故答案为:
,故答案为: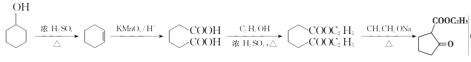 。
。


科目:高中化学 来源: 题型:
【题目】砷及其化合物有着广泛的用途。砷有两种常见的弱酸,砷酸(H3AsO4)和亚砷酸(H3AsO3)。已知砷酸(H3AsO4)的pKa1、pKa2、pKa3依次为2.25、6.77、11.40(pKa=-lgKa)。回答下列问题:
(1)已知:As(s)+![]() H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+![]() O2(g)=H2O(l) ΔH2
O2(g)=H2O(l) ΔH2
As(s)+![]() O2(g)=
O2(g)=![]() As2O5(s) ΔH3
As2O5(s) ΔH3
则反应As2O5(s)+3H2O(l)=2H3AsO4(s) ΔH=______。
(2)写出砷酸(H3AsO4)的第二步电离方程式_______。
(3)NaH2AsO4溶液呈___(填“酸性”“中性”或“碱性”),试通过计算说明_______。
(4)亚砷酸(H3AsO3)水溶液中存在多种微粒形态,各种微粒分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与溶液的pH关系如图所示。
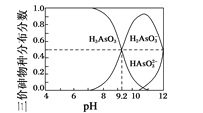
以酚酞为指示剂(变色范围pH 8.2~10.0),将NaOH溶液逐滴加入到H3AsO3溶液中,当溶液由无色变为浅红色时停止滴加。该过程中主要反应的离子方程式为_______。
(5)某化学兴趣小组同学欲探究可逆反应:AsO33-+I2+2OH-![]() AsO43-+2I-+H2O。设计图Ⅱ所示装置。实验操作及现象:按图Ⅱ装置加入试剂并连接装置,电流由C2流入C1。当电流变为零时,向图Ⅱ装置左边烧杯中逐滴加入一定量2 mol·L-1盐酸,发现又产生电流,实验中电流与时间的关系如图Ⅲ所示。
AsO43-+2I-+H2O。设计图Ⅱ所示装置。实验操作及现象:按图Ⅱ装置加入试剂并连接装置,电流由C2流入C1。当电流变为零时,向图Ⅱ装置左边烧杯中逐滴加入一定量2 mol·L-1盐酸,发现又产生电流,实验中电流与时间的关系如图Ⅲ所示。
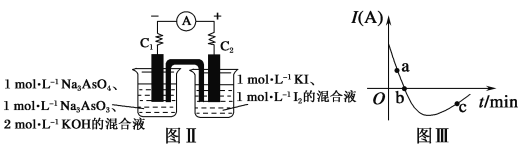
①图Ⅲ中AsO43-的逆反应速率:a__(填“>”“<”或“=”)b。
②写出图Ⅲ中c点对应图Ⅱ装置的正极反应式______。
③能判断该反应达到平衡状态的是__。
a 2v(I-)正=v(AsO33-)逆 b 溶液的pH不再变化
c 电流表示数变为零 d 溶液颜色不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重铬酸钾常用作有机合成的氧化剂和催化剂等。由含铬废液(主要含Cr3+、Fe3+、K+、SO42-等)制备K2Cr2O7的流程如图所示。

已知:i.在酸性条件下,H2O2能将Cr2O72-还原为Cr3+。
ii.相关金属离子形成氢氧化物沉淀的pH范围如下:
金属离子 | Fe3+ | Cr3+ |
开始沉淀的pH | 1.5 | 4.9 |
沉淀完全的pH | 2.8 | 6.8 |
回答下列问题:
(1)滤渣①的主要成分为_________(填化学式)。
(2)"氧化”步骤中发生反应的离子方程式为____________。
(3)“加热"操作的目的是_________。
(4)“酸化"过程中发生的反应为2CrO42- +2H+![]() Cr2O72-+ H2O (K=4.0×1014L3·mol -3)。已知“酸化”后溶液(pH=1)中c(Cr2O72- )=6. 4×10-3 mol·L-1,则溶液中c(CrO42-)=_______。
Cr2O72-+ H2O (K=4.0×1014L3·mol -3)。已知“酸化”后溶液(pH=1)中c(Cr2O72- )=6. 4×10-3 mol·L-1,则溶液中c(CrO42-)=_______。
(5)可利用微生物电池将镀铬废水中的Cr2O72-催化还原,其工作原理如图所示:
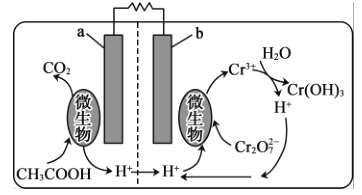
在该电池中,b作______极,a极的电极反应为__________
(6)K2 Cr2O7标准溶液还可用于测定市售硫代硫酸钠晶体(Na2S2O3·5H2O,M=248 g·mol -1)的纯度。测定步骤如下:
i.溶液配制:称取1.2400g市售硫代硫酸钠晶体样品,用新煮沸并冷却的蒸馏水在烧杯中溶解,完全溶解后.全部转移至100mL容量瓶中.加蒸馏水至刻度线。
ii.滴定:取0.01000 mol. L-1的K2Cr2 O7标准溶液20. 00 mL,稀硫酸酸化后加入过量KI溶液,发生反应(Cr2O72-被还原成Cr3+ ,I-被氧化成I2)。然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:I2+2S2O32 - =S4O62-+2I-。加入淀粉溶液作为指示剂,继续滴定,当溶液蓝色褪去.即为终点。平行滴定3次,样品溶液的平均用量为25.00mL。
①稀硫酸酸化的K2Cr2O7标准溶液与KI溶液反应的离子方程式为_________
②该市售硫代硫酸钠晶体样品的纯度为_______%(保留1位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于苯的叙述正确的是( )
A.苯的分子式为C6H6,它不能使酸性KMnO4溶液褪色,属于饱和烃
B.从苯的凯库勒式(![]() )看,苯分子中含有碳碳双键,应属于烯烃
)看,苯分子中含有碳碳双键,应属于烯烃
C.在催化剂作用下,苯与液溴反应生成溴苯,发生了加成反应
D.苯分子为平面正六边形结构,6个碳原子之间的价键完全相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按官能团的不同,可以对有机物进行分类,请指出下列有机物的种类(填写字母),填在横线上。
(1)CH3CH2CH2COOH____;(2)![]() ____;(3)
____;(3)![]() ____;(4)
____;(4)![]() ____;(5)
____;(5)![]() ____;(6)
____;(6)![]() ____。
____。
A.烷烃 B.烯烃 C.炔烃 D.醚 E.酚 F.醛 G.羧酸 H.芳香烃 I.酯 J.卤代烃 K.醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是
A. 向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
B. 0.1mol/LNa2CO3溶液与0.1mol/LNaHCO3溶液等体积混合:2c(Na+)=3c(CO32-)十3c(HCO3-)+3c(H2CO3)
C. 0.1mol/LNH4Cl溶液与0.1mol/L氨水等体积混合(pH>7):c(NH3·H2O)>c(NH4+)>c(Cl-)>c(OH-)
D. 0.1mol/LNa2C2O4溶液与0.1mol/LHCl溶液等体积混合(H2C2O4为二元弱酸):2c(C2O42-)+c(HC2O4-)+c(OH-)=c(Na+)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制得的乙炔中常混有H2S、PH3等杂质气体。如图是两学生设计的实验装置,用来测定CaC2样品的纯度,右边的反应装置相同而左边的气体发生装置则不同,分别如Ⅰ和Ⅱ所示。
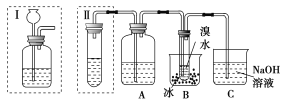
(1)A瓶中的液体可以从酸性KMnO4溶液和FeCl3溶液中选择,应该选择________,它的作用是___________________________。
(2)装置Ⅰ的主要缺点是______________________________________。
(3)装置Ⅱ的主要缺点是_____________________;
若选用此装置来完成实验,则应采取的措施是___________________。
(4)若称取a g CaC2,反应完全后,测得B处溴水增重b g,则CaC2的纯度为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在t℃下,某反应达到平衡,平衡常数K=![]() 。恒容时,温度升高时NO浓度减小。下列 说法正确的是
。恒容时,温度升高时NO浓度减小。下列 说法正确的是
A.该反应的焓变为正值
B.若恒温下增大压强(缩小体积),则反应体系的颜色加深
C.在t℃时,加入催化剂,该反应的化学平衡常数增大
D.该反应化学方程式为NO+SO3![]() NO2+SO2
NO2+SO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com