
【题目】医生建议因缺少某种元素而导致甲状腺肿大的病人多吃海带,这是由于海带中含有较丰富的( )
A. 碘元素 B. 铁元素 C. 钾元素 D. 锌元素
科目:高中化学 来源: 题型:
【题目】以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等.实验室模拟工业以硫酸渣制备铁红(Fe2O3),过程如图:

(1)硫酸渣的成分中既能与酸又能与碱反应的是 ,写出酸溶过程Fe2O3与稀硫酸反应的离子反应方程式: .
(2)生产过程中,为了确保铁红的纯度,氧化过程需要调节溶液的pH的范围是 (部分阳离子以氢氧化物形式沉淀时溶液的pH见表)
沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
开始沉淀 | 2.7 | 3.8 | 7.5 | 9.4 |
完全沉淀 | 3.2 | 5.2 | 9.7 | 12.4 |
(3)滤渣A的主要成分为 ,滤液B含有的主要物质有 .
(4)如何证明洗涤环节充分洗净 .
(5)已知硫酸渣质量为a kg,假设铁红制备过程中铁元素损耗25%,最终得到铁红的质量为b kg,则原来硫酸渣中铁元素质量分数为 .(用题中所给数据计算并用最简整数比表示结果)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关甲烷分子结构的说法中,错误的是 ( )
A.甲烷分子中含有4个C—H共价健
B.甲烷分子中C—H共价键的夹角为109°28'
C.甲烷是正四面体结构
D.甲烷是一种直线型分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的镁、铜合金加入到稀硝酸溶液中,两者恰好完全反应,假设反应过程中还原产物全部是NO,向所得溶液中加入物质的量浓度为3molL﹣1的NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1g,则下列有关叙述中正确的是( )
A.开始加入合金的质量可能为3.6g
B.参加反应的硝酸的物质的量为0.1mol
C.沉淀完全时消耗NaOH溶液的体积为100mL
D.溶解合金时产生NO的体积为2.24L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【改编题】不规范的实验操作都有安全隐患,进入高中后化学实验明显增多,作为高中生实验时要规范操作。请改正下列各操作中的错误(在下图对应的横线上用文字简要回答)。
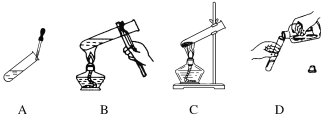
A.________________________________________________________________________
B.________________________________________________________________________
C.________________________________________________________________________
D.________________________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 分子数为NA的CO和C2H4混合气体的体积约为22.4 L
B. 标准状况下,4.48 L重水(D2O)中含有的中子数为2NA
C. 用MnO2与浓盐酸制取Cl2时,每生成0.5mol Cl2则转移电子数为NA
D. 0.1 L 3.0 mol·L-1的NH4NO3溶液中含有NH![]() 的数目为0.3NA
的数目为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属在现代社会中发挥着巨大的作用,铝的化合物在工农业生产及人们的日常生活中也具有广泛地作用。
(1)若将铝溶解,下列试剂中最好选用________(填选项字母)。
A.浓硫酸B.稀硫酸C.稀硝酸
(2)以铝土矿(主要成分是Al2O3,杂质有SiO2、Fe2O3等)为原料,采用拜耳法生产Al2O3的流程如下图所示:
①Al2O3可用于电解制Al,电解时需加入冰晶石(Na3AlF6)作为助熔剂,用NaF和Al2(SO4)3反应制备冰晶石的化学方程式为________________;电解时用石墨作阳极,温度维持在950~970℃,阳极需定期更换,其原因为________________________。
②赤泥中铝硅酸钠的化学式可表示为:3Na2O·3Al2O3·5SiO2·5H2O,则滤液I的主要成分是________________;铝土矿的品位常用铝硅比(A/S,即矿石中Al2O3与SiO2的质量比)来衡量。某种铝土矿的A/S=10.2,则加入足量NaOH溶液后铝的理论溶出率为________________。
③该生产过程中,需向沉淀池中加入过量的X,该反应的离子方程式为________________。
(3)铍(Be)与铝元素相似,其氧化物及氢氧化物具有两性,请写出BeO与盐酸反应的离子方程式,Be(OH)2溶于NaOH溶液的化学方程式为:Be(OH)2+2NaOH=Na2BeO2+2H2O,往10.0mL1.00mol·L-1的Be(NO3)2溶液中逐滴加入等浓度的NaOH溶液,请在以下坐标图中画出沉淀量随NaOH溶液加入量的变化图:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com