
利用下列实验装置不能完成相应实验的是 ( )。

A.用装置①测量生成 氧气的化学反应速率
氧气的化学反应速率
B.用装置②比较NaHCO3和Na2CO3的热稳定性
C.装置③中分液漏斗内的液体可顺利加入蒸馏烧瓶
D.装置④可实现制取CO2实验中的“即关即止,即开即用”的作用
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:
向过氧化氢溶液中逐渐滴入FeCl2溶液,可能观察到的现象有 ( )
A.有白色沉淀生成,溶液颜色由浅绿色变棕色
B.有红褐色沉淀生成,上层溶液呈棕黄色
C.有无色无味的气体产生,该气体能使带火星的木条复燃
D.能看到溶液颜色加深,既无沉淀产生,也无气体放出
查看答案和解析>>
科目:高中化学 来源: 题型:
电解法促进橄榄石(主要成分是Mg2SiO4)固定CO2的部分工艺流程如下:
已知:Mg2SiO4(s) +4HCl(aq) 2MgCl2(aq) +SiO2 (s) + 2H2O(l) △H =-49.04 kJ·mol-1
2MgCl2(aq) +SiO2 (s) + 2H2O(l) △H =-49.04 kJ·mol-1
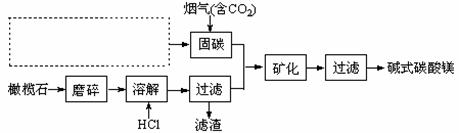
(1)某橄榄石的组成是Mg9FeSi5O20,用氧化物的形式可表示为 ▲ 。
(2)固碳时主要反应的方程式为NaOH(aq)+CO2 (g)=NaHCO3 (aq),该反应能自发进行的原因是 ▲ 。
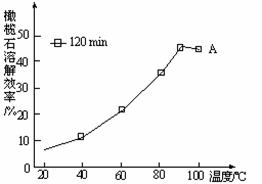 (3)请在上图虚框内补充一步工业生产流程 ▲ 。
(3)请在上图虚框内补充一步工业生产流程 ▲ 。
(4)下列物质中也可用作“固碳”的是 ▲ 。
(填字母)
a.CaCl2 b.H2NCH2COONa c.(NH4)2CO3
(5)由图可知,90℃后曲线A溶解效率下降,分
析其原因 ▲ 。
(6)经分析,所得碱式碳酸镁产品中含有少量NaCl和Fe2O3。为提纯,可采取的措施依次为:对溶解后所得溶液进行除铁处理、对产品进行洗涤处理。判断产品洗净的操作是 ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
普罗帕酮为广谱高效抗心律失常药,它可由有机物X经多步反应合成:
|
|

下列有关说法正确的是
A.在有机物X的1H核磁共振谱图中,有4组特征峰
B.可用溴水或FeCl3溶液鉴别X和Y
C.普罗帕酮分子中有2个手性碳原子
D.X、Y和普罗帕酮都能发生加成、水解、氧化、消去反应
查看答案和解析>>
科目:高中化学 来源: 题型:
硫代硫酸钠(Na2S2O3)俗称保险粉,可用于照相业作定影剂,也可用于纸浆漂白
作脱氯剂等。实验室可通过如下反应制取:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2。

(1)用图5所示装置制取Na2S2O3,其中NaOH溶液的作用是 ▲ 。如将分液漏斗中的H2SO4
改成浓盐酸,则三颈烧瓶内除Na2S2O3生成外,还有 ▲ (填化学式)杂质生成。
(2)为测定所得保险粉样品中Na2S2O3·5H2O的质量分数,可用标准碘溶液进行滴定,反
应方程式为2Na2S2O3+I2=2NaI+Na2S4O6。
①利用KIO3、KI和HCl可配制标准碘溶液。写出配制时所发生反应的离子方程式: ▲ 。
②准确称取一定质量的Na2S2O3·5H2O样品于锥形瓶中,加水溶解,并滴加 ▲ 作
指示剂,滴定终点的现象是 ▲ 。
③若滴定时振荡不充分,刚看到溶液局部变色就停止滴定,则测量的Na2S2O3·5H2O的
质量分数会 ▲ (填“偏高”、“偏低”或“不变”)。
(3)本实验对Na2S的纯度要求较高,利用图6所示的装置可将工业级的Na2S提纯。已知Na2S
常温下微溶于酒精,加热时溶解度迅速增大,杂质不溶于酒精。提纯步骤依次为:
①将已称量好的工业Na2S放入圆底烧瓶中,并加入一定质量的酒精和少量水;
②按图6所示装配所需仪器,向冷凝管中通入冷却水,水浴加热;
③待烧瓶中固体不再减少时,停止加热,将烧瓶取下;
④趁热过滤;
⑤ ▲ ;
⑥将所得固体洗涤、干燥,得到Na2S·9H2O晶体。
查看答案和解析>>
科目:高中化学 来源: 题型:
某校化学实验小组为了证明铜与稀硝酸反应产生一氧化氮,用如图所示装置进行实验(加热装置和夹持装置均已略去,装置气密性良好,F是用于鼓入空气的双连打气球)。
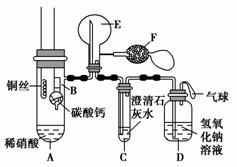
实验操作及现象:
| 实验操作 | 现象 |
| Ⅰ.将B装置下移,使碳酸钙与稀硝酸接触 | 产生气体 |
| Ⅱ.当C装置中产 | |
| Ⅲ.将A装置中铜丝放入稀硝酸中,给A装置微微加热 | A装置中产生无色气体 E装置中开始时出现浅红棕色气体 |
| Ⅳ.用F装置向E装置中鼓入空气 | E装置内气体颜色逐渐加深 |
| Ⅴ.一段时间后 | C装置中白色沉淀溶解 |
试回答下列问题:
(1)操作Ⅰ中产生气体的化学式为___________________________________;
操作Ⅰ的目的是_________________________________________________;
D装置的作用是_________________________________________________。
(2)C装置中白色沉淀的化学式是___________________________________,
操作Ⅱ中当C装置中产生白色沉淀时立刻将B装置上提的原因是_________________________________________________________________。
(3)操作Ⅲ中A装置中产生无色气体的化学方程式是_____________________ _________________________________________________________________。
(4)E装置内气体颜色逐渐加深的原因是__________________________ ________________________________________ _________________________。
_________________________。
(5)操作Ⅴ现象产生的原因是(用化学方程式说明)________________________ _________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、R、W是5种短周期元素,原子序数依次增大;它们可组成离子化合物Z2Y和共价化合物RY3、XW4;已知Y、R同主族, Z、R 、W同周期。下列说法错误的是( )
A.原子半径:Z>R>W
B.W的气态氢化物稳定性强于R的气态氢化物
C.XW4分子中各原子均满足8电子结构
D.Y、Z、R三种元素组成的化合物水溶液一定显碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
一种一元强酸HA溶液中加入一种碱MOH,溶液呈中性,下列判断正确的是
A.加入的碱过量 B.反应后溶液中c(A-)= c(M+)
C.生成的盐发生水解 D.混合前酸与碱中溶质的物质的量相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com