
【题目】辉铜矿石主要含有硫化亚铜(Cu2S)及少量脉石(SiO2).一种以辉铜矿石为原料制备硝酸銅的工艺流程如下所示:

(1)写出“浸取”过程中Cu2S溶解时发生反应的离子方程式:_________。
(2)“矿渣”中除了S以外,还有_______(填化学式);“回收S”"过程中温度控制在50~60℃之间,不宜过高或过低的原因是_________ 。
(3)“保温除铁”过程中,加入CuO的目的是_________;“蒸发浓缩、冷却结晶”过程中,要用HNO3溶液调节溶液的pH,其理由是_________ 。
(4)气体NOx与氧气混合后通入水中能生成流程中可循环利用的一种物质,该反应的化学方程式为________________;向“滤液M”"中加入(或通入)________ (填字母代号),可得到另一种流程中可循坏利用的物质。
A.铁 B.氯气 C.高锰酸钾
【答案】 Cu2S+4Fe3+=2Cu2++4Fe2++S SiO2 温度过高苯易挥发,温度过低矿渣中硫的溶解速率或溶解度小 调节溶液的pH,促进Fe3+水解平衡正向移动,生成Fe(OH)3沉淀 抑制Cu2+的水解 4NOx+(5-2x)O2+2H2O=4HNO3 B
【解析】考查化学工艺流程,(1)Cu2S中Cu显+1价,S显-2价,都具有还原性,FeCl3中Fe3+具有强氧化性,根据流程,浸取发生的离子反应是Cu2S+4Fe3+=2Cu2++4Fe2++S;(2)根据辉铜矿的成分,含有少量的脉石,SiO2不与FeCl3发生反应,因此矿渣中还含有SiO2;苯的沸点较低,温度过高,苯易挥发,温度过低,反应速率慢或溶解度小;(3)置换过程过滤后,得到固体物质是Cu和Fe,Cu和Fe与硝酸反应生成Cu(NO3)2和Fe(NO3)3,Fe3+水解:Fe3++3H2O ![]() Fe(OH)3+3H+,加入CuO的目的是调节件pH,促使Fe3+水解,生成氢氧化铁沉淀;Cu(NO3)2溶液中Cu2+发生水解,Cu2++2H2O=Cu(OH)2+2H+,加入硝酸,抑制Cu2+水解;(4)氮的氧化物与氧气、H2O反应生成HNO3,硝酸是循环利用的一种物质,该反应的化学方程式为4NOx+(5-2x)O2+2H2O=4HNO3;置换中发生Fe+CuCl2=FeCl2+Cu、Fe+2FeCl3=3FeCl2,滤液M中成分是FeCl2,根据流程图,FeCl3是循环物质,即需要加入Cl2,把FeCl2氧化成FeCl3,故选项B正确。
Fe(OH)3+3H+,加入CuO的目的是调节件pH,促使Fe3+水解,生成氢氧化铁沉淀;Cu(NO3)2溶液中Cu2+发生水解,Cu2++2H2O=Cu(OH)2+2H+,加入硝酸,抑制Cu2+水解;(4)氮的氧化物与氧气、H2O反应生成HNO3,硝酸是循环利用的一种物质,该反应的化学方程式为4NOx+(5-2x)O2+2H2O=4HNO3;置换中发生Fe+CuCl2=FeCl2+Cu、Fe+2FeCl3=3FeCl2,滤液M中成分是FeCl2,根据流程图,FeCl3是循环物质,即需要加入Cl2,把FeCl2氧化成FeCl3,故选项B正确。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】金刚烷是一种重要的化工原料,工业上可通过下列途径制备:

请回答下列问题:
(1)环戊二烯分子中最多有 __________个原子共平面;
(2)金刚烷的分子式为 ____________ ;
(3)下面是以环戊烷为原料制备环戊二烯的合成路线:

其中,反应①的产物名称是 __________,反应②的反应试剂和反应条件是 __________。
(4)已知烯烃能发生如下反应:

请写出下列反应产物的结构简式:
![]()
![]() ____________________________________。
____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第23号元素钒在地壳中的含量大约为0.009%,在过渡元素中仅次于Fe、Ti、Mn、Zn,排第五位。我国四川攀枝花地区蕴藏着极其丰富的钒钛磁铁矿。
(1)钒在周期表中的位置为__________,电子占据的最高能层的轨道形状为__________。
(2)在地壳中含量最高的五种过渡金属元素Fe、Ti、Mn、Zn、V中,基态原子核外单电子数最多的是__________。
(3)过渡金属可形成许多羰基配合物,即CO作为配体形成的配合物。
①CO的等电子体有N2、CN-、__________(任写一个)等。
②CO作配体时,配位原子是C而不是O,其原因是__________。
(4)过渡金属配合物常满足“18电子规则”,即中心原子的价电子数加上配体提供的电子数之和等于18,如[Fe(CO)5]、[Mn(CO)5]-等都满足这个规则。
①下列钒配合物中,钒原子满足18电子规则的是__________。
A.[V(H2O)6]2+ B.[V(CN)6]4- C.[V(CO)6]- D.[V(O2)4]3-
②化合物 的熔点为138 ℃,其晶体类型为__________;已知该化合物满足18电子规则,其配体“
的熔点为138 ℃,其晶体类型为__________;已知该化合物满足18电子规则,其配体“![]() ”中的大π键可表示为__________。
”中的大π键可表示为__________。
(5)VCl2(熔点1027 ℃)和VBr2(熔点827 ℃)均为六方晶胞,结构如图所示。

①VCl2和VBr2两者熔点差异的原因是__________。
②设晶体中阴、阳离子半径分别为r-和r+,该晶体的空间利用率为__________(用含a、c、r+和r-的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的Mg和Al混合物投入到200mL稀硫酸中,固体全部溶解后,向所得溶液中滴加NaOH溶液至过量,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。则下列说法不正确的是

A. Mg和Al的总质量为9g
B. 最初20mLNaOH溶液用于中和过量的稀硫酸
C. NaOH溶液物质的量浓度为5mol·L-1
D. 生成的氢气在标准状况下的体积为11.2L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学反应速率的说法中,正确的是
A. 2mol/L盐酸与锌反应时,加入4mol/L的氯化钠溶液,生成氢气的速率加快
B. 对于可逆反应2CO+2NO![]() N2+2CO2,使用合适的催化剂,CO的生成速率和消耗速率都加快
N2+2CO2,使用合适的催化剂,CO的生成速率和消耗速率都加快
C. 工业上合成氨是放热反应,升高温度,正反应速率减慢
D. 在K2SO4和BaCl2两溶液反应时,增大压强,生成沉淀速率加快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂和氮的相关化合物在化工、医药、材料等领域有着广泛的应用。请回答下列问题
(1)Li的氢标电势是最负的,达到-3.045V,与水有很大的反应倾向,然而将Li单质加入水中,其反应烈程度远不如其他碱金属,试解释原因__________。
(2)基态氮原子中,核外电子占据的最高能层的符号为_______,核外电子能量最高的电子的电子云轮廓图形状为_________。
(3)氮元素既可与其他元素形成正离子,比如N2O5结构中存在NO2+的结构,其空间构型为__________,氮原子的杂化形式为____________;它也可以形成全氮的正离子,比如N5AsF6中存在高能量的N5+,N5+的空间构型为_______。(每个N原子都满足8电子稳定结构)
(4)下图为一种N和Li形成的二元化合物的晶体结构,试在图中画出其晶胞_____,并写出该化合物的化学式_________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】300 mL某浓度的NaOH溶液中含有60 g溶质。现欲配制1 mol /L NaOH溶液,应取原溶液与蒸馏水的体积比约为( )
A. 1∶4 B. 1∶5 C. 2∶1 D. 2∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以CH4为原料制备H2的原理为CH4(g)+H2O(g)![]() CO(g)+3H2(g)。在一定条件下向a、b两个恒温恒容的密闭容器中均通入1.1molCH4(g)和1.1molH2O(g),测得两容器中CO的物质的量随时间的变化曲线分别为a和b。已知容器a的体积为10L,温度为Ta,下列说法不正确的是
CO(g)+3H2(g)。在一定条件下向a、b两个恒温恒容的密闭容器中均通入1.1molCH4(g)和1.1molH2O(g),测得两容器中CO的物质的量随时间的变化曲线分别为a和b。已知容器a的体积为10L,温度为Ta,下列说法不正确的是
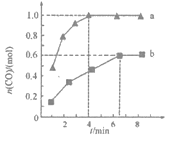
A. 容器a中CH4从反应开始到怡好平衡时的平均反应速率为0.025mol·L-1·min-1
B. a、b两容器的温度可能相同
C. 在达到平衡前,容器a的压强逐渐增大
D. 该反应在Ta温度下的平衡常数为27(mol·L-1)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中能用来区别SO2和CO2气体的是( ) ①石灰水
②H2S溶液
③酸性KMnO4
④氯水
⑤品红溶液
⑥紫色石蕊试液.
A.①②③⑤
B.①⑥
C.①
D.②③④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com