
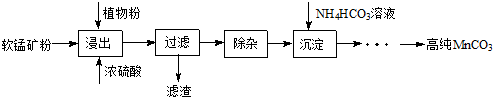
���� ʪ���������̿���Ҫ�ɷ�ΪMnO2��������Fe��Al��Mg������Ԫ�أ��Ʊ��ߴ�̼���̣�����Ũ�����ֲ��۽������˵õ���Һ��ȥ���ʣ�����̼������γɳ���ͨ��һϵ�в����õ��ߴ�̼���̣�
��1�����½��趼���Լӿ����ʵ��ܽⷴӦ���ʣ�����ֲ�����һ�ֻ�ԭ����
��2��ʹ��̼���̵�pH�������Dz������µ����ʣ���������������������Ϊ��������������ԭΪ�����ӣ�
��3������̼����������ֽ��������30�桫35���£���̼�������Һ�μӵ������̾���Һ�У����Ʒ�ӦҺ������pH��6.5��7.0���õ�MnCO3����������泥�������̼��ˮ�����ɵ�MnCO3�����辭���ϴ�ӣ�����ϴ���Ƿ���ȫ�ķ�����ȡ���һ��ϴ��Һ�����Ƿ��������������ƣ�
��4��Ksp ��MnCO3��=c��Mn2+��•c��CO32-������Mn2+������ȫʱ��c��CO32-��=1.8��10-11/1.0��10-5=1.8��10-6 mol•L-1����Mg2+Ҳ���γɳ�������Ҫ��Mg2+��2.6��10-5/1.8��10-6=14.4 mol•L-1��Mg2+��Ũ��0.01mol/LԶС��14.4 mol•L-1��
��� �⣺ʪ���������̿���Ҫ�ɷ�ΪMnO2��������Fe��Al��Mg������Ԫ�أ��Ʊ��ߴ�̼���̣�����Ũ�����ֲ��۽������˵õ���Һ��ȥ���ʣ�����̼������γɳ���ͨ��һϵ�в����õ��ߴ�̼���̣�
��1�����¡����趼���Լӿ����ʵ��ܽⷴӦ���ʣ�����ʱ�¶ȿ�����90�桫95��֮�䣬����Ҫ��������3Сʱ��Ŀ����������̿����̵Ľ����ʣ�����ֲ�����һ�ֻ�ԭ����
�ʴ�Ϊ��������̿����̵Ľ����ʣ�����ԭ����
��2��ʹ��̼���̵�pH�������Dz������µ����ʣ�������Һ�ж�������������������Ϊ��������������ԭΪ�����ӣ���Ӧ�����ӷ���ʽΪ��MnO2+H2O2+2H+=Mn2++2H2O+O2����
�ʴ�Ϊ������MnCO3�IJ������������µ����ʵȣ��� MnO2+H2O2+2H+=Mn2++2H2O+O2����
��3������̼����������ֽ�������¶ȿ���35�����µ�ԭ���Ƿ�ֹ̼����立ֽ⣬��30�桫35���£���̼�������Һ�μӵ������̾���Һ�У����Ʒ�ӦҺ������pH��6.5��7.0���õ�MnCO3����������泥�������̼��ˮ����Ӧ�Ļ�ѧ����ʽΪ��MnSO4+2NH4HCO3 $\frac{\underline{\;30�桫35��\;}}{\;}$MnCO3+��NH4��2SO4+CO2��+H2O�����ɵ�MnCO3�����辭���ϴ�ӣ�����ϴ���Ƿ���ȫ�ķ�����ȡ���һ��ϴ��Һ�����Ƿ��������������ƣ�ȡ���һ�ε�ϴ����Һ1��2 mL ���Թ��У������еμ��������ữ��BaCl2��Һ�����ް�ɫ�����������������ϴ�Ӹɾ���
�ʴ�Ϊ������̼����淋ķֽ⣬���ԭ�������ʣ�MnSO4+2NH4HCO3 $\frac{\underline{\;30�桫35��\;}}{\;}$MnCO3+��NH4��2SO4+CO2��+H2O��ȡ���һ�ε�ϴ����Һ1��2 mL ���Թ��У������еμ��������ữ��BaCl2��Һ�����ް�ɫ�����������������ϴ�Ӹɾ���
��4��Ksp ��MnCO3��=c��Mn2+��•c��CO32-������Mn2+������ȫʱ��c��CO32-��=$\frac{1.8��1{0}^{-11}}{1.0}$��10-5=1.8��10-6 mol•L-1����Mg2+Ҳ���γɳ�������Ҫ��Mg2+��2.6��10-5/1.8��10-6=14.4 mol•L-1��Mg2+��Ũ��0.01mol/LԶС��14.4 mol•L-1��������Һ�е�c��Mg2+��=10-2mol/L��˵��Mg2+�Ĵ��ڲ���Ӱ��MnCO3�Ĵ��ȣ�
��Ksp ��MnCO3��=c��Mn2+��•c��CO32-������Mn2+������ȫʱ��c��CO32-��=$\frac{1.8��1{0}^{-11}}{1.0}$��10-5=1.8��10-6 mol•L-1����Mg2+Ҳ���γɳ�������Ҫ��Mg2+��2.6��10-5/1.8��10-6=14.4 mol•L-1��Mg2+��Ũ��0.01mol/LԶС��14.4 mol•L-1��������Һ�е�c��Mg2+��=10-2mol/L��˵��Mg2+�Ĵ��ڲ���Ӱ��MnCO3�Ĵ��ȣ�
���� ���⿼����������ᴿ���ۺ�Ӧ�ã��������̷������������뷽���������ķ�ӦΪ���Ĺؼ������ط�����ʵ�������Ŀ��飬��Ŀ�Ѷ��еȣ������ڿ���ѧ���ķ��������ͼ���������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
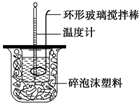 �ⶨϡ�����ϡ���������к��ȵ�ʵ��װ����ͼ��ʾ��ij��ȤС���ʵ����ֵ�������57.3kJ•mol-1���к��ȣ���ԭ������ǣ�������
�ⶨϡ�����ϡ���������к��ȵ�ʵ��װ����ͼ��ʾ��ij��ȤС���ʵ����ֵ�������57.3kJ•mol-1���к��ȣ���ԭ������ǣ�������| A�� | ʵ��װ����С�ձ����е��ڴ��ձ����� | |
| B�� | ��Ũ���������ϡ���� | |
| C�� | �ֶ�ΰ�NaOH��Һ����ʢ�������С�ձ��� | |
| D�� | ���¶ȼƲⶨNaOH��Һ��ʼ�¶Ⱥ�δϴ�ӣ�ֱ�ӲⶨH2SO4��Һ���¶� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
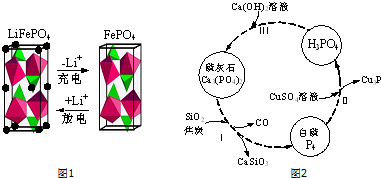
 �л���X��C��H��O����Ԫ����ɣ�����ӽṹģ����ͼ��ʾ��ͼ��������֮�����߱�ʾ������˫���������ڸ��л���������ȷ���ǣ�������
�л���X��C��H��O����Ԫ����ɣ�����ӽṹģ����ͼ��ʾ��ͼ��������֮�����߱�ʾ������˫���������ڸ��л���������ȷ���ǣ�������| A�� | �����к���3�ֹ����� | |
| B�� | 1 mol���л�����������ˮ��Ӧ�������3molBr2 | |
| C�� | 1 mol���л����������2 mol NaOH��Ӧ | |
| D�� | ���л�������ʹ����KMnO4��Һ��ɫ�����֤��������д���̼̼˫�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
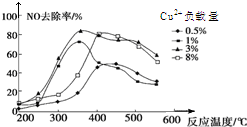 ��������Ӱ�����ǵ��������β�����ŷ������������������Ҫԭ��֮һ����֪����β���ŷ�ʱ���������·�Ӧ��
��������Ӱ�����ǵ��������β�����ŷ������������������Ҫԭ��֮һ����֪����β���ŷ�ʱ���������·�Ӧ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | A | B | C | D |
| ʵ�鷽�� | 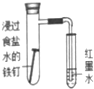 | 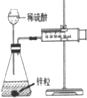 | 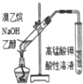 | 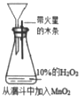 |
| ���� | �������к�ɫ�� | ע�����Ļ��������� | �������������Һ��ɫ | �����ǵ�ľ����ȼ |
| ���ۻ����� | ֤����������������ʴ | �����ڲⶨ��Ӧ��Ũ�ȶԷ�Ӧ���ʵ�Ӱ�� | ��������NaOH�Ҵ���Һ��Ӧ���ɵ���������ϩ | MnO2����H2O2��Ӧ����O2 |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ��4.5gAl | |
| B�� | һ������FeCl2�����ܺ���MgCl2��AlCl3 | |
| C�� | �������ʵ�����ȵģ�NH4��2SO4��MgCl2 | |
| D�� | ����MgCl2��FeCl2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ʵ�鿪ʼʱӦ�ȼ��Ⱥ�ͨ����ˮ | |
| B�� | ������ʪ���pH��ֽ�ⶨ��Һ��pH�������Ȼ��ʹʵ����������� | |
| C�� | ��ȡ�����е�Ԫ��ʱ��Ϊ��֤I-��ȫ����ΪI2���������������H2O2��������ˮ��Ӧ���� | |
| D�� | ���к��Ȳⶨʵ���У�Ϊȷ��÷�Ӧǰ����²Ӧ���ѷֱ����¶ȵ�����������Һ�����������ȼ��п��ٻ�ϣ�������������裬�������Һ������¶� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com