
【题目】现有A、B、C、D、E、F 原子序数依次增大的六种元素,它们位于元素周期表的前四周期。B元素含有3 个能级,且毎个能级所含的电子数相同;D的原子核外有8个运动状态不同的电子,E元素与F元素处于同一周期相邻的族,它们的原子序数相差3,且E元素的基态原子有4个未成对电子。请回答下列问题:
(1)请写出D基态的价层电子排布图:_____。
(2)下列说法正确的是_____。
A.二氧化硅的相对分子质量比二氧化碳大,所以沸点SiO2>CO2
B.电负性顺序:C<N<O<F
C.N2与CO为等电子体,结构相似,化学性质相似
D.稳定性:H2O>H2S,原因是水分子间存在氢键
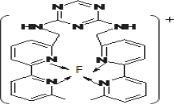
(3)某化合物与F(Ⅰ)(Ⅰ表示化合价为+1)结合形成如图所示的离子,该离子中碳原子的杂化方式是______。
(4)己知(BC)2是直线性分子,并有对称性,且分子中每个原子最外层都达到8电子稳定结构,则(BC)2中σ键和π键的个数比为______。
(5)C元素最高价含氧酸与硫酸酸性强度相近,原因是______。
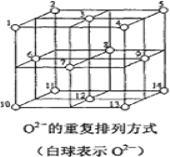
(6)Fe3O4晶体中,O2-的重复排列方式如图所示,该排列方式中存在着由如1、3、6、7的O2-围成的正四面体空隙和3、6、7、8、9、12的O2-围成的正八面体空隙。Fe3O4中有一半的Fe3+填充在正四面体空隙中,另一半Fe3+和Fe2+填充在正八面体空隙中,则Fe3O4晶体中,正四面体空隙数与O2-数之比为_____,有_____%的正八面体空隙没有填充阳离子。Fe3O4晶胞中有8个图示结构单元,晶体密度为5.18g/cm3,则该晶胞参数a=______pm。(写出计算表达式)
【答案】![]() B sp 2、sp 3 3:4 HNO3的非羟基氧个数与H2SO4的非羟基氧个数相同,所以酸性强度相近 2∶1 50%
B sp 2、sp 3 3:4 HNO3的非羟基氧个数与H2SO4的非羟基氧个数相同,所以酸性强度相近 2∶1 50% ![]()
【解析】
A、B、C、D、E、F原子序数依次增大的六种元素,均位于元素周期表的前四周期,B元素含有3个能级,且每个能级所含的电子数相同,核外电子排布为1s22s22p2,故B为碳元素;D的原子核外有8个运动状态不同的电子,则D为O元素;C的原子序数介于碳、氧之间,故C为N元素;E元素与F元素处于同一周期相邻的族,它们的原序数相差3,二者只能处于第四周期,且E元素的基态原子有4个未成对电子,外围电子排布为3d64s2,则E为Fe,F为Cu,(3)中C(氮元素)与A形成的气体x,则A为H元素,形成的x为NH3,据此解答本题。
(1)(1)D为O元素,价电子排布为2s22p4,基态的价层电子排布图为:![]() ,
,
故答案为:![]() ;
;
(2)A、二氧化硅属于原子晶体,二氧化碳形成分子晶体,故点:SiO2>CO2,故A错误;
B、同周期自左而右电负性增大,电负性顺序:C<N<O<F,故B正确;
C、N2与CO为等电子体,氮气分子中N原子之间形成3对共用电子对,化学性质稳定,CO还原性较强,二者化学性质不同,故C错误;
D、水分子间存在氢键,影响物理性质,不影响化学性质,由于非金属性O>S,所以稳定性:H2O>H2S,故D错误,
故答案为:B;
(3)杂环上的碳原子含有3个σ键,没有孤对电子,采用sp2杂化,甲基、亚甲基上碳原子含有4个共价单键,采用sp3杂化,
故答案为:sp2、sp3;
(4)(CN)2是直线型分子,并有对称性,结构式为:N≡C-C≡N,单键为σ键,三键含有1个σ键、2个π键,(CN)2中σ键和π键的个数比为3:4,
故答案为:3:4;
(5)HNO3的非羟基氧个数与H2SO4的非羟基氧个数相同,所以酸性强度相近,
故答案为:HNO3的非羟基氧个数与H2SO4的非羟基氧个数相同,所以酸性强度相近;
(6)结构中如1、3、6、7的O2围成的正四面体空隙有8个,由图可知晶体结构中O2离子数目为8×![]() +6×
+6×![]() =4个,则正四面体空隙数与O2离子数目之比为8:4=2:1;
=4个,则正四面体空隙数与O2离子数目之比为8:4=2:1;
Fe3O4中有一半的Fe3+填充到正四面体空隙中,另一半Fe3+和Fe2+填充在正八面体空隙中,则有50%的正八面体空隙没有填充阳离子;
含有Fe3+和Fe2+的总数为3,晶胞中有8个图示结构单元,不妨取1mol这样的晶胞,则1mol晶胞的质量为m=8×(3×56+4×16)g=8×232g,1mol晶胞即有6.02×1023个晶胞,1个晶胞的体积为V=(a×1010)3cm3,所以晶体密度为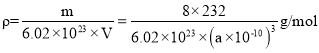 ,所以晶胞边长a=
,所以晶胞边长a=![]() pm,
pm,
故答案为:2:1;50;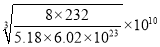 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】常温下,![]() 和
和![]() 两种酸溶液,起始时溶液体积均为
两种酸溶液,起始时溶液体积均为![]() 。分别向两溶液中加水进行稀释,稀释后溶液的体积为V,溶液pH随
。分别向两溶液中加水进行稀释,稀释后溶液的体积为V,溶液pH随![]() 的变化如图所示。下列说法正确的是
的变化如图所示。下列说法正确的是

A.等物质的量浓度的![]() 和
和![]() 溶液中,后者水的电离程度大
溶液中,后者水的电离程度大
B.当稀释至![]() 时,等体积的两种酸中和
时,等体积的两种酸中和![]()
C.当两溶液均稀释至![]() 时,溶液中:
时,溶液中:![]()
D.![]() 的电离方程式:
的电离方程式:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钾的冶炼可采用如下方法:2KF+CaC2![]() CaF2+2K↑+2C,下列有关说法合理的是( )
CaF2+2K↑+2C,下列有关说法合理的是( )
A.该反应的氧化剂是KF,氧化产物是K
B.该反应能说明C的还原性大于K
C.电解KF溶液不可能制备金属钾
D.CaC2、CaF2均为离子化合物,且阴、阳离子个数比均为2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeCl3的水解方程式可写为FeCl3+3H2O![]() Fe(OH)3+3HCl,若提高水解程度采取的方法是 ( )
Fe(OH)3+3HCl,若提高水解程度采取的方法是 ( )
A.降低温度B.加入少量Na2CO3 C.加入少量盐酸D.增加FeCl3的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以氯酸钠(NaClO3)等为原料制备亚氯酸钠(NaClO2)的工艺流程如下,下列说法中,不正确的是
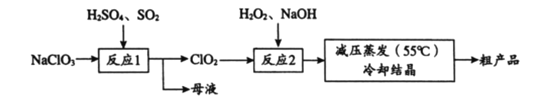
A. 反应1中,每生成1 mol ClO2有0.5 mol SO2被氧化
B. 从母液中可以提取Na2SO4
C. 反应2中,H2O2做氧化剂
D. 采用减压蒸发可能是为了防止NaClO2受热分解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对水样中溶质M的分解速率影响因素进行研究。在相同温度下,M的物质的量浓度(mol·L-1)随时间(min)变化的有关实验数据见下表。
时间 水样 | 0 | 5 | 10 | 15 | 20 | 25 |
Ⅰ(pH=2) | 0.40 | 0.28 | 0.19 | 0.13 | 0.10 | 0.09 |
Ⅱ(pH=4) | 0.40 | 0.31 | 0.24 | 0.20 | 0.18 | 0.16 |
Ⅲ(pH=4) | 0.20 | 0.15 | 0.12 | 0.09 | 0.07 | 0.05 |
Ⅳ(pH=4,含Cu2+) | 0.20 | 0.09 | 0.05 | 0.03 | 0.01 | 0 |
下列说法不正确的是
A. 在0~20min内,I中M的分解速率为0.015 mol·L-1·min-1
p>B. 水样酸性越强,M的分解速率越快C. 在0~25min内,III中M的分解百分率比II大
D. 由于Cu2+存在,IV中M的分解速率比I快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应2SO2(g)+O2(g)![]() 2SO3(g)△H<0,在一定条件下达到平衡状态,时间为t1时改变条件.化学反应速率与反应时间的关系如图所示.下列说法正确的是( )
2SO3(g)△H<0,在一定条件下达到平衡状态,时间为t1时改变条件.化学反应速率与反应时间的关系如图所示.下列说法正确的是( )

A. 维持温度、容积不变,t1时充入SO3(g)
B. 维持压强不变,t1时升高反应体系温度
C. 维持温度、容积不变,t1时充入一定量Ar
D. 维持温度、压强不变,t1时充入SO3(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知: 25℃、101 kPa下:① 2 Na(s) + 1/2 O2(g) = Na2O(s) △H1 = - 414 kJ / mol
② 2 Na(s) + O2(g) = Na2O2(s) △H2 = - 511 kJ / mol
下列说法正确的是
A. ①和②产物的阴阳离子个数比不相等
B. ①和②生成等物质的量的产物,转移电子数不同
C. 常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快
D. 25℃、101 kPa下,Na2O2(s) + 2 Na(s) = 2 Na2O(s) △H = -317 kJ / mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,可逆反应N2+3H2![]() 2NH3达到化学平衡状态,下列说法一定正确的是( )
2NH3达到化学平衡状态,下列说法一定正确的是( )
A.每1 mol N≡N断裂的同时有2 mol N—H生成
B.N2、H2、NH3的浓度之比为1∶3∶2
C.N2减少的速率和NH3减少的速率之比为1∶2
D.气体体积为初始体积的0.7倍
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com