
【题目】下列自然、生活中的事例不属于氧化还原反应的是
A.空气被二氧化硫污染后形成酸雨B.植物进行光合作用
C.用漂粉精杀菌D.明矾净水
科目:高中化学 来源: 题型:
【题目】车用妄全气囊中反应方程式为BNaN3=2Na+3N2↑,用双桥线标出电子 转移的数目和变化类型,指出氧化剂和还原剂.若要得到标准状况下33.6LN2 , 需要多少克NaN3(写出计算过程),NaN3的密度约为2g/cm3 , 则NaN3的体积约为多少立方厘米.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】隐形战机的核心材料是金属钛,我国探明储量世界第一.下列有关推断不正确的是( )
A.钛的原子序数为22
B.钛位于元素周期表第四周期
C.钛原子核外电子排布式为1s22s22p63s23p63d4
D.钛属于过渡元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度为T时,向2.0L恒容密闭容器中充入1.0mol PCl5 , 反应PCl5(g)=PCl3(g)+Cl2(g)经过一段时间后达到平衡.反应过程中测定的部分数据见下表:
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
下列说法正确的是( )
A.反应在前50 s 的平均速率v(PCl3)=0.0032 molL﹣1s﹣1
B.保持其他条件不变,升高温度,平衡时c(PCl3)=0.11 molL﹣1 , 则反应的△H<0
C.相同温度下,起始时向容器中充入1.0 mol PCl5、0.20 mol PCl3 和0.20 mol Cl2 , 反应达到平衡前v(正)>v(逆)
D.相同温度下,起始时向容器中充入2.0 mol PCl3 和2.0 mol Cl2 , 达到平衡时,PCl3 的转化率小于80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组欲鉴定某硫酸钠样品中是否含有亚硫酸钠,设计方案如下:取少量固体配成溶液,往溶液中滴加少量酸性KMnO4溶液,观察溶液是否褪色.如果溶液紫色褪去,说明该样品中含有亚硫酸钠. 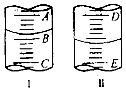
(1)用离子方程式表示该反应原理: .
(2)图I表示100mL量筒中液面的位置,A与B,B与C刻度间相差10mL,如果刻度A为30,量筒中液体的体积是mL.图II表示25mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积(填字母)
A.等于amL B.等于(25﹣a)mL C.大于amL D.大于(25﹣a)mL
(3)该小组同学欲测定样品中亚硫酸钠的含量,操作步骤如下:
a.称取mg样品,用蒸馏水溶解并置于锥形瓶中
b.将V1mL C1mol/L的酸性KMnO4溶液(过量)倒入锥形瓶中振荡
c.用C2mol/L草酸钠(Na2C2O4)溶液滴定过量的KMnO4 , 至滴定终点时用去Na2C2O4溶液V2mL
①KMnO4溶液应装在式滴定管中,达到滴定终点时溶液颜色的变化 .
②样品中Na2SO3的物质的量为mol.(用含C1、V1、C2、V2的代数式表示).
(4)下列操作会导致测得的Na2SO3的物质的量偏高的是(填字母,双选).
A.未用Na2C2O4标准液润洗滴定管
B.滴定前仰视盛有Na2C2O4溶液的滴定管,滴定后俯视
C.滴定前滴定管尖嘴处有气泡,滴定后消失
D.滴定时摇动锥形瓶,瓶中的液滴溅出.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的数值.请回答下列问题:
(1)0.5mol SO2共含有约个原子,它与g SO3所含硫原子数相等.
(2)质量相同的①HCl、②NH3、③CO2、④O2四种气体中,在同温同压条件下,所占体积最小的是(填序号) .
(3)19g某二价金属氯化物(ACl2)中含有0.4mol Cl﹣ , 则ACl2的摩尔质量是;
(4)标准状况下某种O2和N2的混合气体m g,含有b个分子,则n g该混合气体在相同状况下所占的体积应是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了将混有Na2SO4、NaHCO3的NaCl固体提纯,制得纯净的氯化钠溶液,某学生设计了如图所示的实验方案: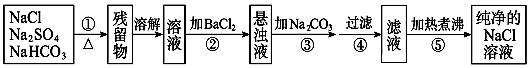
已知碳酸氢钠在加热条件下能分解成碳酸钠、二氧化碳和水,而NaCl和Na2SO4固体加热时不发生化学变化.请回答下列问题:
(1)操作①盛放药品可选用(填仪器名称).
(2)操作②为什么不用Ba(NO3)2溶液,其理由是: .
(3)进行操作②后,判断SO42﹣已除尽的方法是: .
(4)操作③的目的是: .
(5)此设计方案是否严密(填“是”或“否”)理由 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向100mL 0.01molL﹣1HA溶液中逐滴加入0.02molL﹣1MOH溶液,图中所示曲线表示,混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中,不正确的是( ) 
A.HA的电离方程式为:HA=H++A﹣
B.MOH为一元弱碱
C.K点对应的溶液中有:c(MOH)+c(M+)=0.02molL﹣1
D.N点对应的溶液中有:c(M+)=c(A﹣)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com