
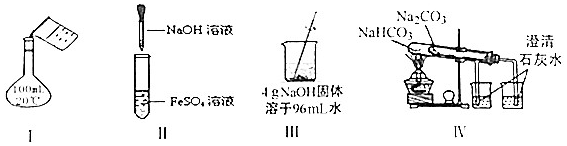
| A. | 实验Ⅰ:配制150mL0.10mol/L盐酸 | B. | 实验II:制取Fe(OH)2 | ||
| C. | 实验Ⅲ:配制4%NaOH溶液 | D. | 实验Ⅳ:比较两种物质的热稳定性 |
分析 A.转移液体需要引流;
B.NaOH应在液面下挤出,防止生成的氢氧化亚铁被氧化;
C.在烧杯中溶解固体,溶液质量为100g,NaOH为4g;
D.碳酸氢钠不稳定,加热分解生成碳酸钠.
解答 解:A.图中缺少玻璃棒引流,故A错误;
B.NaOH应在液面下挤出,防止生成的氢氧化亚铁被氧化,操作不合理,故B错误;
C.在烧杯中溶解固体,溶液质量为100g,NaOH为4g,则图中可配制4%NaOH溶液,故C正确;
D.碳酸氢钠不稳定,加热分解生成碳酸钠,为体现对比性,小试管中应为碳酸氢钠,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握实验装置的作用、溶液配制、物质的制备、性质比较、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案科目:高中化学 来源: 题型:选择题
| A. | ④ | B. | ③⑥ | C. | ①② | D. | ③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④①②③ | B. | ④③①② | C. | ④①③② | D. | ③②①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
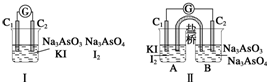
| A. | 甲组操作时,微安表指针不发生偏转 | |
| B. | 甲组操作时,溶液颜色不变 | |
| C. | 乙组操作时,C2作正极 | |
| D. | 乙组操作时,C1上发生的电极反应式为I2+2e-═2I- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 淀粉、CuO、HClO、Cu | |
| B. | 水玻璃、Na2O、CaO•6SiO2、AgO、SO3 | |
| C. | KAl (SO4) 2•12H2O、KCIO3、NH3•H2O、CH3CH2OH | |
| D. | 普通玻璃、H2O、Fe (SCN) 3、葡萄糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | w=$\frac{17c}{1000ρ}$ | B. | w=$\frac{17V}{17V+22400}$ | ||
| C. | c=$\frac{1000Vρ}{17V+22400}$ | D. | ρ=$\frac{17V+22400}{22.4+22.4V}$ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com