
【题目】有机化学基础一选修5]
化合物G是制备治疗高血压药物纳多洛尔的中间体,实验室由A制备G的一种路线如下:

已知:
(1)A的化学式是_____
(2)H中所含官能团的名称是_____;由G生成H的反应类型是_________。
(3)C的结构简式为_________,G的结构简式为___________。
(4)由D生成E的化学方程式为____________。
(5)芳香族化合物X是F的同分异构体,1molX最多可与4 mol NaOH反应,其核磁共振氢谱显示分子中有3种不同化学环境的氢,且峰面积比为3:3:1,写出两种符合要求的X的结构简式:__________。
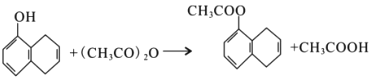
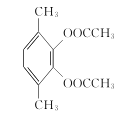
(6)请将以甲苯和(CH3CO)2O为原料(其他无机试剂任选),制备化合物 的合成路线补充完整。
的合成路线补充完整。 ___________________。
___________________。
【答案】![]() 羟基、醚键 取代反应
羟基、醚键 取代反应 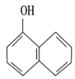
(任写两种) 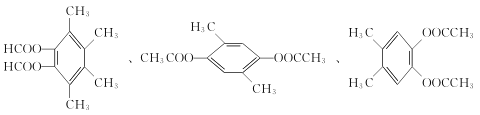
【解析】
结合流程及A、D的结构可知,A发生取代反应生成B为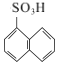 ,B发生取代反应生成C为
,B发生取代反应生成C为 ,C发生加成反应生成D,结合H的结构简式可知D发生取代反应生成E为
,C发生加成反应生成D,结合H的结构简式可知D发生取代反应生成E为 ,E发生加成后水解生成F为
,E发生加成后水解生成F为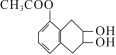 ,G为
,G为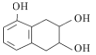 ,G发生取代反应生成H,据此分析。
,G发生取代反应生成H,据此分析。
(1)A的化学名称是萘,根据其结构简式可知其分子式为C10H8;
(2)H中所含官能团的名称是羟基、醚键;根据G的分子式及H的结构简式和另一反应物结构简式可知生成物还有氯化氢,则由G生成H的反应类型是取代反应;
(3)C的结构简式为 ,G的结构简式为
,G的结构简式为 ;
;
(4)由D生成E的化学方程式为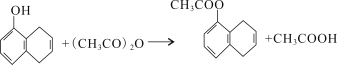 ;
;
(5)芳香族化合物X是F的同分异构体,1molX最多可与4 molNaOH反应,其核磁共振氯谱显示分子中有3种不同化学环境的氢,且峰面积比为3:3:1,则分子中含2个某酸苯酚酯结构、且含甲基,分子中有3种H,符合要求的X的结构简式为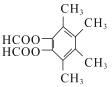 、
、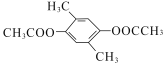 、
、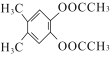 、
、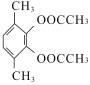 ,故答案为:
,故答案为: 、
、 、
、 、
、 中任意两种;
中任意两种;
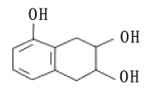
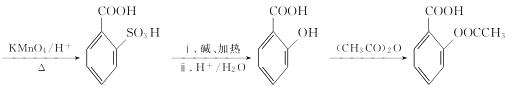
(6)以甲苯和(CH3CO)2O为原料(其他无机试剂任选)制备化合物 ,先甲苯与浓硫酸发生取代反应,后甲基被氧化生成-COOH,再将磺酸基转化为酚-OH,最后与乙酸酐反应,合成路线为
,先甲苯与浓硫酸发生取代反应,后甲基被氧化生成-COOH,再将磺酸基转化为酚-OH,最后与乙酸酐反应,合成路线为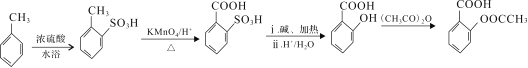 。
。


科目:高中化学 来源: 题型:
【题目】在一定温度下的定容容器中,发生反应:2A(g)+B(s)![]() C(g)+D(g),下列描述中能表明反应已达到平衡状态的是( )
C(g)+D(g),下列描述中能表明反应已达到平衡状态的是( )
①单位时间内生成n molC,同时生成n mol D
②单位时间内生成n molD,同时生成2n mol A
③C(g)的物质的量浓度不变
④容器内A、C、D三种气体的浓度之比为2:1:1
⑤v(A):v(C):v(D)=2:1:1
A. ②③ B. ②③④ C. ②⑤ D. ②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备苯甲醇和苯甲酸的化学原理是

已知苯甲醛易被空气氧化,苯甲醇的沸点为205.3 ℃,苯甲酸的熔点为121.7 ℃,沸点为249 ℃,溶解度为0.34 g;乙醚的沸点为34.8 ℃,难溶于水。制备苯甲醇和苯甲酸的主要过程如下所示:

试根据上述信息,判断以下说法错误的是( )
A. 操作Ⅰ是萃取分液
B. 乙醚溶液中所溶解的主要成分是苯甲醇
C. 操作Ⅱ蒸馏所得产品甲是苯甲醇
D. 操作Ⅲ过滤得到产品乙是苯甲酸钾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏德罗常数,下列叙述正确的是 ( )
A. 标准状况下,22.4LH2O含有的分子数为1 NA
B. 常温常压下,16g O2含有的原子数为1 NA
C. 通常状况下,1NA 个SO2分子占有的体积约为22.4L
D. 物质的量浓度为0.5mol/L的K2SO4溶液中,含有SO42-个数为0.5 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1983年,福瑞堡大学的普林巴克(Prinzbach),合成多环有机分子.如图分子,因其形状像东方塔式庙宇(pagoda﹣style temple),所以该分子也就称为pagodane(庙宇烷),有关该分子的说法正确的是( )
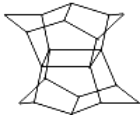
A. 分子式为C20H20
B. 一氯代物的同分异构体只有两种
C. 分子中含有二个亚甲基(﹣CH2﹣)
D. 分子中含有4个五元碳环
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)检验溶液中Fe3+存在的试剂是________,证明Fe3+存在的现象是________。
(2)写出FeCl3溶液与金属铜发生反应的离子方程式:________。
(3)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得纯净的FeCl3溶液,准备采用下列步骤:

请写出上述实验中加入或生成的有关物质的化学式。
①________,④________。
(4)要证明某溶液中不含Fe3+而可能含有Fe2+,进行如下实验操作时的最佳顺序为________。
①加入足量氯水②加入足量KMnO4溶液③加入少量KSCN溶液
A.①③ B.③② C.③① D.①②③
(5)写出向②⑤的混合液中通入⑥的离子方程式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环己酮是重要的化工原料,也是重要的工业溶剂。实验室制备环己酮的原理、有关数据及装置示意图如下:
反应原理:

反应放热,温度过高或者重铬酸钠过量会进一步氧化.
主要物料及产物的物理参数:
名称 | 溶解度 | 密度 | 熔点℃ | 沸点℃ | 溶解度 | |
水 | 乙醚 | |||||
环己醇 | 无色,有刺激性气味 | 0.9624 | 25.93 | 161.5 | 5.67g/100mL |
|
环己酮 | 无色,有枣激性气味 | 0.9478 | —— | 155.7 | 2.4g/100mL |
|
实验装置:

实验步骤:
①投料:在100mL三颈烧瓶中加入20mL水,慢慢加入5mL浓硫酸摇动,振荡下缓慢加入5mL(4.8g,0.048mol)环己醇,并将混合液温度降至30℃以下。将5g(0.019mol)重铬酸钠溶于水得橙红色溶液备用.
②反应:将约1/5的重铬酸钠溶液加入三颈烧瓶中,充分搅拌使之混合均匀。冷水浴冷却,控制反应温度在55-60℃。待橙红色消失后,再将剩余的重铬酸钠溶液分四次加入到三颈烧瓶中,当温度自动下降时,加入4mL甲醇使反应液完全变成墨绿色(三价铬);
③蒸馏:在反应瓶中加入30mL水,并改为蒸馏装置,收集90-99℃之间的馏分(环己酮与水的共沸物)至无油珠为止;
④萃取、干燥:将馏出液用食盐饱和后转入分液漏斗中,分出有机层。水层用8mL乙醚提取一次,将乙醚提取液和有机层合并,用无水硫酸镁干燥;5.蒸馏,收集环己酮产品2.6g。
请回答下列问题:
(1)装置A的名称是
(2)完成并配平反应方程式:
_____![]() +_____Na2Cr2O7+____H2SO4→____
+_____Na2Cr2O7+____H2SO4→____![]() +____Na2SO4+____Cr2(SO4)3+___H2O___________
+____Na2SO4+____Cr2(SO4)3+___H2O___________
(3)反应过程中加入甲醇后有无色气体生成。加入甲醇的作用是______,请用离子方程式表示反应原理________.
(4)步骤4向馏出液加入食盐的目的是_________,将乙醚提取液和有机层合并的原因是_________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A. PH4+、 PO43-、XeO4 的空间构型均为正四面体形
B. CO32-、 NO3-、CH2O的空间构型均为平面三角形
C. NH2-、NF3、Cl2O、 I3- 的VSEPR 模型名称均为四面体形
D. 微粒 N2H5、 NH4 、Fe(CO)3、Fe(SCN)3、H3O+、[Ag(NH3)2]OH 中均含有配位键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com