
【题目】已知①中国古代四大发明之一的黑火药,它是由硫磺、木炭粉和硝石组成;②油条中铝含量超标十分普遍,是影响人们健康的食品安全隐患。油条无铝配方由碳酸氢钠(小苏打)和臭粉组成。下列关于硝石和臭粉的成份组合正确的是
A.KNO3、NH4HCO3
B. KNO3、Na2CO3
C. HNO3、(NH4)2CO3
D.NH4NO3、Na2CO3
科目:高中化学 来源: 题型:
【题目】(1)VLFe2(SO4)3溶液中含Fe3+mg,则溶液中SO![]() 的物质的量浓度为mol·L-1
的物质的量浓度为mol·L-1
(2)标况下,mg气体A和ng气体B具有相等的体积,则同温同压下的密度之比为________,同质量的A、B的分子数目之比为________。
(3)在无土栽培中,配制1L内含5molNH4Cl、1.6molKCl、2.4molK2SO4的某营养液,若用KCl、NH4Cl、(NH4)2SO4配制,则需KCl、NH4Cl的物质的量分别为___、____。
(4)相同条件下,某Cl2与O2混合气体100ml恰好与150mlH2化合成HCl和H2O,则混合气体中Cl2与O2的体积比为,混合气体的平均摩尔质量为。
(5)在同温、同压下,实验测得CO、N2和O2三种气体的混合气体的密度是H2的14.5倍,其中O2的体积分数为,若其中CO和N2的物质的量之比为1:1,则混合气体中氧元素的质量分数为。(计算结果保留三位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)配制0.5mol/L的NaOH溶液,定容时向容量瓶中加蒸馏水超过刻度线,其结果 .(填“偏大”、“偏小”、或“不变”)
(2)从石油中分离出汽油、煤油和柴油等,所采用的方法是 .(填“干馏”或“分馏”)
(3)除去二氧化碳气体中的氯化氢杂质,选用的试剂是 .(填“NaOH溶液”或“饱和NaHCO3溶液”)
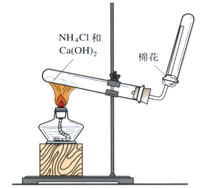
(4)如图是实验室制取氨气的装置,回答下列问题:
①收集氨气的方法是 排空气法.
②验证氨气是否收集满的方法是 .(写一种)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. 植物油中由于含有碳碳双键,因此在空气中长时间放置容易氧化变质
B. 利用乙醇的氧化性以及Cr3+、Cr2O72-的颜色差异来检验酒后驾车
C. 石油可以通过裂解、裂化等物理变化获得重要化工原料乙烯
D. 黄河入海口沙洲的形成体现了胶体电泳的性质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,m g气体A与n g气体B的分子数目一样多,下列说法不正确的是( )
A. 在任意条件下,若两种分子保持原组成,则其相对分子质量之比为m∶n
B. 25 ℃、1.25×105 Pa时,两气体的密度之比为n∶m
C. 同质量的A、B在非标准状况下,其分子数之比为n∶m
D. 相同状况下,同体积的气体A与B的质量之比为m∶n
查看答案和解析>>
科目:高中化学 来源: 题型:
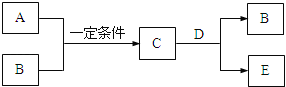
【题目】A、B、C、D、E是中学化学中的常见物质,A、B是短周期元素组成的单质.其转化关系如图:
请回答:
(1)若C的焰色反应为黄色;常温下,D为无色气体,能参与绿色植物的光合作用.
①组成A的元素在周期表中的位置是 .
②下列叙述正确的是 (填字母).
a.A与冷水剧烈反应
b.C与水反应可生成B
c.E与酸反应可生成D
(2)若C是能使湿润的红色石蕊试纸变蓝的气体,D是黄绿色气体.
①C与D反应的化学方程式是 .
②上述反应中转移1.2mol电子时,生成B的体积为 (标准状况).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将6.5 g锌投入100 mL 2 mol/L的稀硫酸(已知溶液密度为1.12 g/cm3)中充分反应。试计算
(1)产生的氢气在标准状况下的体积。
(2)反应后所得溶液的质量。
(3)现有2 mol/L的稀盐酸和稀硫酸各100 mL,分别加入等质量的铁,反应后生成的气体在标准状况下的体积比为2∶3,求加入铁的质量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 用括号中的试剂和方法除去各物质中的少量杂质,正确的是
A.苯中的甲苯(溴水、分液)
B.乙醇中的乙酸(NaOH溶液,分液)
C.乙醇中的水(新制CaO,蒸馏)
D.乙酸乙酯中的乙酸(NaOH溶液,分液)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气中的主要污染物是NO和CO。为减轻大气污染,人们提出通过以下反应来处理汽车尾气:
(1)2NO(g)+2CO(g)![]() 2CO2(g)+N2(g)△H=﹣746.5kJmol-1(条件为使用催化剂)
2CO2(g)+N2(g)△H=﹣746.5kJmol-1(条件为使用催化剂)
已知:2C(s)+O2(g)![]() 2CO(g)△H=﹣221.0kJmol-1
2CO(g)△H=﹣221.0kJmol-1
C(s)+O2(g)![]() CO2(g)△H=﹣393.5kJmol-1
CO2(g)△H=﹣393.5kJmol-1
则N2(g)+O2(g)=2NO(g) △H = kJmol-1。
(2)T ℃下,在一容积不变的密闭容器中,通入一定量的NO和CO,用气体传感器测得不同时间NO和CO的浓度如下表
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)/10-4 mol/L | 10.0 | 4.50 | c1 | 1.50 | 1.00 | 1.00 |
c(CO)/10-3 mol/L | 3.60 | 3.05 | c2 | 2.75 | 2.70 | 2.70 |
则c2合理的数值为 (填字母标号)。
A.4.20 B.4.00 C.2.95 D.2.80
(3)将不同物质的量的H2O(g)和CO(g)分别通入体积为2 L的恒容密闭容器中,进行反应:H2O(g)+CO(g)![]() CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
H2O | CO | CO | H2 | |||
i | 650 | 2 | 4 | 2.4 | 1.6 | 5 |
ii | 900 | 1 | 2 | 1.6 | 0.4 | 3 |
iii | 900 | a | b | c | d | t |
若a=2,b=1,则c= ,达平衡时实验组ii中H2O(g)和实验组iii中CO的转化率的关系为αii(H2O) αiii(CO)(填“<”、“>”或“=”)。
(4)二甲醚是清洁能源,用CO在催化剂存在下制备二甲醚的反应原理为:2CO(g)+4H2(g)![]() CH3OCH3(g)+H2O(g),已知一定条件下,该反应中CO的平衡转化率随温度、投料比
CH3OCH3(g)+H2O(g),已知一定条件下,该反应中CO的平衡转化率随温度、投料比![]() 的变化曲线如图1所示。
的变化曲线如图1所示。
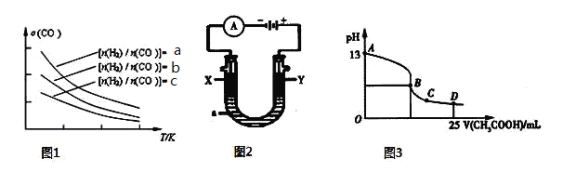
① a、b、c按从大到小的顺序排序为 。
② 根据图象可以判断该反应为 反应(填吸热或放热)。
(5)CO分析仪的传感器可测定汽车尾气是否符合排放标准,该分析仪的工作原理类似于燃料电池,其中电解质是氧化钇(Y2O3)和氧化锆(ZrO2)晶体,能传导O2-。
① 负极的电极反应式为 。
② 以上述电池为电源,通过导线连接成图2。若X、Y为石墨,a为2 L 0.1 mol/L KCl溶液电解一段时间后,取25 mL 上述电解后的溶液,滴加0.4 mol/L醋酸得到图3曲线(不考虑能量损失和气体溶于水,溶液体积变化忽略不计)。根据图2计算,上述电解过程中消耗一氧化碳的质量为 g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com