
【题目】下列关系正确的是( )
A.熔点:戊烷>2,2一二甲基戊烷>2,3一二甲基丁烷>丙烷
B.密度:CCl4>CHCl3>H2O>苯
C.同质量的物质燃烧耗O2量:丙炔>乙烷>乙烯>乙炔>甲烷
D.同物质的量物质燃烧耗O2量:已烷>环已烷>苯>苯甲酸
 优等生题库系列答案
优等生题库系列答案科目:高中化学 来源: 题型:
【题目】在阿富汗战争和伊拉克战争中美军士兵佩带的头盔、防弹背心和刚性前后防护板能够有效防御子弹和炮弹碎片,它们在战争中保住了许多美军士兵的生命.新型纤维不久将有望取代使用了数十年的凯夫拉纤维,成为未来防弹装备的主要制造材料.M5纤维是近年来开发出的一种超高性能纤维,它比现有的防爆破材料轻35%,下面是M5纤维的合成路线(部分反应未注明条件): 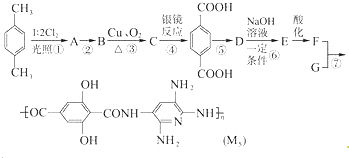
已知:当反应条件为光照且与X2反应时,通常是X2与烷或苯环侧链烃基上的H原子发生的取代反应,而当反应条件为催化剂存在且与X2反应时,通常为苯环上的H原子直接被取代.根据上述合成M5纤维的过程,回答下列问题:
(1)合成M5的单体G的结构简式为 , F的含氧官能团的名称有 .
(2)在①~⑦的反应中,不属于取代反应的是 , ②的反应条件是 .
(3)生成A的同时可能生成的A的同分异构体为 .
(4)1mol的C和足量新制的氢氧化铜悬浊液反应可以生成mol砖红色沉淀.
(5)1mol的F和Na2CO3溶液反应最多消耗Na2CO3mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中:① ![]() ②
② ![]() ③
③  ④
④  ⑤NaHSO 3溶液
⑤NaHSO 3溶液
(1)能与NaOH溶液发生反应的是 .
(2)能与溴水发生反应的是 .
(3)能与金属钠发生反应的是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】单斜硫和正交硫转化为二氧化硫的能量变化如图所示,下列说法不正确的是( ) 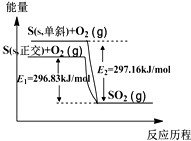
A.单斜硫和正交硫互为同素异形体
B.正交硫比单斜硫稳定
C.相同物质的量的正交硫比单斜硫所含有的能量高
D.由单斜硫制取正交硫是一个放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】前四周期A,B,C,D,E,F,G原子序数依次增大,A元素的质子数和质量数相等,B元素具有三个能级且所排电子数相同,D元素2p能级上电子数是2s能级的两倍;D和E相邻且同主族.F是第四周期未成对电子最多的原子,G是目前使用量最多的金属 请回答下列问题:(用推出的元素符号或者化学式作答)
(1)F的价电子排布式为 , B,C,D三种元素的第一电离能从大到小的顺序为 .
(2)BD32﹣中B原子的杂化方式为 , 该离子的空间构型为
(3)写出一种由A,C,D组成且既含离子键又含共价键的物质的化学式 , 化合物ABC中σ键和π键数目之比为 , C的气态氢化物在一定的压强下,测得的密度比该压强下理论密度略大,请解释原因 .
(4)E和G形成的某种晶胞如下图所示:其中白球表示E,黑球表示G.则该物质的化学式为 , 假设该晶胞的密度为ρ g/cm3 , 用NA表示阿伏加德罗常数,则该晶胞中距离最近的G原子之间的距离为cm. 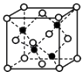
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是元素周期表的前三周期,其中①﹣⑩分别代表相应位置的元素.回答下列问题 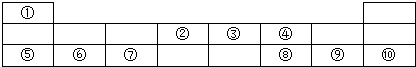
(1)元素⑥和⑨形成的化合物,其电子式为 .
(2)元素③的最低价氢化物,其结构式为 .
(3)元素⑤、⑥、⑦的最高价氧化物对应的水化物中,有两种能相互反应,则反应的离子方程式为 .
(4)元素⑧和⑨的最高价氧化物对应的水化物中,酸性最强的是(填化学式).
(5)元素④和⑧两种元素所形成的最低价氢化物,较不易分解的是(填化学式).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在①HC≡CH ②C2H5Cl,③CH3CH2OH,④CH3COOH,⑤聚乙烯,⑥ ![]() 六种物质中:
六种物质中:
①能与溴水发生化学反应是;②属于高分子化合物的是;
③能与Na2CO3溶液反应的是;④能发生酯化反应的是;
⑤能发生消去反应的是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组探究SO2气体还原Fe3+、I2 , 他们使用的药品和装置如图所示: 
(1)在配制氯化铁溶液时,需先把氯化铁晶体溶解在中,再加水稀释,这样操作的目的是 .
(2)根据以上现象,该小组同学认为SO2 与 FeCl3溶液发生氧化还原反应.
①写出SO2与FeCl3溶液反应的离子方程式;
②请设计实验方案检验有Fe2+生成;
③该小组同学向C烧杯反应后的溶液中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,即可证明反应生成了SO42﹣ . 该做法(填“合理”或“不合理”),理由是 .
(3)装置中能表明I﹣的还原性弱于SO2的现象是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com