
【题目】A、B属于短周期不同主族的元素,A、B原子的最外层电子中,成对电子和未成对电子占据的轨道数相等,若A元素的原子序数为a,则B元素的原子序数不可能为
A. a+3 B. a-5 C. a+8 D. a+11
科目:高中化学 来源: 题型:
【题目】下列实验能成功的是
A. 用 1体积的乙醇与3体积的浓H2SO4混合加热到140℃制乙烯
B. 加入适量浓溴水除去苯中混有的少量苯酚
C. 用饱和食盐水和电石(CaC2)制乙炔
D. 以盐酸、石灰石、苯酚钠溶液为试剂,验证酸性强弱关系:盐酸>石炭酸>碳酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个不导热的密闭反应器中,只发生两个反应:
a(g)+b(g) ![]() 2c(g) ΔH1<0
2c(g) ΔH1<0
x(g)+3y(g) ![]() 2z(g)ΔH2>0
2z(g)ΔH2>0
进行相关操作且达到平衡后(忽略体积改变所做的功),下列叙述错误的是( )
A.等压时,通入惰性气体,c的物质的量不变
B.等压时,通入z气体,反应器中温度升高
C.等容时,通入惰性气体,各反应速率不变
D.等容时,通入z气体,y的物质的量浓度增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4A(s)+3B(g) ![]() 2C(g)+D(g),经2 min B的浓度减少0.6 mol·L-1。对此反应速率的正确表示是( )
2C(g)+D(g),经2 min B的浓度减少0.6 mol·L-1。对此反应速率的正确表示是( )
A.用A表示的反应速率是0.8 mol·L-1·s-1
B.分别用B、C、D表示反应的速率,其比值是3∶2∶1
C.在2 min末时的反应速率,用反应物B来表示是0.3 mol·L-1·min-1
D.在这2 min内用B和C表示的反应速率的值都是相同的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质组成的说法正确的是
A.物质均是由分子构成,分子均是由原子构成
B.某物质经测定,只含有一种组成元素,则该物质一定是单质
C.碱性氧化物均是金属氧化物,酸性氧化物均是非金属氧化物
D.纯净的硫酸是纯净物,而纯净的盐酸是混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表对陈述Ⅰ、Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是( )
选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
A | 缺乏维生素A | 引发贫血症 | Ⅰ对,Ⅱ对,无 |
B | 人体缺铁 | 引发骨质疏松 | Ⅰ对,Ⅱ错,有 |
C | 人体缺钙 | 引发甲状腺肿大 | Ⅰ对,Ⅱ对,有 |
D | 缺乏维生素C | 引发坏血病 | Ⅰ对,Ⅱ对,有 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一密封体系中发生下列反应:N2+3H2![]() 2NH3 ΔH<0,下图是某一时间段中反应速率与反应进程的曲线关系图:
2NH3 ΔH<0,下图是某一时间段中反应速率与反应进程的曲线关系图:
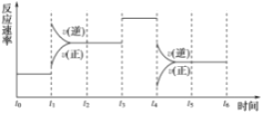
回答下列问题:
(1)处于平衡状态的时间段是___________、___________、___________。
(2)t1、t3、t4时刻体系中分别是什么条件发生了变化:____________、___________、___________。
(3)下列各时间段时,氨的百分含量最高的是___________(填序号)。
A.t0~t1 B.t2~t3 C.t3~t4 D.t5~t6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里用下图所示仪器和药品制取纯净的无水氯化铁。图中A、B、C、D、E、F表示玻璃管接口,接口的弯曲和伸长部分未画出,其中⑤、⑥所用为双孔塞,


根据要求回答下列问题:
(1)如果规定气体从左向右流动,上述各仪器装置的正确连接顺序是(填装置的序号):
③→______→______→_______→_______→_______。
(2)装置④的作用是_______________。
(3)实验开始时,应首先______________;实验结束时,应先熄灭装置__________处的酒精灯。该实验条件下生成的氯化铁呈烟状,且易水解,为便于收集,需要在__________和__________(填装置序号)之间增加装置⑦,该装置中烧杯里的液体可以是___________。
(4)在装置⑤的烧瓶中,发生反应的化学方程式为__________________。
(5)可用离子交换和滴定的方法测定FeCl3的纯度:称取0.68g的FeCl3样品,溶解后先进行阳离子交换预处理,再通过含有饱和OH―的阴离子交换柱,使Cl―和OH―发生交换。交换完成后,流出溶液中的OH―用0.4000 mol/L的盐酸滴定,滴至终点时消耗盐酸30.00 mL。则该样品中FeCl3的质量分数为___________%。
(6)设计一个简单实验,证明装置①的硬质玻璃管中有少量的铁未能与Cl2发生反应(写出实验操作及相关实验现象)_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com