
| A、16g O2中含有的氧原子数为NA |
| B、只有在标准状况下,NA个H2的体积才是22.4L |
| C、1mol Fe与足量Cl2反应转移的电子数为2NA |
| D、1mol?L-1 CuSO4溶液中含有的Cu2+数目为NA |
| m |
| M |
| m |
| M |
| 16g |
| 32g/mol |


科目:高中化学 来源: 题型:
| A、工业电解熔融Al203冶炼Al |
| B、用浸有KMn04溶液的硅土吸收水果释放的乙烯 |
| C、使用催化剂改变工业合成NH3的日产量 |
| D、蔗糖及其水解产物均可发生银镜反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2mol SO2气体与足量的O2在一定条件下反应,转移的电子数为4×6.02×1023 |
B、铵根离子的结构式: |
| C、谷氨酸的熔点高达205℃,主要是因为晶体中羧基与氨基之间形成较强的氢键 |
| D、常温下,100mL pH=1的硫酸溶液中含有的H+离子数为0.01×6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NO |
| B、NO2 |
| C、N2O |
| D、N2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 将一定质量的镁和铝的混合物投入200mL稀硫酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如图所示,则下列说法不正确的是
将一定质量的镁和铝的混合物投入200mL稀硫酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如图所示,则下列说法不正确的是查看答案和解析>>
科目:高中化学 来源: 题型:
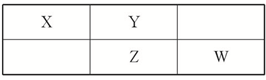 四种短周期元素在周期表中的相对位置如表所示,其中Z元素原子核外电子总数是其最外层电子数的3倍.
四种短周期元素在周期表中的相对位置如表所示,其中Z元素原子核外电子总数是其最外层电子数的3倍.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com