
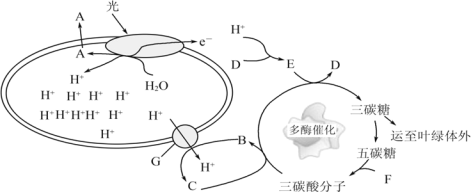
【题目】(下图为某植物的光合作用过程模式图,字母 A-G 表示物质或结构,二烷氨基乙醇羧酸脂(DA-6)是一种新型的叔胺类植物生长调节剂。某科研小组研究了 DA-6 对西瓜光合作用的影响,其相关指标测定(Rubisco 是碳反应的关键酶)结果如下表:
D A - 6 对西瓜光合作用的影响实验结果记录表
组 别 | 处理 | 光合速率 | 气孔导度 | 胞间二氧化碳浓度 | Rubisco 活性 |
(mmolm-2s-1) | (mmolm-2s-1) | (mmolm-2s-1) | (umolm-2s-1) | ||
① | 不遮光+清水 | 10.1 | 0.16 | 260 | 38.2 |
② | 不遮光+DA-6 | 15.2 | 0.24 | 255 | 42.1 |
③ | 遮光+清水 | 8.3 | 0.14 | 278 | 25.3 |
④ | 遮光+DA-6 | 13.4 | 0.23 | 269 | 35.7 |
(1)图中产生物质 A 的结构是___________________________,D 物质为___________________________。
(2)据图推测类囊体腔中积累H+的生理意义最可能是___________________________。
(3)突然停止光照,短期内三碳酸分子的含量将会___________________________。
(4)胞间 CO2 进入叶绿体内参与卡尔文循环,该过程生成 3 个 RuBP 需消耗___________________________个三碳糖磷酸,RuBP 的元素组成为__________________________。
(5)气孔导度表示气孔开放的程度。该研究能说明气孔导度不是遮光条件下光合速率下降的主要限制因素,可以证明此结论的实验组别是___________
A.① ② B.① ③ C.③ ④ D.② ④
(6)DA-6 可提高西瓜叶片的光合速率。从表数据进行推测,DA-6 提高西瓜叶片光合速率作用机制是:DA-6 通过__________________________,从而提高光合作用的速率。
【答案】类囊体(或光合膜) NADP+ 形成膜内外两侧的 H+浓度差,有利于 ATP 的合成 上升 5 CHOP BD 增大气孔导度,增加 CO2 吸收量,同时能提高 Rubisco 活性,加快碳反应速率
【解析】
光合作用过程分为光反应和暗反应,光反应是水光解产生O2和[H],同时将光能转变成化学能储存在ATP中,暗反应包括CO2固定和C3还原,二氧化碳固定是二氧化碳与五碳化合物结合形成C3,C3还原是C3被还[H]和ATP还原形成有机物和C5。
影响光合作用的外因包括CO2浓度、光照、温度、矿质元素、水等,CO2通过影响光合作用的暗反应阶段影响光合作用,光照强度通过影响光反应进而影响光合作用,温度通过影响酶活性而影响光合作用。
(1)图中物质A是O2,由H2O在光下分解产生,场所是类囊体;物质D为NADP+和H+产生物质E为NADPH,NADPH参与C3的还原。
(2)类囊体腔中的H+达到一定浓度时,可经类囊体膜上的ATP合成酶复合体穿过膜进入基质,同时将能量传递给ADP,使ADP和Pi合成ATP,所以其意义是形成膜内外两侧的 H+浓度差,有利于 ATP 的合成。
(3)突然停止光照,ATP含量减少,C3被还原的速率减慢,而CO2被固定的速率暂时不变,故C3的含量会上升。
(4)RuBP 中文名1,5-二磷酸核酮糖也就是卡尔文循环中的C5,其元素组成C、H、O、P;在卡尔文循环中CO2+ C5→2C3→C5+(CHO),故生成3个RuBP需要消耗5个C3。
(5)设置对照试验,无关变量保持一致,故能够证明气孔导度不是遮光条件下光合速率下降的主要限制因素的组别是①③或②④。
(6)从表数据进行推测,DA-6 提高西瓜叶片光合速率作用机制是:DA-6 通过增大气孔导度,增加 CO2 吸收量,同时能提高 Rubisco 活性,加快碳反应速率,从而提高光合作用的速率。


 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:
【题目】对于放热反应Zn+H2SO4===ZnSO4+H2↑,下列叙述正确的是( )
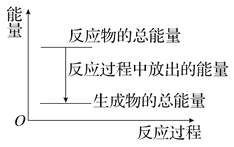
A. 反应过程中的能量关系可用上图表示
B. 1 mol Zn的能量大于1 mol H2的能量
C. 若将其设计为原电池,则锌作正极
D. 若将其设计为原电池,当有32.5 g Zn溶解时,正极放出的气体一定为11.2 L
查看答案和解析>>
科目:高中化学 来源: 题型:
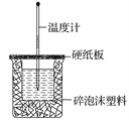
【题目】已知H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·mol-1。回答有关中和反应的问题:
(1)用0.1 mol NaOH配成稀溶液与足量稀硝酸反应,能放出________热量。
(2)如图装置中缺少的仪器名称是_____,碎泡沫塑料的作用______。
(3)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会___________(填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,回答下列问题:
族 周期 | ⅠA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ |
(1)③、④、⑤的原子半径由大到小的顺序为______(用元素符号回答)。
(2)②、③、⑦的最高价氧化物对应的水化物酸性由强到弱的顺序是_____。(用化学式回答)
(3)由①、④、⑤三种元素形成化合物的电子式______ 。
(4)⑥的单质与NaOH溶液反应的离子方程式_______。
(5)⑦的氢化物是一种无色气体,遇到空气能发生爆炸性自燃。已知室温下1 g氢化物自燃放出45.0 kJ的热量(产物水为液态),其热化学方程式为_________。
(6)由表中元素形成的常见物质A、B、C、D、E、F转化关系如下图所示。已知:A是常见的气态氢化物,B是能使带火星的木条复燃的无色无味气体, E的相对分子质量比D大17 ,D为红棕色气体(部分反应中生成物没有全部列出,反应条件未列出)

①A的结构式为_______。
②A和B反应生成C和F的化学方程式为_______,反应Ⅰ的离子方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由CH3CH2CH2Br制备CH3CH(OH)CH2OH,依次发生的反应类型和反应条件都正确的是
选项 | 反应类型 | 反应条件 |
A | 加成、取代、消去 | KOH醇溶液/加热、KOH水溶液/加热、常温 |
B | 消去、加成、取代 | NaOH醇溶液/加热、常温、KOH水溶液/加热 |
C | 氧化、取代、消去 | 加热、KOH醇溶液/加热、KOH水溶液/加热 |
D | 消去、加成、水解 | NaOH水溶液/加热、常温、NaOH醇溶液/加热 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在常温下,向一定量的0.1molL-1一元碱(BOH)溶液中逐滴加入一定浓度的盐酸。溶液中由水电离出的氢离子浓度的负对数[用pC表示,pC=-lgc水(H+)]与加入盐酸体积的关系如图所示。下列说法错误的是
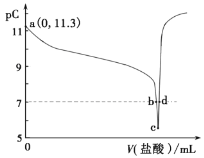
A.该一元碱为弱碱且Kb的数量级为10-5
B.b点溶液呈中性
C.c点到d点的溶液中:c(BOH)+c(OH-)>c(H+)
D.c点溶液中水的电离程度最大,且c(B+)<c(C1-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】火山爆发时会喷出SO2,SO2是大气主要污染物之一,在工业中可用于制备硫酸。回答下列问题:
(1)SO2是_____(填“电解质”或“非电解质”)。
(2)Cu2S与O2反应可生成SO2,已知:
Cu(s)+![]() O2(g)=CuO(s) △H=x kJmol-1
O2(g)=CuO(s) △H=x kJmol-1
Cu(s)+![]() S(s)=
S(s)=![]() Cu2S(s) △H=y kJmol-1
Cu2S(s) △H=y kJmol-1
S(s)+O2(g)=SO2(g) △H=z kJmol-1
写出Cu2S与O2反应生成CuO和SO2的热化学方程式__________________________。
(3)硫酸工业中涉及反应:2SO2(g)+O2(g)2SO3(g)△H=Q kJ·mol-1。一定条件下,在2L恒容密闭容器中,通入2molSO2和1molO2发生上述反应,SO2的平衡转化率与压强、温度的关系如图所示。a点时此反应的平衡常数的数值为_____。
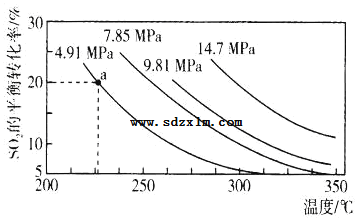
关于该反应,下列说法正确的是____。
A.容器内混合气体的密度不再变化时,反应达到平衡
B.相同时间内生成2molSO2同时消耗1molO2,反应达到平衡
C.Q大于0
D.相同温度下,压强越大,SO2的平衡转化率就越大,该反应的平衡常数就越大
E.反应达到平衡后保持温度不变,再充入2molSO2和1molO2,SO2的平衡转化率增大
F.反应达到平衡后保持温度不变,再充入He(g),SO2的平衡转化率增大
(4)将SO2通入酸化的硝酸钡溶液可生成硫酸钡沉淀,25℃时,KSP(BaSO4)=1×10-10。KSP(BaCO3)=2.6×10-9。该温度下,BaSO4和BaCO3沉淀共存的悬浊液中,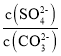 =___。
=___。
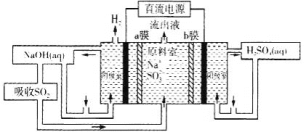
(5)用如图装置回收SO2可制得硫酸,电极为惰性电极,a、b膜分别为阳离子交换膜、阴离子交换膜。阳极的电极反应为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)按系统命名法命名有机物![]() :___________________。
:___________________。
(2)写出有机物2,3-二甲基-4-乙基己烷的结构简式:_______________________。
(3)有机物X(![]() )广泛存在于水果中,尤以苹果、葡萄、西瓜、山楂内含量较多。
)广泛存在于水果中,尤以苹果、葡萄、西瓜、山楂内含量较多。
①有机物X中含有的官能团名称是____________________________________;
在一定条件下,有机物X可发生化学反应的类型有________(填字母)。
A.水解反应 B.取代反应 C.加成反应 D.消去反应 E.加聚反应 F.中和反应
②写出X与金属钠发生反应的化学方程式:___________________________________。
③与X互为同分异构体的是________(填字母)。
a.![]() b.
b.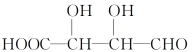
c.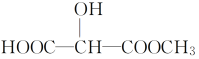 d.
d.![]()
e.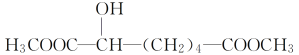 f.
f.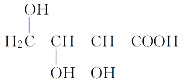
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】度鲁特韦可以用于治疗HIV-1感染,M是合成度鲁特韦的一种中间体。合成M的路线如下:(部分反应条件或试剂略去)
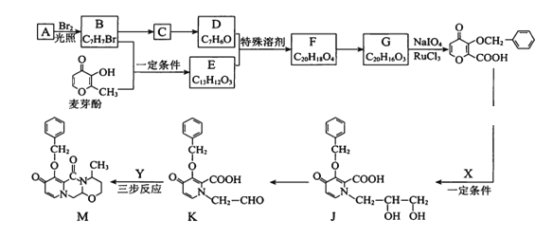
己知:
Ⅰ.![]()
Ⅱ.![]()
Ⅲ.![]()
(1)麦芽酚中含有官能团的名称是羰基、醚键、_______和______。
(2)A是苯的同系物,A—B的反应类型是_____。
(3)B- C的反应条件是____。
(4)C-D的化学方程式是_______。
(5)E不能与金属Na反应生成氢气,麦芽酚生成E的化学方程式是_______。
(6)G的结构简式是_____。
(7)X的分子式为C3H9O2N,X的结构简式是_______。
(8)Y的分子式为C4H11ON,Y与X具有相同种类的官能团,下列说法正确的是_______。
a.Y与X互为同系物
b.Y能与羧酸发生酯化反应
c.Y在浓硫酸、加热的条件下能发生消去反应
(9)K-M转化的一种路线如下图,中间产物2的结构简式是_______。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com