
在电解水制取H2和O2时,为了增强溶液的导电性,常常要加入一些电解质,最好选用下列物质中的( )
|
| A. | HCl | B. | MgSO4 | C. | CuSO4 | D. | NaCl |
科目:高中化学 来源: 题型:
下列说法中不正确的是( )
①水分子的电子式为H+ 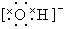 ②离子半径由小到大的顺序是:Mg2+<Na+<Cl-<S2-
②离子半径由小到大的顺序是:Mg2+<Na+<Cl-<S2-
③氮分子的电子式为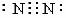 ④只含有离子键的化合物才是离子化合物
④只含有离子键的化合物才是离子化合物
A.①② B.③④ C.①④ D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
将镁带投入盛放在敞口容器的盐酸里,产生H2的速率与时间
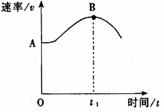 的关系可由右图表示。
的关系可由右图表示。
(1)写出离子反应方程式
(2)在下列因素中①H+的浓度 ②镁带的表面积 ③溶液的温度
④Cl-的浓度 能影响该反应速率的因素有__________(填序号);
(3)解释图中AB段形成的原因 ;
(4)解释图中t1时刻后速率变小的原因 。
查看答案和解析>>
科目:高中化学 来源: 题型:
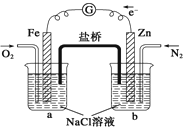
如图所示,下列判断中正确的是( )
|
| A. | 烧杯a中的溶液H+增大 |
|
| B. | 烧杯b中发生氧化反应 |
|
| C. | 烧杯a中发生的反应为:2H++2e﹣═H2 |
|
| D. | 烧杯b中发生的反应为:2Cl﹣﹣2e﹣═Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
1L0.1mol•L﹣1 AgNO3溶液在以Ag作阳极,Fe作阴极的电解槽中电解,当阴极增重2.16g时,下列判断正确的是(设电解按理论进行,溶液不蒸发)( )
|
| A. | 转移的电子数是1.204×1022 | B. | 阳极上产生112mLO2(标准状况) |
|
| C. | 溶液的浓度变化为0.08mol•L﹣1 | D. | 反应中有0.01molAg被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
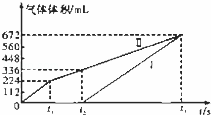
常温下用惰性电极电解200mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如图中Ⅰ、Ⅱ所示(以下气体体积已换算成标准状况下的体积).根据图中信息回答下列问题.
(1)通过计算推测:
①原混合溶液中NaCl和CuSO4的物质的量浓度.
c(NaCl)= 0.1 mol•L﹣1,c(CuSO4)= 0.1 mol•L﹣1.
②t2时所得溶液的pH= 1 .
(2)若用惰性电极电解NaCl和CuSO4的混合溶液200mL,经过一段时间后两极均得到224mL气体,则原混合溶液中氯离子浓度的取值范围为 0<c(Cl﹣)<0.1mol/L ,铜离子浓度的取值范围为 c(Cu2+)=0.05mol/L .
查看答案和解析>>
科目:高中化学 来源: 题型:
在水泥厂和冶金厂中常用高压电对气溶胶作用来除去烟尘,以减少对空气的污染,这种做法所应用的原理是( )
|
| A. | 布朗运动 | B. | 丁达尔效应 | C. | 电泳 | D. | 渗析 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知过氧化钠能与水发生如下反应:2Na2O2+2H2O====4NaOH+ O2↑
7.8g过氧化钠与足量水反应后,将会产生多少摩尔NaOH,生成的O2在标准状况下所占的体积是多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com