
【题目】许多物质与身体健康有着密切关系,请结合所学知识,判断下列叙述中错误的是( )
A.缺镁易患心血管病,缺碘易患甲状腺肿大
B.在医疗上FeCl3常用作止血剂,ZnSO4常用作收敛剂
C.葡萄糖、食盐、味精均可作食品添加剂
D.苏丹红是一种呈红色的有机物,能当作辣椒红色素用于食品加工
科目:高中化学 来源: 题型:
【题目】下列各图均能表示甲烷的分子结构,按要求回答下列问题。


(1)甲烷的球棍模型是________,甲烷的电子式是__________ (填序号)。甲烷的空间构型是__________________。
(2)写出甲烷与氯气发生反应的化学方程式_____________(只写第一步),该反应的反应类型是________________。
(3)相对分子质量为72的烷烃的分子式是_______________。
(4)甲烷与丙烷互为______
A.同位素
B.同素异形体
C.同系物
D.同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂排出的铬渣含有SiO2、A12O3、Fe2O3、Na2Cr2O7(易溶于水,是强氧化剂)等,处理建议是将+6价铬转化为低毒性的+3价铬后制备K2Cr2O7。实验室模拟处理铬渣的工艺流程如下(部分操作和条件略):

(1)已知过滤1后的滤液中存在如下平衡:Cr2O72-(橙色)+H2O![]() 2CrO42-(黄色)+2H+,则滤液应呈现的颜色是_________
2CrO42-(黄色)+2H+,则滤液应呈现的颜色是_________
(2)滤渣1的成分为______ 滤渣2中所含的金属元素为___________
(3)根据表中生成成氧化物沉淀的pH数据判断,流程中a的范围为__________。
物质 | Fe(OH)3 | Al(OH)3 | Cr(OH)3 | Fe(OH)2 |
开始沉淀 | 1.5 | 3.4 | 4.9 | 6.3 |
完全沉淀 | 2.8 | 4.7 | 5.5 | 8.3 |
(4)过滤3所得滤液又回流到过滤1所得滤液中,其目的是__________
(5)由Cr(OH)3得到黄色溶液过程中发生的反应的离子方程式是_________
(6)向橙色的K2Cr2O7溶液中,滴加Ba(NO3)2溶液,产生黄色沉淀,溶液pH减小。试推测黄色沉淀是_________,用平衡移动的原理解释溶液pH变小的原因是________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中Q单质可制成半导体材料.下列判断正确的是( )
A.W形成的离子半径大于T形成的离子半径
B.W的单质在过量氧气中燃烧生成WO3
C.最高价氧化物的水化物的酸性:R<Q
D.T是地壳中含量最多的金属元素,其单质的化学性质较活泼
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是一种消毒杀菌效率高、二次污染小的水处理剂.实验室可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4 ![]() 2ClO2↑+K2SO4+2CO2↑+2H2O.
2ClO2↑+K2SO4+2CO2↑+2H2O.
下列说法中错误的是( )
A.KClO3在反应中得到电子
B.ClO2中氯的化合价为+4价
C.在反应中H2C2O4是还原剂
D.1 mol KClO3参加反应有2mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于自然界中氮循环(如图)的说法正确的是
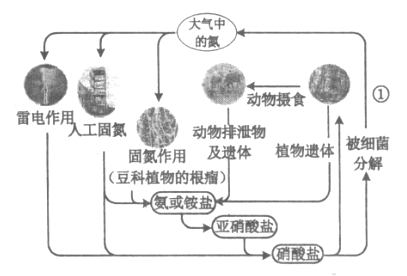
A. “雷电作用”中发生的反应是:![]()
B. 工业合成氨属于人工固氮
C. 氮元素均被还原
D. 过程①必须有O2参与
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图所示装置进行下列实验,实验结果与预测的现象不一致的是

选项 | ① | ② | 现象 |
A | 淀粉KI溶液 | 浓硫酸 | 溶液变蓝 |
B | 酚酞溶液 | 浓盐酸 | 无明显变化 |
C | AlCl3溶液 | 浓氨水 | 有白色沉淀 |
D | 浓盐酸 | 浓氨水 | 有白烟产生 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在300mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g)Ni(CO)4(g),已知该反应平衡常数与温度的关系如表:
温度/℃ | 25 | 80 | 230 |
平衡常数 | 5×104 | 2 | 1.9×10﹣5 |
下列说法不正确的是( )
A.上述生成Ni(CO)4(g)的反应为放热反应
B.25℃时反应Ni(CO)4(g)Ni(s)+4CO(g)的平衡常数为2×10﹣5
C.80℃达到平衡时,测得n(CO)=0.3mol,则Ni(CO)4的平衡浓度为2 mol/L
D.在80℃时,测得某时刻,Ni(CO)4、CO浓度均为0.5 mol/L,则此时v(正)>v(逆)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烃A是一种重要的化工原料.己知A在标准状况下的密度为1.16gL﹣1,B可发生银镜反应.它们之间的转化关系如图:

请回答:
(1)有机物A中含有的官能团名称是____;
(2)反应④的原子利用率达100%,该反应的化学方程式是___________________________;
(3)将金属钠与有机物D反应所得的产物溶于水得饱和溶液,滴加2滴酚酞试液,加热后水溶液显红色,其原因是__________________________;(用离子方程式表示)
(4)下列说法正确的是________;
A.有机物C在一定条件下合成乙酸乙酯也能实现原子利用率100%
B.反应②、③、⑤的类型各不相同
C.由于乙酸乙酯和水均为无色液体,故用分液漏斗无法分离乙酸乙酯和水的混合物
D.相同条件下乙酸乙酯在氢氧化钠溶液中水解较在稀硫酸中更完全.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com