
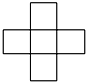
 A、B、C、D、E五种主族元素所处周期表的位置如图所示,且原子序数依次由小到大.已知A元素能与氧元素形成化合物AO2,AO2中氧的质量分数为50%,且A原子中质子数等于中子数,则C元素在周期表的位置( )
A、B、C、D、E五种主族元素所处周期表的位置如图所示,且原子序数依次由小到大.已知A元素能与氧元素形成化合物AO2,AO2中氧的质量分数为50%,且A原子中质子数等于中子数,则C元素在周期表的位置( )| A、第三周期ⅥA族 |
| B、第三周期VA族 |
| C、第四周期ⅥA族 |
| D、第四周期VA族 |
 ,则B、C、D、E分别是As、Se、Br、Te元素,据此判断C元素位置.
,则B、C、D、E分别是As、Se、Br、Te元素,据此判断C元素位置. ,则B、C、D、E分别是As、Se、Br、Te元素,S位于第三周期第VIA族,元素C和S属于同一主族且位于S元素下一周期,所以C元素位于第四周期第VIA族,故选C.
,则B、C、D、E分别是As、Se、Br、Te元素,S位于第三周期第VIA族,元素C和S属于同一主族且位于S元素下一周期,所以C元素位于第四周期第VIA族,故选C.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、此电池能发出蓝色火焰 |
| B、H2为正极,O2为负极 |
| C、工作时,电解液的pH不断减小 |
| D、电极反应为:负极2H2+4OH--4e-=4H2O;正极O2+2H2O+4e-=4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、蛋白质在体内水解的最终产物都是氨基酸 |
| B、蛋白质是生命的基础,没有蛋白质就没有生命 |
| C、人工合成具有生命活力的蛋白质-结晶牛胰岛素是我国科学家在1965年首次合成 |
| D、蛋白质的功能是构成机体和修复组织,而人体所需的热能全部由淀粉和油脂提供 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C21H23NO3 |
| B、C21H22NO5 |
| C、C21H23NO5 |
| D、C21H27NO7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
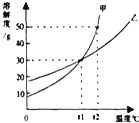
| A、t1℃时,甲、乙各30g分别加入70g水中均能恰好完全溶解 |
| B、t1℃时,甲和乙的饱和溶液中溶质的质量分数相等 |
| C、t2℃时,分别在100g水中各溶解20g甲、乙,同时降低温度,甲先达到饱和 |
| D、t2℃时,在100g水中放入60g甲,所得溶液溶质的质量分数为37.5% |
查看答案和解析>>
科目:高中化学 来源: 题型:
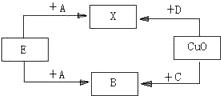 A、B、C、D、E是常见的五种无色气体,它们之间的转化关系如图所示(图中反应条件已略去,X在常温下为液体).则下列推断正确的是( )
A、B、C、D、E是常见的五种无色气体,它们之间的转化关系如图所示(图中反应条件已略去,X在常温下为液体).则下列推断正确的是( )| A、D是H2 |
| B、C是CO2 |
| C、A是O2 |
| D、B是CO |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、能导电 |
| B、熔点高、耐高温,化学性质稳定 |
| C、密度小 |
| D、硬度小,有润滑作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||||||
| B、CH3COOH(aq)+KOH(aq)=CH3COOK(aq)+H2O(l) | ||||||
| C、HNO3(浓)+NaOH(aq)=NaNO3(aq)+H2O(l) | ||||||
D、HCl(aq)+
|
查看答案和解析>>
科目:高中化学 来源: 题型:
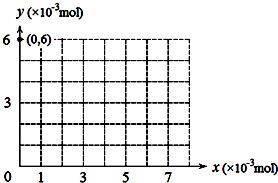
| 步骤 | 现象 |
| ⅰ.向盛有30mL 0.2mol?L-1 KI溶液的锥形瓶中依次滴入几滴淀粉溶液和足量稀硫酸,再用滴定管逐滴加入KBrO3溶液 | 随着KBrO3溶液滴入,溶液由无色变为蓝色并逐渐加深,最终保持不变 |
| ⅱ.继续向上述溶液中滴入KBrO3溶液 | 溶液的蓝色逐渐褪去 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com