
| A、标况下,0.3 mol的NH3 |
| B、4℃时,18克水 |
| C、2mol的Al (密度为2.7g/cm3 ) |
| D、100g 37% 密度1.20 g/cm3 NaCl 溶液 |
| 100g |
| 1.20g/mL |


科目:高中化学 来源: 题型:
| A、用一束激光照射胶体和溶液都有光亮的通路 |
| B、制备氢氧化铁胶体时加入的饱和氯化铁溶液越多越好 |
| C、用过滤的方法不能分离氢氧化铁胶体和氯化铁溶液 |
| D、向氢氧化铁胶体中加入过量盐酸后出现红褐色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
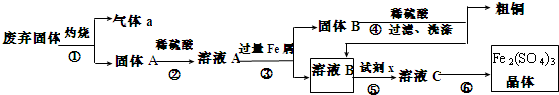
查看答案和解析>>
科目:高中化学 来源: 题型:
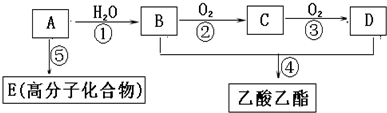
| 同一反应时间 | 同一反应温度 | ||||
| 反应温度/℃ | 转化率(%) | 选择性(%)* | 反应时间/h | 转化率(%) | 选择性(%)* |
| 40 | 77.8 | 100 | 2 | 80.2 | 100 |
| 60 | 92.3 | 100 | 3 | 87.8 | 100 |
| 80 | 92.6 | 100 | 4 | 92.3 | 100 |
| 120 | 94.5 | 98.7 | 6 | 93.0 | 100 |
| *选择性100%表示反应生成的产物是乙酸乙酯和水 | |||||
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol NaCl固体溶于1 L水所得溶液中NaCl的物质的量浓度为1 mol?L-1 |
| B、2.3 g钠转化为钠离子时失去的电子数目为0.1NA |
| C、常温常压下,11.2 L H2所含的原子数目为NA |
| D、28 g氮气所含的原子数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、稀硫酸滴在铁片上:2Fe+6H+=Fe3++3H2↑ |
| B、过量的CO2通入澄清的石灰水中:CO2+OH-=HCO3- |
| C、碳酸钙溶于足量的盐酸中:CO32-+2H+=H2O+CO2↑ |
| D、过量的NaHCO3溶液与Ca(OH)2溶液混合:Ca2++HCO3-+OH-=CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
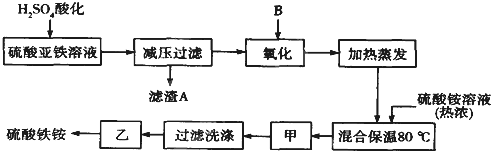
查看答案和解析>>
科目:高中化学 来源: 题型:
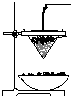 铁砂的主要成分是微粒状的磁性氧化铁、石英、石灰石等混合物.某化学兴趣小组从铁砂中分离出磁性氧化铁,并进行铝热反应实验.
铁砂的主要成分是微粒状的磁性氧化铁、石英、石灰石等混合物.某化学兴趣小组从铁砂中分离出磁性氧化铁,并进行铝热反应实验.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com