

| ʵ����� | ���� | ���� |
| ʵ��һ | �رյ��ɼУ��μ�һ����Ũ���ᣬ���� | A�У� ��I�����ȳ��ڣ�CuƬ�����ڣ���Һ������ɫ ��II���������ȣ�ͭƬ����������ݣ��γɺ�ɫ��Һ������ƿ�ײ��лҺ�ɫ������� ��III���������ȣ��д����������ɣ���Һ����壬����ƿ�ײ��д�����ɫ���壨���м�������ɫ������ԻҰ�ɫ����CuƬ��ʧB��������ð������Һ��ɫ |
| ʵ��� | ֹͣ���ȣ���ȴ��������ƿ�е�����Һ����ʢ��ˮ���ձ��� | ����ƿ�����д�����ɫ���壨���м�������ɫ������ԻҰ�ɫ�� �ձ�����Һ�¶����ߣ���Һֻ�Դ���ɫ |

���� ʵ��һ����I�����ȳ��ڣ�CuƬ�����ڣ���Һ������ɫ����ʱͭ��������������ͭ��Ϊ��ɫ���壻
��II���������ȣ�ͭƬ����������ݣ��γɺ�ɫ��Һ������ƿ�ײ��лҺ�ɫ���������ͭ��Ũ���ᷴӦ��������ͭ�Ͷ�������ɫ����Ϊ����ͭ����ͭ������ͭ��
��III���������ȣ��д����������ɣ���Һ����壬����ƿ�ײ��д�����ɫ���壨���м�������ɫ������ԻҰ�ɫ����˵����������ͭ��CuƬ��ʧB��������ð������Һ��ɫ��˵�����ɶ������������������壬����Ϊ���⣻
ʵ���������ƿ�����д�����ɫ���壨���м�������ɫ������ԻҰ�ɫ�����ձ�����Һ�¶����ߣ���Һֻ�Դ���ɫ��˵����������ͭ��
��1��ʹƷ����ɫ��˵������Ư���ԣ�
��2������ƿ�еİ�ɫ������CuSO4��������Ƿ�����ͭ���ɷֱ���������Ӻ������ӣ�
��3���ڼ���������ͭ��Ũ���ᷢ��������ԭ��Ӧ��������ͭ�����������ˮ��
��4����A�д������뵪���������ʹ����������ȫ���գ�
��5���γ�������ԭ����������ɶ����������£�Ҳ����Ϊ������ں�����������ˮ�γɵ��������������Ȼ�����Ӧ���������������Ȼ�����Һ����Ӧ��
��6�������ɫ������CuO�������ᷢ����Ӧ���ܽ⣬����CuO+H2SO4=CuSO4+H2O����Ϊ��ͭ������ͭ�������¾�������ϡ���
��7���ٺ�ɫ�������ϡ�������ˣ���Һ��������������Һδ�����ɳ�����˵��û�з�Ӧ��0.896g�������ΪCuS��Cu2S����ߵĻ��������������պ��أ�����Ϊ0.880g���躬��xmolCuS��ymolCu2S���з��̼��㣻
����A�к�ɫ������Ũ���ᷴӦ�ܵõ��������Һ������ʽΪ5Cu2S+CuS+34H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$11CuSO4+29SO2��+34H2O��
��� �⣺ʵ��һ����I�����ȳ��ڣ�CuƬ�����ڣ���Һ������ɫ����ʱͭ��������������ͭ��Ϊ��ɫ���壻
��II���������ȣ�ͭƬ����������ݣ��γɺ�ɫ��Һ������ƿ�ײ��лҺ�ɫ���������ͭ��Ũ���ᷴӦ��������ͭ�Ͷ�������ɫ����Ϊ����ͭ����ͭ������ͭ��
��III���������ȣ��д����������ɣ���Һ����壬����ƿ�ײ��д�����ɫ���壨���м�������ɫ������ԻҰ�ɫ����˵����������ͭ��CuƬ��ʧB��������ð������Һ��ɫ��˵�����ɶ������������������壬����Ϊ���⣻
ʵ���������ƿ�����д�����ɫ���壨���м�������ɫ������ԻҰ�ɫ�����ձ�����Һ�¶����ߣ���Һֻ�Դ���ɫ��˵����������ͭ��
��1��BΪƷ����Һ����Һ��ɫ��˵�������������Ư���ԣ��ʴ�Ϊ��Ư�ף�
��2������ƿ�еİ�ɫ������CuSO4��������Ƿ�����ͭ���ɷֱ���������Ӻ������ӣ�������ȡ������ɫ��������ˮ����Һ����ɫ��˵�������к���ͭ���ӣ�����Һ�еμ��Ȼ�����Һ������ϡ���ᣬ���ְ�ɫ������˵�������к�����������ӣ�
�ʴ�Ϊ��CuSO4��ȡ������ɫ��������ˮ����Һ����ɫ��˵�������к���ͭ���ӣ�����Һ�еμ��Ȼ�����Һ������ϡ���ᣬ���ְ�ɫ������˵�������к�����������ӣ�
��3���ڼ���������ͭ��Ũ���ᷢ��������ԭ��Ӧ������ʽΪ2H2SO4��Ũ��+Cu$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+2H2O��
�ʴ�Ϊ��2H2SO4��Ũ��+Cu$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+2H2O��
��4�����װ��ǰ������������Ϳ�ʹװ���в���������ȫ�����գ�Ӧ����ȡ�IJ�������A�д������뵪���������
�ʴ�Ϊ����A�д������뵪���������
��5���γ�������ԭ����������ɶ����������£�Ҳ����Ϊ������ں�����������ˮ�γɵ�������������Ƿ������ᣬ�ɽ�Ʒ����Һ��Ϊ�����ữ���Ȼ�����Һ��ʵ��ǰ��ͨ��һ��ʱ�䵪����Ȼ���ټ���װ��A���ʵ�飬���Ȼ�����Һ�г��ְ�ɫ����������뷨��������ȷ�ģ�
�ʴ�Ϊ����Ʒ����Һ��Ϊ�����ữ���Ȼ�����Һ��ʵ��ǰ��ͨ��һ��ʱ�䵪����Ȼ���ټ���װ��A���ʵ�飬���Ȼ�����Һ�г��ְ�ɫ����������뷨��������ȷ�ģ�
��6�������ɫ������CuO�������ᷢ����Ӧ���ܽ⣬����CuO+H2SO4=CuSO4+H2O����Ϊ��ͭ������ͭ�������¾�������ϡ���ᣬ
�ʴ�Ϊ��CuO+H2SO4=CuSO4+H2O��
��7���ٺ�ɫ�������ϡ�������ˣ���Һ��������������Һδ�����ɳ�����˵��û�з�Ӧ��0.896g�������ΪCuS��Cu2S����ߵĻ��������������պ��أ�����Ϊ0.880g���躬��xmolCuS��ymolCu2S����$\left\{\begin{array}{l}{96x+160y=0.896}\\{80x+160y=0.880}\end{array}\right.$��x=0.001mol��y=0.005mol��
�ʴ�Ϊ��CuS0.001mol��Cu2S0.005mol��
����A�к�ɫ������Ũ���ᷴӦ�ܵõ��������Һ������ʽΪ5Cu2S+CuS+34H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$11CuSO4+29SO2��+34H2O��
�ʴ�Ϊ��5Cu2S+CuS+34H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$11CuSO4+29SO2��+34H2O��
���� ���������о�̽��ͭ��Ũ���ᷴӦ�������ɼ�����Ϊ���忼����ѧ���ķ�����������������ѧʵ���������漰���ӷ���ʽ����д����������ѡ�����ʵļ���ȣ�������ѧ���������֪ʶ����������Ŀ�Ѷ��еȣ�


 ������״Ԫ���Ծ�ϵ�д�
������״Ԫ���Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ H2SO3 | B�� | ����������ɱ� CO | ||
| C�� | ���������������� CaO | D�� | ���մ� NaHCO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
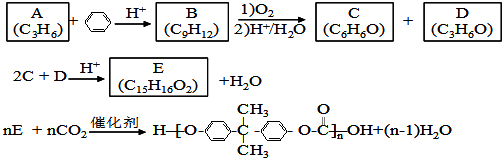
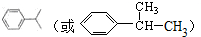 ��
��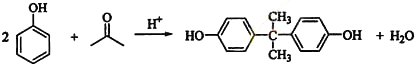 ��
��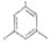 ��д���ṹ��ʽ����
��д���ṹ��ʽ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��ͼ��M��N���ֲ����ᾧˮ�Ĺ��������ܽ�����ߣ�����˵������ȷ���ǣ�������
��ͼ��M��N���ֲ����ᾧˮ�Ĺ��������ܽ�����ߣ�����˵������ȷ���ǣ�������| A�� | t1��ʱ��N��M���ܽ�ȴ� | |
| B�� | �¶ȴ�t1�����ߵ�t3��ʱ��N�ı�����Һ�����ʵ��������������� | |
| C�� | M��N���ܽ�ȴ� | |
| D�� | N�к�������Mʱ�����ý��½ᾧ���ᴿN |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
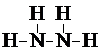 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��H3����H2����H1����H4����H5 | B�� | ��H1����H2����H3����H5����H4 | ||
| C�� | ��H4����H5����H1����H2����H3 | D�� | ��H4����H5����H3����H2����H1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
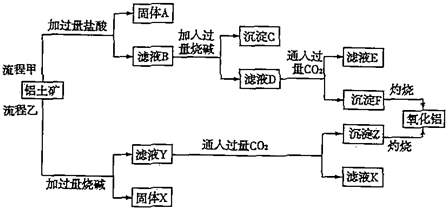
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com