
判断集气瓶中是否装满氨气,下列操作中正确的是
A. 在瓶口闻一下是否有刺激性气味 B. 将湿润的红色石蕊试纸放在瓶口
C. 将蘸有浓硫酸的玻璃棒放在瓶口 D. 将蘸有浓盐酸的玻璃棒伸入集气瓶内
 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案科目:高中化学 来源: 题型:
塑料制品是人类日常生活中使用量最大的合成高分子材料,如食品袋、塑料薄膜等都是塑料制品。大量的塑料制品的生产和使用,给人们的生活带来了极大的方便,同时也造成了严重的环境问题——白色污染。当今白色污染问题已得到了人们应有的重视,一些科学家也成功地寻找到了治理白色污染的有效途径。结合学过的知识,回答下列问题:
 (1)写出工业上利用石油裂解气生产聚乙烯的化学方程式:______________ ________________________________________________
(1)写出工业上利用石油裂解气生产聚乙烯的化学方程式:______________ ________________________________________________ ____。
____。
(2)塑料废弃物的危害有 ( )。
①破坏土壤结构,影响植物生长 ②造成海难事件 ③破坏环境卫生 ④危及海洋生物的生存
A.①②③ B.①②④
C.①③④ D.全部
(3)某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图(加热装置略)。
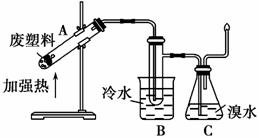
加热某种废弃塑料得到的产物有氢气、甲烷、乙烯、丙烯、苯、甲苯、炭等。
①试管B收集到的产品为________和________,其一氯代物分别有几种?________
②锥形瓶C中观察到的现象为________________________________________。
③写出C中逸出的气体在工业上的两种用途________________________、__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
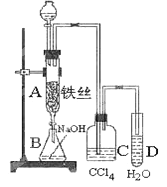
某化学课外小组用右图装置制取溴苯.先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中.
(1)写出A中有机反应的化学方程式
(2)已知上述反应是放热反应.观察到A中的现象是
C6H6+Br2
(3)实验结束时,打开A下端的活塞,让反应液流入B中,在B中的氢氧化钠溶液里可观察到的现象是 充分振荡,目的是 除去溶于溴苯中的溴
,写出有关的化学方程式
(4)C中盛放CCl4的作用是 除去溴化氢气体中的溴蒸气
.
(5)向试管D中滴入 若产生 现象,则证明苯和液溴发生的是取代反应,而不是加成反应,在上述整套装置中,具有防倒吸作用的装置有 (填装置编号)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应的离子方程式书写正确的是
A. 铁片放入稀盐酸中: Fe + 2H+ = Fe3+ + H2 ↑
B. 氢氧化铜与稀硫酸: OH- + H+ = H2O
C. 氯化钡溶液与硝酸银溶液: Cl- + Ag+ = AgCl ↓
D. 碳酸钙与稀硝酸: CO32- + 2H+ = CO2 ↑ +H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
将铜棒与锌棒用导线连接,依次插入分别盛有:①硫酸溶液;②硫酸铜溶液;③硫酸钠溶液的三个烧杯中,此时,
(1)铜片上发生的主要反应的电极反应式是:①________________________;
②______________________________________________________________;
③_______________________________________________________________。
(2)铁制品在经常下酸雨的地区电化 学腐蚀严重,写出此电化学腐蚀的电极反应式:
学腐蚀严重,写出此电化学腐蚀的电极反应式:
正极____________________________________________________________;
负极____________________________________________________________。
(3)将表面去掉氧化膜的镁片与铝片用带电流表的导线连接,插入盛有烧碱溶液的烧杯中,此时发现电流计指针偏转,判断此原电池的正负极,并写出电极反应式和总反应方程式。
正极:________,电极反应式:_____________________________________,负极:________,电极反应式:_____________________________________,
总反应:________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
现有四种元素的基态原子的电子排布式如下:

则下列有关比较中正确的是( )
A.第一电离能:④>③>②>① B.原子半径:④>③>②>①
C.电负性:④>③>②>① D.最高正化合价:④>③=②>①
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com