
| A. | 124 g P4含有P-P键的个数为4NA | |
| B. | 12 g石墨中含有C-C键的个数为1.5NA | |
| C. | 12 g金刚石中含有C-C键的个数为4NA | |
| D. | 60gSiO2中含Si-O键的个数为2NA |
分析 通过n=$\frac{m}{M}$计算各物质的物质的量,结合各晶体的结构确定各个化学键的个数.
解答 解:A、n(P4)=$\frac{124g}{124g/mol}$=1mol,1个P4分子含有6个P-P键,因此124g P4含有的P-P键的物质的量为6mol,P-P键的个数为6NA,故A错误;
B、12g石墨中含有碳原子的物质的量n=$\frac{m}{M}$=$\frac{12g}{12g/mol}$=1mol,在石墨晶体中一个碳原子形成3个C-C键,每个C-C键由2个碳原子构成,因此12g石墨中含有C-C键的物质的量为1mol×3×$\frac{1}{2}$=1.5mol,C-C键的个数为1.5NA,故B正确;
C、12g金刚石中含有碳原子的物质的量n=$\frac{m}{M}$=$\frac{12g}{12g/mol}$=1mol,在金刚石晶体中每个碳原子形成4个C-C键,每个C-C键由2个碳原子构成,因此12g金刚石中含有C-C键的物质的量为1mol×4×$\frac{1}{2}$=2mol,C-C键的个数为2NA,故C错误;
D、n( SiO2)=$\frac{m}{M}$=$\frac{60g}{60g/mol}$=1mol,在二氧化硅晶体中,每个硅原子形成4个Si-O键,因此60g SiO2中含Si-O键的物质的量为4mol,Si-O键的个数为4NA,故D错误;
故选B.
点评 本题考查阿伏伽德罗常数的有关计算,难度中等,侧重于分子晶体、原子晶体、混合晶体结构的考查,掌握物质的晶体结构是解题的关键.


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源: 题型:选择题
| A. | 原电池是一种直接把化学能转化为电能的装置,在此转化过程中无能量损耗 | |
| B. | 在Zn-Cu-H2SO4构成的原电池中,H+不断移向负极 | |
| C. | 钢铁在潮湿的环境中易被腐蚀与原电池有关 | |
| D. | 纯铁比生铁(含有少量杂质)与稀HCl反应快 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 热化学方程式中的化学计量数表示物质的量,可以是分数 | |
| B. | △H>0 kJ•mol-1表示放热反应,△H<0 kJ•mol-1表示吸热反应 | |
| C. | 1 mol H2SO4与1 molBa(OH)2反应生成H2O时放出的热叫做中和热 | |
| D. | 1 mol H2与0.5 molO2反应放出的热就是H2的燃烧热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 它有酸性,能与纯碱溶液反应 | |
| B. | 它在一定条件下能发生水解,且产物只有一种 | |
| C. | 1 mol该有机物最多能与7 mol NaOH反应 | |
| D. | 1 mol该有机物最多能与4 mol Br2反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
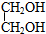 ,写出有关反应的化学方程式.CH3CH2Cl+NaOH$→_{△}^{乙醇}$CH2=CH2+NaCl+H2O;CH2=CH2+Cl2→CH2Cl-CH2Cl;CH2Cl-CH2Cl+2NaOH $→_{△}^{水}$HOCH2CH2OH+2NaCl.
,写出有关反应的化学方程式.CH3CH2Cl+NaOH$→_{△}^{乙醇}$CH2=CH2+NaCl+H2O;CH2=CH2+Cl2→CH2Cl-CH2Cl;CH2Cl-CH2Cl+2NaOH $→_{△}^{水}$HOCH2CH2OH+2NaCl.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 共价化合物中不可能含有离子键 | |
| B. | 只有金属元素和非金属元素才能形成离子键 | |
| C. | 水分子很稳定,因为水分子间存在氢键 | |
| D. | 所有的分子晶体内都存在两种以上作用力 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上月考一化学试卷(解析版) 题型:选择题
已知:①CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g)△H=-akJ·mol一 1
1
②CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-bkJ·mol一1
③CH4(g)+2O2(g)=CO2(g)+2H2O(1)△H=-ckJ·mol一1
则下列叙述正确的是
A.由上述热化学方程式可知b>c
B.甲烷的燃烧热为bkJ/mol
C.2CH3OH(g)=2CH4(g) +O2(g) △H=2(b一a)KJ? mol一1
D.当甲醇和甲烷物质的量之比为1:2时,其完全燃烧生成CO2和H2O(1)时,放出的热量 为Q kJ,则该混合物中甲醇的物质的量为Q/(a+2b) mol
为Q kJ,则该混合物中甲醇的物质的量为Q/(a+2b) mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com