

| A. | 它有酸性,能与纯碱溶液反应 | |
| B. | 它在一定条件下能发生水解,且产物只有一种 | |
| C. | 1 mol该有机物最多能与7 mol NaOH反应 | |
| D. | 1 mol该有机物最多能与4 mol Br2反应 |
分析 由结构简式可知,该物质中含5个酚-OH、1个-COOH、1个-COOC-,结合酚、羧酸、酯的性质来解答.
解答 解:A.含有酚羟基,具有酸性,但酸性比碳酸弱,比碳酸氢钠强,则可与碳酸钠反应,故A正确;
B.分子中含有酯基,能发生水解,1mol 有机物水解后能生成2mol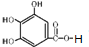 ,故B正确;
,故B正确;
C.在1molZ中含有1mol水解后生成1mol羧基和1mol酚羟基的酯基、1mol羧基、5mol酚羟基,可以和8molNaOH发生反应,故C错误;
D.酚羟基的邻、对位氢原子,可以与Br2发生取代反应,所以1 molX最多能与4 molBr2反应,故D正确.
故选C.
点评 本题考查有机物的结构与性质,为高考常见题型,把握物质的官能团及性质的关系为解答的关键,熟悉苯酚、羧酸、酯的性质即可解答,选项BC为易错点,题目难度不大.


 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案科目:高中化学 来源: 题型:选择题
| A. | 加入H2O(g),平衡向正反应方向移动,体系压强减小 | |
| B. | 加入少量C,正反应速率增大 | |
| C. | 降低温度,平衡向正反应方向移动 | |
| D. | 加入CO,混合气体的密度增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{MV}{22.4(V+0.1)d}$ | B. | $\frac{1000VdM}{MV+2240}$ | C. | $\frac{1000Vd}{MV+2240}$ | D. | $\frac{Vd}{MV+2240}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 基态原子含有未成对电子最多的第二周期元素 | |
| B. | 某激发态为1s22s12p3的原子 | |
| C. | 基态原子最外层电子排布为2s22p6的元素 | |
| D. | 基态原子最外层电子排布为3s23p5的元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
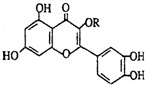 )存在于槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述错误的是( )
)存在于槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述错误的是( )| A. | 1mol维生素P最多可以和5mol溴水发生加成反应 | |
| B. | 可溶于有机溶剂 | |
| C. | 分子中有三个苯环 | |
| D. | 1mol维生素P最多可以和4molNaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 124 g P4含有P-P键的个数为4NA | |
| B. | 12 g石墨中含有C-C键的个数为1.5NA | |
| C. | 12 g金刚石中含有C-C键的个数为4NA | |
| D. | 60gSiO2中含Si-O键的个数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第IA族的所有元素都是金属元素 | |
| B. | 同周期主族元素中,第ⅦA族元素原子半径最小 | |
| C. | 稀有气体元素原子的最外层电子数均为8 | |
| D. | 一般在元素周期表的金属与非金属分界线附近寻找一些化学反应新型催化剂 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上月考一化学试卷(解析版) 题型:填空题
按要求回答下列有关问题。
(1)汽车尾气净化的主要原理为:2NO(g)+2CO(g)=N2(g)+2CO2(g);△H<0,在一定温度下,在一体积固定的密闭容器中充入一定量的NO和CO达到平衡状态。若要同时提高该反应的速率和NO的转化率,采取的措施有 、 。(写出2个)
(2)对反应N2O4(g) 2NO2(g) △H>0 在温度为Tl、T2时平衡体系中NO2的体积分数随压强变化曲线如图所示,下列说法正确的是__________。
2NO2(g) △H>0 在温度为Tl、T2时平衡体系中NO2的体积分数随压强变化曲线如图所示,下列说法正确的是__________。

a.A、C两点的反应速率:A>C
b.A、C两点气体的颜色:A浅,C深
c.由状态A到状态B,可以用加热的方法
d.A、C两点的化学平衡常数:A>C
(3)某温度下,在一个2 L的密闭容器中,加入4 mol A和2 mol B进行如下反应:3A(g)+2B(g) 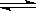 4C(?)+2D(?)。反应一段时间后达到平衡,测得生成1.6 mol C,且反应的前后压强之比为5∶4(相同的温度下测量)。则该反应的化学平衡常数:K=____________。
4C(?)+2D(?)。反应一段时间后达到平衡,测得生成1.6 mol C,且反应的前后压强之比为5∶4(相同的温度下测量)。则该反应的化学平衡常数:K=____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com