
【题目】下图是部分短周期元素化合价与原子序数的关系图六,下列说法正确的是
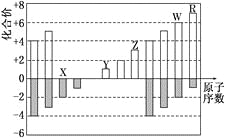
A. 原子半径:Z>Y>X
B. 气态氢化物的稳定性:R>W
C. WX3和水反应形成的化合物是离子化合物
D. Y和Z两者最高价氧化物对应的水化物的碱性:Y<Z
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:
【题目】如图是由乙烯合成乙酸乙酯的几种可能的合成路线: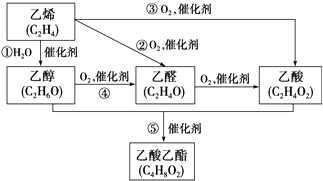
(1)乙酸乙酯的结构简式为;
(2)乙醇中含氧官能团的名称是;
(3)请写出反应④的化学方程式:;
(4)写出上述几种路线中涉及到的有机化学反应基本类型:反应①: , 反应⑤: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.使pH试纸显深蓝色的溶液中:NH ![]() 、NO
、NO ![]() 、SO42﹣、Na+
、SO42﹣、Na+
B.由水电离的c(H+)=1×10﹣14mol?L﹣1的溶液中:Ca2+、K+、HCO ![]() 、NO
、NO ![]()
C.pH=1的无色溶液中:K+、Fe3+、SO ![]() 、SCN﹣
、SCN﹣
D.![]() =1012的溶液中:Mg2+、Al3+、NO
=1012的溶液中:Mg2+、Al3+、NO ![]() 、Cl﹣
、Cl﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种盐X与烧碱混合共热,可放出无色气体Y,Y经一系列氧化后再溶于水可得Z溶液,Y和Z反应又生成X,则X是( )
A.(NH4)2SO4B.NH4NO3
C.NH4ClD.NH4HCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雾霾严重影响人们的生活,汽车尾气排放是造成雾霾天气的重要原因之一.已知汽车尾气排放时容易发生以下反应:①N2(g)+O2(g)2NO(g)△H1=a kJmol﹣1
②2NO(g)+O2(g)=2NO2(g)△H2=b kJmol﹣1
③CO(g)+ ![]() O2(g)CO2(g)△H3=c kJmol﹣1
O2(g)CO2(g)△H3=c kJmol﹣1
④2CO(g)+2NO(g)N2(g)+2CO2(g)△H4
请回答下列问题:
(1)根据反应①②③,确定反应④中△H4=kJmol﹣1 .
(2)对于气体参与的反应,表示平衡常数Kp时用气体组分(B)的平衡压强p(B)代替该气体物质的量浓度c(B),则反应①的Kp=(用表达式表示).
(3)下列情况能说明反应②已达平衡状态的是(填编号).
A.单位时间内生成1mol NO2的同时消耗了1mol NO
B.在恒温恒容的容器中,混合气体的密度保持不变
C.在恒温恒压的容器中,容器的体积保持不变
D.混合气体的平均相对分子质量保持不变
(4)反应③在(填“高温”或“低温”)下不利于自发进行.
(5)探究反应④中NO的平衡转化率与压强、温度的关系,得到如图所示的曲线.试分析实际化工生产中不采用高压的原因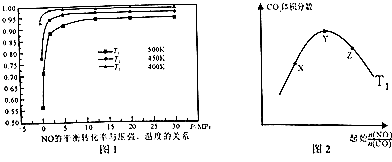
(6)探究反应④中平衡时CO2的体积分数与反应物中 ![]() 的比值、温度的关系,得到如图2所示的曲线. ①在X、Y、Z三点中,CO的转化率从大到小的顺序是 .
的比值、温度的关系,得到如图2所示的曲线. ①在X、Y、Z三点中,CO的转化率从大到小的顺序是 .
②若保持其他条件不变,请在图2中,画出温度为T2(T2<T1)时的变化趋势曲线 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有物质A﹣H的转化关系如图: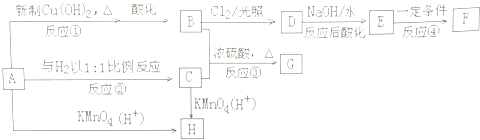
若A的分子式为C8H8O,其苯环上的一溴代物只有两种:F为高分子化合物.请回答下列问题:
(1)反应②的反应类型是 . D中含氧官能团的名称是 .
(2)写出有关物质的结构简式:E , H .
(3)写出下列反应的化学方程式:A与新制Cu(OH)2的反应;B+C→G .
(4)B的同分异构体且属于酯类的芳香族化合物共有6种,以下已有四种.请写出另两种同分异构体的结构简式:、 . ![]()
(5)E的一种同分异构体苯羟乙酸是一种化工产品.请结合题目中有关信息,设计以苯乙烯为原料,制备苯羟乙酸的合成路线(用流程图表示,无机试剂任选).注:合成路线的书写格式参照如下示例流程图:
CH3CHO ![]() CH3COOH
CH3COOH ![]() CH3COOCH2CH3 .
CH3COOCH2CH3 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. 已知t1℃时,反应C+CO2![]() 2CO ΔH >0的速率为υ,若升高温度,逆反应速率减小
2CO ΔH >0的速率为υ,若升高温度,逆反应速率减小
B. 恒压容器中发生反应N2+O2![]() 2NO,若在容器中充入He,正逆反应速率均不变
2NO,若在容器中充入He,正逆反应速率均不变
C. 当一定量的锌粉和过量的6molL-1盐酸反应时,为了减慢反应速率,又不影响产生H2的总量,可向反应器中加入少量的CuSO4溶液
D. 对于工业合成氨反应N2+3H2![]() 2NH3,选用450℃主要为了提高催化剂(铁触媒)的催化效率
2NH3,选用450℃主要为了提高催化剂(铁触媒)的催化效率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列元素的原子半径:根据以上数据,磷原子的半径(10-10m)可能是( )
元素 | N | S | O | Si |
原子半径/10-10m | 0.75 | 1.02 | 0.74 | 1.17 |
A.0.80B.1.15C.1.19D.0.70
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com