
| A. | Na+、HCO3-、Ca2+、Cl- | B. | Ba2+、K+、OH-、NO3- | ||
| C. | H+、Fe3+、NH4+、SO42- | D. | Mg2+、Na+、Cl-、CO32- |
分析 根据离子之间不能结合生成沉淀、气体、水等,则离子大量共存,并结合加入OH-有沉淀析出,加入H+能放出气体来解答.
解答 解:A.该组离子之间不反应,可大量共存,加入OH-与HCO3-、Ca2+反应生成碳酸钙沉淀析出,加入H+与HCO3-反应放出气体,故A正确;
B.该组离子之间不反应,可大量共存,但加入OH-没有沉淀析出,加入H+没有放出气体,故B错误;
C.该组离子之间不反应,可大量共存,但加入H+没有放出气体,故C错误;
D.Mg2+、CO32-结合生成沉淀,不能大量共存,故D错误;
故选A.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意复分解反应的条件,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 用100mL量筒取5.0mL稀硫酸 | |
| B. | 用托盘天平准确称取2.50gNaCl固体 | |
| C. | 实验室制取蒸馏水的装置中,温度计水银球应插入蒸馏烧瓶液面以下 | |
| D. | 配制240mL0.1mol/LNaOH溶液应该选择250mL的容量瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol液态肼在足量氧气中完全燃烧生成水蒸气,放出642kJ的热量:N2H4(l)+O2(g)═N2(g)+2H2O(g)△H=+642 kJ•mol-1 | |
| B. | 101 kPa下,26 g乙炔在足量氧气中完全燃烧生成液态水,放出1 299.6 kJ的热量:C2H2(g)+$\frac{5}{2}$O2(g)═2CO2(g)+H2O(l)△H=-1 299.6 kJ | |
| C. | 12 g石墨转化为CO时,放出110.5 kJ的热量:2C(石墨,s)+O2(g)═2CO(g)△H=-110.5 kJ•mol-1 | |
| D. | 1 mol B2H6气体完全燃烧生成固态三氧化二硼和液态水,放出2 165 kJ的热量:B2H6(g)+3O2(g)═B2O3(s)+3H2O(l)△H=-2 165 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 雪白、漂亮的“白木耳”,可能是在用硫黄熏制的过程中产生的SO2所致 | |
| B. | 钢铁在潮湿的空气中放置,易发生化学腐蚀而生锈 | |
| C. | 绿色化学的核心是从源头上消除工业生产对环境的污染 | |
| D. | 硅胶可用作食品干燥剂和催化剂载体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
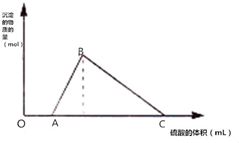 将M克钠和铝的混合物投入到一定量的水中,金属全部溶解,并收集到标准状况下体积为N升的气体,在所得溶液中逐滴加入1mol/L H2SO4,所得沉淀的物质的量随滴入硫酸溶液的体积变化如图所示;已知:A、C点对应的横坐标数据分别是500mL和2500mL,则
将M克钠和铝的混合物投入到一定量的水中,金属全部溶解,并收集到标准状况下体积为N升的气体,在所得溶液中逐滴加入1mol/L H2SO4,所得沉淀的物质的量随滴入硫酸溶液的体积变化如图所示;已知:A、C点对应的横坐标数据分别是500mL和2500mL,则查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 L 0.1 mol L-1NaHCO3溶液含有0.1NA个HCO3- | |
| B. | 1L0.1mol•L-1乙酸溶液电离的H+数为0.1NA | |
| C. | 2.8 g乙烯与丙烯的混合物中含碳原子的数目为0.2 NA | |
| D. | 标准状况下,22.4L溴苯的分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 将含有少量CO2的CO通入足量Na2O2的试管中并不断用电火花引燃 | |
| B. | 向等物质的量的干冰和CaO的混合物中加几滴水 | |
| C. | 将1molCu置于含2molH2SO4的浓溶液中加热 | |
| D. | 在强光持续照射下,向过量的Ca(ClO)2浊液中通入少量的CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com