
已知:101kPa时,辛烷的燃烧热为5518kJ·mol-1,强酸与强碱在稀溶液中发生反应时的中和热为57.3kJ·mol-1,则下列热化学方程式书写正确的是 ( )
① C8H18(l)+ O2(g)= 8CO2(g)+9H2O(g);△H = -5518kJ·mol-1
O2(g)= 8CO2(g)+9H2O(g);△H = -5518kJ·mol-1
② C8H18(l)+ O2(g)= 8CO2(g)+9H2O(l);△H = -5518kJ·mol-1
O2(g)= 8CO2(g)+9H2O(l);△H = -5518kJ·mol-1
③ H+ + OH- = H2O;△H = -57.3kJ·mol-1
④ NaOH(aq)+ H2SO4(aq)
H2SO4(aq)  Na2SO4(aq)+H2O(l);△H= +57.3kJ·mol-1
Na2SO4(aq)+H2O(l);△H= +57.3kJ·mol-1
A.①③ B.② C.②④ D.②③
科目:高中化学 来源: 题型:

| ||
| ||

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
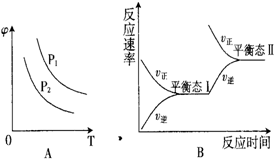 硫酸生产过程中关键阶段的反应为:
硫酸生产过程中关键阶段的反应为:| 催化剂 | 加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、有水生成的反应都是放热反应 | B、稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量 | C、24g C与1L O2反应生成2L CO时放出221kJ热量 | D、碳的燃烧热大于110.5 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
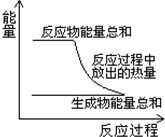 已知在101KPa时:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-820KJ?mol-1.则下列说法中正确的是( )
已知在101KPa时:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-820KJ?mol-1.则下列说法中正确的是( )| A、反应过程中的能量变化关系可如图所示 | B、11.2LCH4完全燃烧放出热量410KJ | C、CH4的燃烧热为820KJ | D、凡是有水生成的氧化还原反应都是放热反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com