

| 32 |
| X |
| 32 |
| X |


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
| 0.64V |
| w |
| 0.64V |
| w |
查看答案和解析>>
科目:高中化学 来源:2012年普通高等学校招生全国统一考试理综化学部分(安徽卷带解析) 题型:单选题
(15分)亚硫酸盐是一种常见食品添加剂。为检验某食品中亚硫酸盐含量(通常1kg样品中含SO2的质量计),某研究小组设计了如下两种实验流程:
(1)气体A的主要成分是 ,为防止煮沸时发生暴沸,必须先向烧瓶中加入
;通入N2的目的是 。
(2)写出甲方案第①步反应的离子方程式: 。
(3)甲方案第②步滴定前,滴定管需用NaOH标准溶液润洗,其操作方法是
。
(4)若用盐酸代替稀硫酸处理样品,则按乙方案实验测定的结果 (填“偏高”、“偏低”或“无影响”)
(5)若取样品wg,按乙方案测得消耗0.01000mol·L—1I2溶液VmL,则1kg样品中含SO2的质量是 g(用含w、V的代数式表示)。
查看答案和解析>>
科目:高中化学 来源:2012年普通高等学校招生全国统一考试理综化学部分(安徽卷解析版) 题型:选择题
(15分)亚硫酸盐是一种常见食品添加剂。为检验某食品中亚硫酸盐含量(通常1kg样品中含SO2的质量计),某研究小组设计了如下两种实验流程:
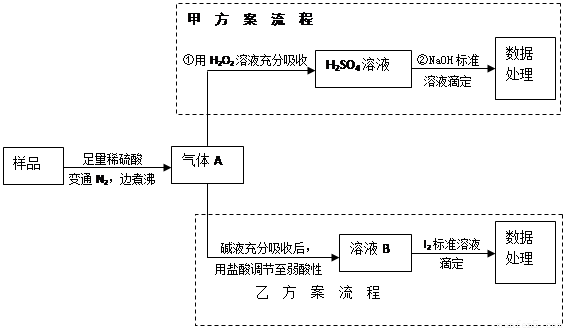
(1)气体A的主要成分是 ,为防止煮沸时发生暴沸,必须先向烧瓶中加入
;通入N2的目的是 。
(2)写出甲方案第①步反应的离子方程式: 。
(3)甲方案第②步滴定前,滴定管需用NaOH标准溶液润洗,其操作方法是
。
(4)若用盐酸代替稀硫酸处理样品,则按乙方案实验测定的结果 (填“偏高”、“偏低”或“无影响”)
(5)若取样品wg,按乙方案测得消耗0.01000mol·L—1I2溶液VmL,则1kg样品中含SO2的质量是 g(用含w、V的代数式表示)。
查看答案和解析>>
科目:高中化学 来源:2013年山东省潍坊市高考化学仿真试卷(二)(解析版) 题型:填空题
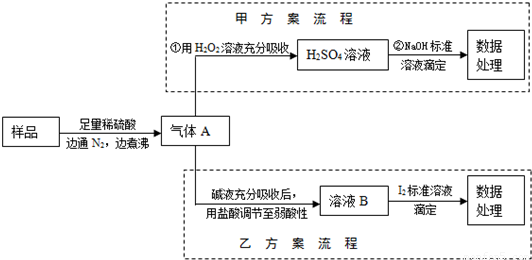
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com