
在复杂的体系中,确认化学反应先后顺序有利于解决问题,下列化学反应先后顺序判断正确的是
A.在含AlO2-、SO32-、OH-的溶液中逐滴加入硫酸氢钠溶液:OH-、AlO2-、SO32-
B.含等物质的量的FeBr2、FeI2的溶液中,缓慢通入氯气:I-、Br-、Fe2+
C.含等物质的量的Ba(OH)2、KOH的溶液中,缓慢通入CO2:KOH、Ba(OH)2、K2CO3、BaCO3
D.在含Fe3+、H+、NH4+的溶液中逐渐加入烧碱溶液:H+、NH4+、Fe3+
A
【解析】
试题分析:A、在含AlO2-、SO32-、OH-的溶液中逐滴加入硫酸氢钠溶液,硫酸氢钠电离产生的氢离子先与氢氧根离子反应,若再与亚硫酸根离子先反应生成的二氧化硫溶于水使溶液显酸性,又与偏铝酸根离子反应生成氢氧化铝沉淀和亚硫酸根离子,实际相当于先与偏铝酸根离子反应,最后与亚硫酸根离子反应,正确;B、根据离子的还原性的强弱,判断氯气先与碘离子反应,再与亚铁离子反应,最后与溴离子反应,错误;C、二氧化碳通入混合液中,先与氢氧根离子反应生成碳酸根离子,由于溶液中存在钡离子,所以生成碳酸钡沉淀,实质相当于先与氢氧化钡反应,再与氢氧化钾反应,再与碳酸钾、碳酸钡反应,错误;D、氢氧根离子先与氢离子反应,因为铵根离子与强碱溶液反应。而此时溶液呈弱酸性,所以氢氧根离子再与铁离子反应,最后与铵根离子反应,错误,答案选A。
考点:考查离子反应的顺序的判断


科目:高中化学 来源:2015届江西省高三上学期第一次月考化学试卷(解析版) 题型:选择题
下图是CO2电催化还原为CH4的工作原理示意图。下列说法不正确的是
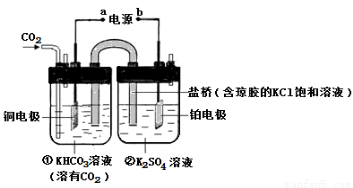
A.该过程是电能转化为化学能的过程
B.一段时间后,①池中n(KHCO3)不变
C.一段时间后,②池中溶液的pH一定下降
D.铜电极的电极反应式为CO2+8H++8e-=CH4+2H2O
查看答案和解析>>
科目:高中化学 来源:2015届江西省南昌市三校高三上第一次联考化学试卷(解析版) 题型:填空题
(10分)越来越多的食品问题所造成的危害有目共睹,给我们敲响了警钟。一些“毒奶粉”竟然顶着国家“免检产品”桂冠。某品牌奶粉被鉴定为所含亚硝酸盐残留量高出正常值7. 8倍,长期食用可能致癌。NaNO2有像食盐一样的咸味,能发生如下反应:
2NaNO2+4HI=2NO+I2+2NaI+2H2O。
(1)上述反应中氧化剂是______,若有1.75 mol的还原剂被氧化,则被还原的氧化剂是_______mol。
(2)根据上述反应,可以用试纸和生活中常见的物质进行实验,以鉴别NaNO2和NaCl,可选用的物质有:①自来水、②碘化钾淀粉试纸、③淀粉、④白糖、⑤食醋、⑥白酒。进行实验时,必须选用的物质有________。(填编号)
(3)某厂废切削液中,含2%~5%的NaNO2,直接排放会造成污染,下列试剂__________能使NaNO2转化为不引起二次污染的N2。(填编号)
①NaCl ②NH4Cl ③H2O2 ④浓H2SO4
反应的化学方程式为____________________________________________。
查看答案和解析>>
科目:高中化学 来源:2015届江西省南昌市三校高三上第一次联考化学试卷(解析版) 题型:选择题
室温时,两个容积相同的烧瓶中分别盛有M和N两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体接触(如图),容器内的压强由大到小的顺序是
编号 | ① | ② | ③ | ④ |
气体M | H2S | H2 | NH3 | NO |
气体N | SO2 | Cl2 | HCl | O2 |
A.①②③④ B.①④③② C.②④①③ D.④①②③
查看答案和解析>>
科目:高中化学 来源:2015届江西省高三上学期第一次考试化学试卷(解析版) 题型:计算题
(9分)(1)在标准状况下,将224 L HCl气体溶于635 mL水中,所得盐酸的密度为
1.18 g·cm-3。试计算:
①所得盐酸物质的量浓度是 。
②取出这种盐酸10 mL,稀释至118 mL,所得稀盐酸的物质的量浓度是 。如取10 mL盐酸时仰视其他操作均正确得稀盐酸浓度 。(填“偏大”、 “等于”、“偏小”)
③在40.0 mL 0.065 mol·L-1 Na2CO3溶液中,逐渐加入(2)所稀释的稀盐酸,边加边振荡。若使反应不产生CO2气体,加入稀盐酸的体积最多不超过 mL。
(2)配制0.80 mol·L-1 NaOH溶液475 mL,回答下列问题:
①根据计算用托盘天平称取NaOH的质量为__________g。在实验中其他操作均正确,若容量瓶用蒸馏水洗涤后未干燥,则所得溶液浓度_______0.80 mol·L-1(填“大于”、“等于”或“小于”,下同)。若还未等溶液冷却就定容了,则所得溶液浓度__________0.80 mol·L-1。
②0.80 mol·L-1 NaOH溶液质量分数 3.2%,和等质量的水混合溶液浓度 0.40 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2015届江西省高三上学期第一次考试化学试卷(解析版) 题型:选择题
磁流体是电子材料的新秀,它既具有固体的磁性,又具有液体的流动性,制备时将含等物质的量的FeSO4和Fe2(SO4)3的溶液混合,再滴入稍过量的NaOH溶液,随后加入油酸钠溶液,即可生成黑色的、分散质粒子直径在36~55 nm的磁流体。下列说法中正确的是
A.所得的分散系属于悬浊液
B.该分散系能产生丁达尔效应
C.所得的分散系中分散质为Fe2O3
D.所得分散系为胶体,且胶粒直径即为氢氧化铁分子直径
查看答案和解析>>
科目:高中化学 来源:2015届江西省高三上学期第一学期月考化学试卷(解析版) 题型:实验题
(16分)某小组为测定某碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数,甲、乙两组同学分别进行了下列相关实验。
方案Ⅰ.甲组同学用沉淀分析法,按如下图所示的实验流程进行实验:[已知Ba(HCO3)2可溶于水]
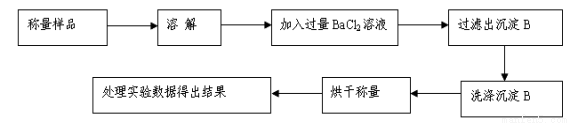
(1)实验时,过滤操作中,除了玻璃棒、漏斗外,还要用到的玻璃仪器为 。
(2)洗涤沉淀B的操作是 。
(3)若实验中测得样品质量为m g,沉淀质量为n g,则碳酸钠的质量分数为____________。
方案Ⅱ.乙组同学的主要实验流程图如下:
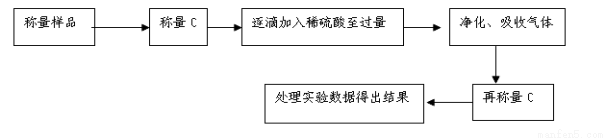
按如下左图所示装置进行实验:
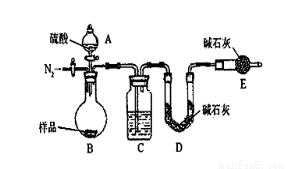
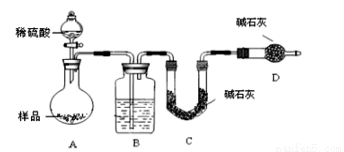
(4)该实验中装置B盛放的物质是_____________________,分液漏斗中 (填“能”或“不能”)用盐酸代替稀硫酸进行实验。
(5)在C中装碱石灰来吸收净化后的气体。
①样品中碳酸钠的质量分数越大,则实验中干燥管C在充分吸收气体前后的质量差____________________。(填“越大”、“越小”或“不变化”)
②D装置的作用是_________________________。
(6)有同学认为为了减少实验误差,在反应前后都要通入N2(如上右图),反应后通入
N2的目的是______________________________。
查看答案和解析>>
科目:高中化学 来源:2015届江西省高三上学期第一学期月考化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值。下列说法正确的是
A.常温常压下,14g由N2与CO组成的混合气体含有的原子数目为2NA
B.1L 1mol·L-1的NaClO 溶液中含有ClO-的数目为NA
C.质量a g的C2H4和C3H6的混合物中共用电子对数目为3a NA /14
D.常温下,pH=13的NaOH溶液中含有OH一的数目为0.1NA
查看答案和解析>>
科目:高中化学 来源:2015届江苏省苏州市高三9月学情调研化学试卷(解析版) 题型:选择题
下列物质性质与应用对应关系正确的是
A.漂白粉在空气中不稳定,可用于漂白纸张
B.医用酒精能使蛋白质变性,可用于消毒杀菌
C.二氧化硅不与强酸反应,可用石英器皿盛放氢氟酸
D.铜的金属活泼性比铁的弱,可在铁闸上装若干铜块以减缓其腐蚀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com