
| A. | 常温下,1L0.1mol/LNH4NO3溶液中的氮原子数为0.2NA | |
| B. | 常温下,向含1molH2SO4的浓硫酸加入足量的铁粉,转移的电子数为2NA | |
| C. | 标准状况下,2.24L己烷分子中含有1.9NA对共用电子 | |
| D. | 将1mol明矾晶体完全溶于水制成胶体,其中所含胶体微粒数目为NA |
分析 A.根据n=nM计算出该溶液中含有硝酸铵的物质的量,然后利用N守恒计算出含有的氮原子数目;
B.常温下铁与浓硫酸发生钝化,阻止了反应的继续进行;
C.标准状况下,己烷的状态不是气体;
D.氢氧化铝胶体为氢氧化铝的聚集体,无法计算含有胶粒数目.
解答 解:A.1L0.1mol/LNH4NO3溶液中含有硝酸铵的物质的量为:0.1mol/L×1L=0.1mol,0.1molNH4NO3中含有0.2molN原子,含有氮原子数为0.2NA,故A正确;
B.常温下Fe与浓硫酸发生了钝化现象,则无法计算转移电子数,故B错误;
C.标准状况下己烷不是气体,不能使用标准状况下的气体摩尔体积计算2.24L己烷的物质的量,故C错误;
D.将1mol明矾晶体完全溶于水制成胶体,由于氢氧化铝胶体为氢氧化铝的聚集体,则无法计算该胶体中含有胶粒数目,故D错误;
故选A.
点评 本题考查了阿伏伽德罗常数的综合应用,题目难度不大,明确标准状况下气体摩尔体积的使用条件为解答结构,注意熟练掌握物质的量与阿伏伽德罗常数、摩尔质量等之间的关系,试题培养了学生的分析能力及化学计算能力.


 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:选择题
| A. | 羽毛球拍属于复合材料 | B. | 包装纸箱属于无机材料 | ||
| C. | 塑料笔杆属于高分子材料 | D. | 生肖纪念币属于合金材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
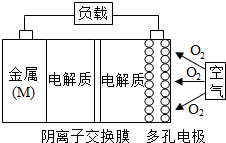 金属(M)-空气电池(如图)具有原料易得,能量密度高等优点,有望成为新能源汽车和移动设备的电源,该类电池放电的总反应方程式为:4M+nO2+2nH2O=4M(OH)n,已知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能,下列说法不正确的是( )
金属(M)-空气电池(如图)具有原料易得,能量密度高等优点,有望成为新能源汽车和移动设备的电源,该类电池放电的总反应方程式为:4M+nO2+2nH2O=4M(OH)n,已知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能,下列说法不正确的是( )| A. | 采用多孔电极的目的是提高电极与电解质溶液的接触面积,并有利于氧气扩散至电极表面 | |
| B. | 比较Mg,Al,Zn三种金属-空气电池,Al-空气电池的理论比能量最高 | |
| C. | M-空气电池放电过程的正极反应式:4M++nO2+2nH2O+4ne-=4M(OH)n | |
| D. | 在Mg-空气电池中,为防止负极区沉积Mg(OH)2,宜采用中性电解质及阳离子交换膜 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
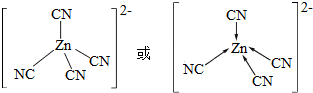 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用热的纯碱可除去炊具上的油污 | |
| B. | 垃圾是放错地方的资源,应分类回收利用 | |
| C. | 石油分馏可获得乙烯、丙烯和丁二烯 | |
| D. | 红葡萄酒储藏时间长后变香是因为乙醇发生了酯化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 14g乙烯与14g苯含有的氢原子数均为2NA | |
| B. | 0.1molFe3+与足量的HI溶液反应,转移的电子数为0.1NA | |
| C. | 1L0.1mol•L-1NaHS溶液中,HS-与H2S数目之和为0.1NA | |
| D. | 6.4g铜溶于30mL10mol•L-1硝酸中,产生气体的分子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同周期元素中,ⅦA族元素的原子半径最大 | |
| B. | 原子核外各电子层容纳的电子数为2n2个 | |
| C. | 核外电子的分层排布就是核外电子的分层运动 | |
| D. | ⅥA族元素的原子,其半径越大,越容易得电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
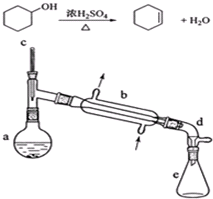
| 相对分子质量 | 密度(g/cm3) | 沸点/℃ | 溶解性 | |
| 环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正极反应式为O2+4e-═2O2- | |
| B. | 放电时溶液中的阳离子向正极方向移动 | |
| C. | 该电池反应为CH4+2O2═CO2+2H2O | |
| D. | 通入CH4一极的电极反应式为CH4+2O2+8e-═CO2+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com