

| 容积 | 容积/L | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | |
| C(s) | H2O | H2 | ||||
| 甲 | 2 | T1 | 2 | 4 | 3.2 | 8 |
| 乙 | 1 | T2 | 1 | 2 | 1.2 | 3 |
分析 Ⅰ、(1)前5min 内生成CaO的质量为11.2g,n(CO)=n(CaO)=$\frac{11.2g}{56g/mol}$=0.2mol,则v(CO)=$\frac{0.2mol}{1L•5min}$=0.04mol•L-1•min-1;该反应中只有CO和CO2为气体,将容器体积由1L压缩为0.5L,气体浓度增大,平衡逆向移动,温度不变,平衡常数不变,即K=[CO]•[CO2]不变,据此分析;
(2)该反应的K=$\frac{[{C}_{2}{{O}_{4}}^{2-}]}{[C{{O}_{3}}^{2-}]^{\;}}$=$\frac{[{C}_{2}{{O}_{4}}^{2-}]•[C{a}^{2+}]}{[C{{O}_{3}}^{2-}]•[C{a}^{2+}]}$=$\frac{Ksp(CaC{{\;}_{2}O}_{4})}{Ksp(CaC{O}_{3})}$=$\frac{5.0×1{0}^{-9}}{2.5×1{0}^{-9}}$=2.0,设c(CO32-)转化了x,则生成c(C2O42-)=x,剩余c(CO32-)=(0.6-x),结合K的表达式计算;
Ⅱ、根据图象,反应①在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下反应相同时间后,CH4的转化率为Ⅰ>Ⅱ>Ⅲ,结合催化剂只改变反应速率不改变平衡移动,所以最终不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下达平衡时CH4的转化率相同,据此分析;
Ⅲ、从表中数据可知,甲乙两容器中反应物浓度相同,乙达到平衡所有时间短,说明T2温度高,乙中水的转化率低,说明温度越高反应物转化率越低,正反应放热.
解答 解:Ⅰ、(1)前5min 内生成CaO的质量为11.2g,n(CO)=n(CaO)=$\frac{11.2g}{56g/mol}$=0.2mol,则v(CO)=$\frac{0.2mol}{1L•5min}$=0.04mol•L-1•min-1;
A、该反应中只有CO和CO2为气体,将容器体积由1L压缩为0.5L,气体浓度增大,平衡逆向移动,CaC2O4的分解率减小,故A错误;
B、温度不变,平衡常数不变,故B错误;
C、温度不变,平衡常数不变,即K=[CO]•[CO2]不变,所以平衡移动后,CO和CO2的浓度都没有改变,故C正确;
D、平衡逆向移动,CaO质量减小,故D正确;
故答案为:0.04;CD;
(2)该反应的K=$\frac{[{C}_{2}{{O}_{4}}^{2-}]}{[C{{O}_{3}}^{2-}]^{\;}}$=$\frac{[{C}_{2}{{O}_{4}}^{2-}]•[C{a}^{2+}]}{[C{{O}_{3}}^{2-}]•[C{a}^{2+}]}$=$\frac{Ksp(CaC{{\;}_{2}O}_{4})}{Ksp(CaC{O}_{3})}$=$\frac{5.0×1{0}^{-9}}{2.5×1{0}^{-9}}$=2.0,设c(CO32-)转化了x,则生成c(C2O42-)=x,剩余c(CO32-)=(0.6-x),可得方程:$\frac{x}{0.6-x}$=2.0,解得x=0.4 mol•L?1,
故答案为:0.4;
Ⅱ、(1)根据图象,反应①在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下反应相同时间后,CH4的转化率为Ⅰ>Ⅱ>Ⅲ,所以三种催化剂Ⅰ、Ⅱ、Ⅲ的催化效率由高到低的顺序是
Ⅰ>Ⅱ>Ⅲ,故答案为:Ⅰ>Ⅱ>Ⅲ;
(2)因为催化剂只改变反应速率不改变平衡移动,所以最终不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下达平衡时CH4的转化率相同,故a点所代表的状态没有达到平衡状态,反应正向进行,正反应速率大于逆反应速率,故答案为:大于;
(3)此时反应一直向正反应方向移动,b和c都没平衡,c点温度高,反应速率快,相同时间内转化率高,所以c点CH4的转化率高于b点,故答案为:b和c都没平衡,c点温度高,反应速率快,相同时间内转化率高;
Ⅲ、(1)从表中数据可知,甲乙两容器中反应物浓度相同,乙达到平衡所有时间短,说明T2温度高,故答案为:甲乙两容器中反应物浓度相同,乙达到平衡所有时间短,说明T2温度高;
(2)乙中水的转化率低,说明温度越高反应物转化率越低,正反应放热,升温反应物转化率降低,故答案为:变小.
点评 本题考查了化学反应速率的求算、化学平衡的移动以及据化学平衡常数判断平衡状态、沉淀转化的计算、图象分析、影响平衡移动的因素,题目难度较大.


科目:高中化学 来源: 题型:选择题
| A. | 惰性电极电解饱和食盐水,若电路中通过NA个电子,则阳极产生气体11.2L | |
| B. | 标准状况下,4.0 g CH4中含有共价键的数目为NA | |
| C. | 1 mol C12发生化学反应,转移的电子数必为2NA | |
| D. | 在反应KIO3+6HI=KI+3I2+3H2O中,每生成3mol I2转移的电子数为6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式为C7H8O,且属于芳香族化合物的同分异构体只有4种 | |
| B. | 甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物最多有6种 | |
| C. | 丙烷的一氯代物有2种,丙烷的二氯代物有4种 | |
| D. | 联苯(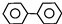 )的一氯代物有3种,二氯代物有12种 )的一氯代物有3种,二氯代物有12种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铝、氢氧化钠、碳酸钠都是常见的胃酸中和剂 | |
| B. | 研发易降解的生物农药有利于环境保护 | |
| C. | 做衣服的棉、麻、蚕丝的成分都是纤维素 | |
| D. | 常用无水酒精来消毒,是因为酒精能够使细菌蛋白发生变性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
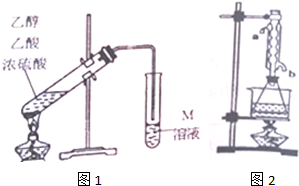
| 相对分子质量 | 沸点(℃) | |
| 乙醇 | 46 | 78.5 |
| 乙酸 | 60 | 117.9 |
| 乙酸乙酯 | 88 | 77.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 实验步骤 | 实验现象 |
| ①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 | 镁浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色. |
| ②在盛有冷水的烧杯中滴入几滴酚酞溶液,再将一小块金属钠放入其中 | 有气体产生,溶液变成浅红色 |
| ③将镁条投入稀盐酸中 | 剧烈反应,迅速产生大量无色气体 |
| ④将铝条投入稀盐酸中 | 反应不十分剧烈;产生无色气体 |
| ⑤向A1Cl3溶液中滴加NaOH溶液至过量 | 生成白色胶状沉淀,继而沉淀消失 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序 号 | 实 验 目 的 | 答案 | 供选择的化学试剂及方法 |
| (1) | 实验室检验二氧化碳气体 | F | A让激光透过 B 滴入无色KSCN溶液 C抽少许纱,灼烧 D新制的Cu(OH)2,加热 E通过盛溴水的洗气瓶 F通入澄清石灰水中 |
| (2) | 鉴别溶液和胶体 | A | |
| (3) | 化验糖尿病 | D | |
| (4) | 鉴别Fe2+和Fe3+ | B | |
| (5) | 识别棉织品和毛织品 | C |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
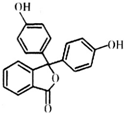 酚酞医药名为果桃,可治疗消化系统疾病,其有效成分的结构简式如图所示.下列对该有效成分的说法正确的是( )
酚酞医药名为果桃,可治疗消化系统疾病,其有效成分的结构简式如图所示.下列对该有效成分的说法正确的是( )| A. | 所有原子可能共平面 | |
| B. | 能发生加聚反应生成高分子化合物 | |
| C. | 酚酞的水解产物中含有醇羟基 | |
| D. | 1 mol该物质最多能与含4 mol NaOH的烧碱溶液反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com