

分析 含锗烟尘中含有ZnO、CeO2、SiO2,加入稀硫酸过滤,溶解的有ZnO、CeO2,第①步中不溶于稀硫酸的滤渣主要成分有SiO2,滤液中加入有机萃取剂萃取得到有机层萃取层中加入氢氧化钠进行反萃取得到水层,加入盐酸得到GeCl4,加入纯水过滤得到GeO2•nH2O,加热分解得到GeO2;
(1)根据题目中的流程可以看出第①步中不溶于稀硫酸的滤渣主要成分有SiO2、PbO,实验室蒸馏操作用到的玻璃仪器有分液漏斗、烧杯.
(2)第③步萃取时,从生产成本角度考虑,由图可知有机萃取剂的用量在V水相/V有机相的值为8时比V水相/V有机相的值为4时少,此时萃取率处于较高水平,而有机萃取剂较贵,故V水相/V有机相的值为8时较适宜.
(3)第④步加入盐酸作用为中和NaOH,作反应物,抑制GeCl4水解.
(4)第⑤步反应GeCl4水解得到氯化氢和GeO2?nH2O;
(5)检验GeO2•nH2O是否洗涤干净的操作是取最后一次洗涤液于试管中,检验是否含有氯离子设计实验验证.
解答 解:(1)根据题目中的流程可以看出,含锗烟尘中含有ZnO、CeO2、SiO2,加入稀硫酸过滤,溶解的有ZnO、CeO2,第①步中不溶于稀硫酸的滤渣主要成分有SiO2,锥形瓶、牛角管、温度计、酒精灯、冷凝管和蒸馏烧瓶,
故答案为:SiO2;蒸馏烧瓶;
(2)第③步萃取时,从生产成本角度考虑,由图可知有机萃取剂的用量在V水相/V有机相的值为8时比V水相/V有机相的值为4时少,此时萃取率处于较高水平,而有机萃取剂较贵,从生产成本角度考虑,故V水相/V有机相的值为8时较适宜;
故答案为:8;
(3)第④步加入盐酸作用为中和NaOH,作反应物,同时抑制GeCl4水解;
故答案为:中和NaOH,作反应物,抑制GeCl4水解;
(4)第⑤步反应是GeCl4水解得到氯化氢和GeO2?nH2O,反应的化学方程式:GeCl4+(n+2)H2O=GeO2?nH2O+4HCl;
故答案为:GeCl4+(n+2)H2O=GeO2?nH2O+4HCl;
(5)检验GeO2•nH2O是否洗涤干净的操作是:取最后一次洗涤液于试管中,往其中加入HNO3酸化的AgNO3溶液,若不产生白色沉淀,则说明洗涤干净.若产生白色沉淀,则说明未洗涤干净;
故答案为:取最后一次洗涤液于试管中,往其中加入HNO3酸化的AgNO3溶液,若不产生白色沉淀,则说明洗涤干净.若产生白色沉淀,则说明未洗涤干净.
点评 本题考查制备实验方案设计,为高考高频点,此种题型涉及物质性质、实验基本操作,明确物质的性质及每一步发生的反应、基本操作方法是解本题关键,熟练掌握元素化合物知识,灵活运用知识解答问题,题目难度中等.


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | M气体是密度最小的气体 | |
| B. | X的氧化物与Y的最高价氧化物对应水化物能发生化学反应 | |
| C. | Z在周期表的第五周期,ⅤA族 | |
| D. | X的离子比Y离子半径小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
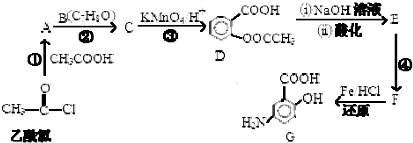
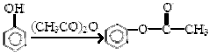 ,
, (具有还原性,极易被氧化)
(具有还原性,极易被氧化) .
. .
. (写出其中一种结构简式)
(写出其中一种结构简式)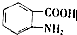 的流程图(无机试剂任选).合成路线流程图如下:X$→_{反应条件}^{反应物}$Y$→_{反应条件}^{反应物}$Z…目标产物.
的流程图(无机试剂任选).合成路线流程图如下:X$→_{反应条件}^{反应物}$Y$→_{反应条件}^{反应物}$Z…目标产物.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,4.4g体积比为3:1的CO2和N2O组成的混合气体中所含原子总数为0.3NA | |
| B. | CH4与P4的分子结构均为正四面体形,在1molCH4或P4分子中含有共价键数皆为4NA | |
| C. | 含有NA个阴离子的Na2O溶于水形成1L的溶液中,溶质的物的质量浓度为1mol•L-1 | |
| D. | 标准状况下,5.6L18O2参加反应一定转移NA个e- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 有人设计出一种在隔绝空气条件下让钠与FeSO4溶液反应的方法以验证反应实质.实验时,往100mL大试管中先加40mL煤油,取3粒米粒大小的金属钠放入大试管后塞上橡皮塞,通过长颈漏斗加入FeSO4溶液使煤油的液面至胶塞,并夹紧弹簧夹(如图),仔细观察,回答下列问题:
有人设计出一种在隔绝空气条件下让钠与FeSO4溶液反应的方法以验证反应实质.实验时,往100mL大试管中先加40mL煤油,取3粒米粒大小的金属钠放入大试管后塞上橡皮塞,通过长颈漏斗加入FeSO4溶液使煤油的液面至胶塞,并夹紧弹簧夹(如图),仔细观察,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| Cu(OH)2 | Mg(OH)2 | Fe(OH)3 | Al(OH)3 | |
| 开始沉淀的pH | 4.8 | 9.3 | 2.7 | 3.8 |
| 完全沉淀的pH | 6.4 | 10.8 | 3.7 | 4.7 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t℃ | 600 | 800 | 830 | 1000 | 1200 |
| K | 0.25 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
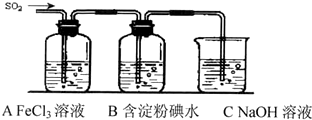
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com