
【题目】用废铅蓄电池的铅泥(含PbSO4、PbO和Pb等)可制备精细化工产品3PbO·PbSO4· H 2O(三盐),主要制备流程如下。

(1)铅蓄电池在生活中有广泛应用,其工作原理是Pb+PbO2+2H2SO4 ![]() 2PbSO4+2H2O。铅蓄电池在充电时,阳极的电极反应式为_________。若铅蓄电池放电前正、负极质量相等,放电时转移了lmol电子,则理论上两极质量之差为___________。
2PbSO4+2H2O。铅蓄电池在充电时,阳极的电极反应式为_________。若铅蓄电池放电前正、负极质量相等,放电时转移了lmol电子,则理论上两极质量之差为___________。
(2)将滤液I、滤液III合并,经蒸发浓缩、降温结晶、过滤等操作,可得到一种结晶水合物( Mr=322) ,其化学式为______________。
(3)步骤③酸溶时铅与硝酸反应生成Pb(NO3)2及NO的离子方程式为_____________;滤液II中溶质的主要成分为________(填化学式)。
(4)步骤⑥合成三盐的化学方程式为____________ 。
(5)步骤⑦的洗涤操作中,检验沉淀是否洗涤完全的操作方法是____________。
【答案】 PbSO4+2H2O-2e-=PbO2+SO42-+4H+ 16g Na2SO4·10H2O 3Pb+8H++2NO3-=3Pb2++2NO+4H2O HNO3 4PbSO4+6NaOH![]() 3PbO·PbSO4·H2O+3Na2SO4+2H2O 取少量最后一次洗涤后的滤液于试管中,滴加BaCl2溶液和稀盐酸,若产生白色沉淀,则沉淀末洗涤完全;若没有白色沉淀生成,则沉淀已洗涤完全
3PbO·PbSO4·H2O+3Na2SO4+2H2O 取少量最后一次洗涤后的滤液于试管中,滴加BaCl2溶液和稀盐酸,若产生白色沉淀,则沉淀末洗涤完全;若没有白色沉淀生成,则沉淀已洗涤完全
【解析】(1)铅蓄电池在充电时,阳极上PbSO4失去电子生成PbO2,根据电荷配平,可知阳极的电极反应式为PbSO4+2H2O-2e-=PbO2+SO42-+4H+;铅蓄电池放电时正极电极反应为: PbO2+SO42-+4H++2e-= PbSO4+2H2O,负极电极反应为:Pb +SO42--2e-= PbSO4,若铅蓄电池放电前正、负极质量相等,放电时转移了lmol电子,则理论上两极质量之差为: ![]() ;(2)铅泥与碳酸钠反应转化为碳酸铅和硫酸钠,过滤后滤液Ⅰ的主要成分是硫酸钠,碳酸铅、氧化铅和铅用硝酸溶解转化为铅离子,用稀硫酸反应沉铅生成硫酸铅,过量未反应的硝酸综合利用,以滤液Ⅱ的主要成分循环酸溶沉铅,过滤后的硫酸铅进入合成,与氢氧化钠反应,生成的硫酸钠以滤液Ⅲ过滤出,合成后过滤、洗涤干燥得到三盐。将滤液I、滤液III合并,经蒸发浓缩、降温结晶、过滤等操作,可得到一种结晶水合物为硫酸钠晶体,设化学式为:Na2SO4xH2O,则Mr=142+18x=322,解得:x=10,故结晶水合物化学式为:Na2SO4·10H2O;(3)步骤③酸溶时铅与硝酸反应生成Pb(NO3)2及NO转移电子数为6,其离子方程式为:3Pb+8H++2NO3-=3Pb2++2NO+4H2O;滤液II中溶质的主要成分为HNO3,循环使用,综合利用;(4)步骤⑥硫酸铅与氢氧化钠在50-60℃条件下合成三盐,同时生成硫酸钠和水,其化学方程式为4PbSO4+6NaOH
;(2)铅泥与碳酸钠反应转化为碳酸铅和硫酸钠,过滤后滤液Ⅰ的主要成分是硫酸钠,碳酸铅、氧化铅和铅用硝酸溶解转化为铅离子,用稀硫酸反应沉铅生成硫酸铅,过量未反应的硝酸综合利用,以滤液Ⅱ的主要成分循环酸溶沉铅,过滤后的硫酸铅进入合成,与氢氧化钠反应,生成的硫酸钠以滤液Ⅲ过滤出,合成后过滤、洗涤干燥得到三盐。将滤液I、滤液III合并,经蒸发浓缩、降温结晶、过滤等操作,可得到一种结晶水合物为硫酸钠晶体,设化学式为:Na2SO4xH2O,则Mr=142+18x=322,解得:x=10,故结晶水合物化学式为:Na2SO4·10H2O;(3)步骤③酸溶时铅与硝酸反应生成Pb(NO3)2及NO转移电子数为6,其离子方程式为:3Pb+8H++2NO3-=3Pb2++2NO+4H2O;滤液II中溶质的主要成分为HNO3,循环使用,综合利用;(4)步骤⑥硫酸铅与氢氧化钠在50-60℃条件下合成三盐,同时生成硫酸钠和水,其化学方程式为4PbSO4+6NaOH![]() 3PbO·PbSO4·H2O+3Na2SO4+2H2O;(5)步骤⑦的洗涤操作中,检验沉淀是否洗涤完全,若沉淀不完全则滤渣中含有硫酸根离子,检验是否含有硫酸根离子就可得解,其操作方法是:取少量最后一次洗涤后的滤液于试管中,滴加BaCl2溶液和稀盐酸,若产生白色沉淀,则沉淀末洗涤完全;若没有白色沉淀生成,则沉淀已洗涤完全。
3PbO·PbSO4·H2O+3Na2SO4+2H2O;(5)步骤⑦的洗涤操作中,检验沉淀是否洗涤完全,若沉淀不完全则滤渣中含有硫酸根离子,检验是否含有硫酸根离子就可得解,其操作方法是:取少量最后一次洗涤后的滤液于试管中,滴加BaCl2溶液和稀盐酸,若产生白色沉淀,则沉淀末洗涤完全;若没有白色沉淀生成,则沉淀已洗涤完全。


 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案科目:高中化学 来源: 题型:
【题目】有机物G是一种常用的植物调味油,分子式为C9H8O,能发生银镜反应,其工业合成路线如下图所示:
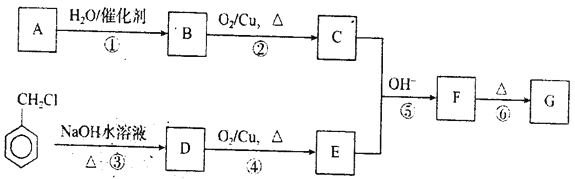
已知:① 烃A可作水果催熟剂
② CH3CHO+CH3CHO![]()
![]()
回答下列问题:
(1)D的名称_________。
(2)F中含有的官能团名称____________。
(3)⑥的反应类型____________。
(4)若要检验G中所含官能团,一次取样检验,按使用试剂的先后顺序,下列选项中_____(填字母编号)更为合理。
a.银氨溶液、溴水 b.溴水、银氨溶液
c.银氨溶液、稀盐酸、溴水 d.溴水、氢氧化钠溶液、银氨溶液
(5)写出反应③的化学反应方程式_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)合成氨反应是极其重要的氮的固定反应。已知键能数据如下:N≡N为E1kJ·mol—1、H—H为E2kJ·mol—1、N—H为E3 kJ·mol—1。则:
N2(g)+3H2(g)==2NH3(g);△H=_____kJ·mol—1(用含E1、E2、E3的式子表示)。
(2)HF与水可任意比混溶,其溶液中存在的分子间氢键有_____种;乙酸用五氧化二磷脱水,可得到乙烯酮( CH2=C=O),该分子中的羰基碳原子采用的杂化方式为________,一个分子中含有____________个![]() 键。
键。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在海水的综合利用中,海水提溴工业是一个重要组成部分,其中一种提溴的工艺是在预先浓缩并酸化的海水中,通入足量氯气,然后使生成的溴与吸收剂SO2反应转化为氢溴酸以达到富集溴元素的目的。在有关上述工艺流程的以下化学用语中,错误的是( )
A. 用电子式表示氢溴酸的形成过程为![]()
B. 海水中Br的电子式为:![]()
C. 海水中通入氯气时反应的离子方程式:2Br-+Cl2==Br2+2Cl-
D. Cl-的结构示意图为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃与氢气发生反应后能生成(CH2)2CHCH2CH3,则该烃不可能是
A. 2-甲基-2-丁烯 B. 3-甲基-1-丁炔
C. 2,3-二甲基-2-丁烯 D. 2-甲基-1,3-丁二烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学—选修3物质结构与性质] T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下表。
元素 | 相关信息 |
T | T元素可形成自然界硬度最大的单质 |
W | W与T同周期,核外有一个未成对电子 |
X | X原子的第一电离能至第四电离能分别是:I1=578kJ/mol,I2=1817kJ/mol,I3=2745kJ/molkJ/mol,I4=11575kJ/mol |
Y | 常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质 |
Z | Z的一种同位素的质量数为63,中子数为34 |
(1)TY2是一种常用的溶剂,是 (填极性分子或非极性分子),分子中存在 个σ 键。W的最简单氢化物容易液化,理由是 。
(2)在25℃、101kpa下,已知13.5g的X固体单质在O2气体中完全燃烧后恢复至原状态,放热419kJ,该反应的热化学方程式为 。
(3)基态Y原子中,电子占据的最高能层符号 ,该能层具有的原子轨道数为 、电子数为 。Y、氧、W元素的第一电离能由大到小顺序为 (用元素符号作答)。
(4)已知Z的晶胞结构如图所示,又知Z的密度为9.00 g/cm3,则晶胞边长为 ;ZYO4常作电镀液,其中YO42-的空间构型是 ,其中Y原子的杂化轨道类型是 。元素Z与人体分泌物中的盐酸以及空气反应可生成超氧酸:Z+HCl+O2=ZCl+HO2,HO2(超氧酸)不仅是一种弱酸而且也是一种自由基,具有极高的活性。下列说法或表示正确的是
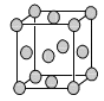
A.O2是 氧化剂
B.HO2 是氧化产物
C. HO2在碱中能稳定存在
D.1 mol Z参加反应有1 mol电子发生转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼是第IIIA族元素,单质硼在加热条件下能与多种非金属反应。某同学欲利用氯气和单质硼反应制备三氯化硼。已知BCl3的沸点为12.5℃,熔点为-107.3℃,遇水剧烈反应。
(1)选用下图所示的装置(可以重复选用)进行实验,装置依次连接的合理顺序为________。

(2)图中g管的作用是______,装置E的作用是_______。
(3)开始实验时,先点燃____(填“A”或“B”)处的酒精灯。
(4)请写出BCl3遇水变质的化学方程式___________。
(5)硼酸是一元弱酸,其钠盐化学式为Na[B(OH)4],则硼酸在水中电离方程式是______。
(6)实验完成后,某同学向F (溶液中含有0.05 mol/LNaC10、0.05 mol/LNaCl、0.1 mol/L NaOH)中滴加品红溶液,发现溶液褪色。现设计实验探究溶液褪色的原因,请将表中数据补充完整,完成实验方案。
实验序号 | 0.1mol/LNaClO溶液/mL | 0.1mol/LNaCl溶液/mL | 0.2mol/LNaOH溶液/mL | H2O /mL | 品红溶液 | 现象 |
① | 4.0 | 0 | 0 | x | 3滴 | 较快褪色 |
② | 0 | 4.0 | 4.0 | 0 | 3滴 | 不褪色 |
③ | 4.0 | 0 | 4.0 | 0 | 3滴 | 缓慢褪色 |
x=_______,结论:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是乙酸乙酯的合成路线图,已知B的水溶液可以溶解CaCO3,E可作果实催熟剂。
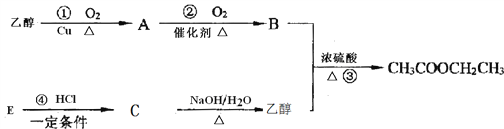
请完成下列问题:
(1)A的名称是_______;B中所含的官能团是__________;E的结构简式为___________________ 。
(2)反应③的反应类型是________;反应④的反应类型是_________________。
(3)写出CH3COOCH2CH3的同分异构体(含有酯基)______________________。
(4)请写出以下反应化学方程式:
A、合成路线①的方程式为____________________;
B、成路线④的方程式为_____________________;
C、物质E在一定条件下发生加聚反应的化学反应方程为___________________________;
D、写出乙酸乙酯在NaOH溶液中的水解反应方程式______________________;
E、写出B的水溶液溶解CaCO3的方程式________________________。
(5)如果用4.6 g的乙醇和9.0 g的B反应制得乙酸乙酯5.28 g。则本实验的产率是:__________(产率指的是某种生成物的实际产量与理论产量的比值)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com