
【题目】碳是形成化合物种类最多的元素,其单质及其化合物是人类生产生活的主要能源物质。请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程如下:ΔH=+88.6 kJ/mol则M、N相比,较稳定的是________。
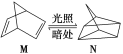
(2)已知CH3OH(l)的燃烧热为-726.5 kJ·mol-1,CH3OH(l)+1/2O2(g)=CO2(g)+2H2(g) ΔH=-a kJ·mol-1,则a________726.5(填“>”“<”或“=”)。
(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:_______________________________。
(4) 已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) △H=+489.0 kJ mol-1;CO(g)+l/2O2(g)=CO2(g)△H=-283. 0kJ mol-1;C(石墨)+O2(g)=CO2(g)△H=-393.5kJ mol-1。则4Fe (s)+3O2(g) =2Fe2O3(s)△H=____________。
【答案】M < 2Cl2(g)+2H2O(g)+C(s)=4HCl(g)+CO2(g)ΔH=-290 kJ·mol-1 -1641.0 kJ mol-1
【解析】
根据反应吸放热判断物质能量高低,进而判断物质的稳定性,根据盖斯定律书写热化学反应方程式并计算反应热。
(1)有机物M经过太阳光光照可转化成N:△H= +88.6kJmol-1,该过程是吸热反应,N暗处转化为M,是放热反应,根据反应物的能量越低越稳定,可知M稳定,故答案为:M;
(2)燃烧热是1mol物质完全燃烧生成稳定氧化物放出的热量,甲醇燃烧生成CO2(g)和H2(g)属于不完全燃烧,放出的热量小于燃烧热,故答案为:<;
(3)有1 mol Cl2参与反应时释放出145kJ热量,2 mol氯气反应放热290 kJ,反应的热化学方程式为:2Cl2(g) +2H2O(g) +C(s)═4HCl(g)+CO2(g)△H= -290 kJmol-1,故答案为:2Cl2(g) +2H2O(g)+C(s)═4HCl(g)+CO2(g)△H= -290kJmol-1 ;
(4)根据盖斯定律,将反应③×6①×2②×6得:4Fe(s)+3O2(g)![]() 2Fe2O3(s),则ΔH=393.5 kJ·mol1×6489.0 kJ·mol1×2+283.0 kJ·mol1×6=1641.0 kJ·mol1,故答案为:-1641.0 kJ mol-1。
2Fe2O3(s),则ΔH=393.5 kJ·mol1×6489.0 kJ·mol1×2+283.0 kJ·mol1×6=1641.0 kJ·mol1,故答案为:-1641.0 kJ mol-1。


科目:高中化学 来源: 题型:
【题目】下列是某化学研究性学习小组对某无色水样成分的检验过程,已知该水样中只可能含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 中的若干种离子,该小组同学取100mL水样进行实验:向样品中先滴加氯化钡溶液,再滴加
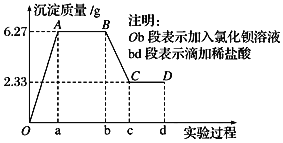
中的若干种离子,该小组同学取100mL水样进行实验:向样品中先滴加氯化钡溶液,再滴加![]() 盐酸,实验过程中沉淀质量的变化如图所示.下列说法正确的是
盐酸,实验过程中沉淀质量的变化如图所示.下列说法正确的是![]()
A.水样中一定不存在![]() 、
、![]() ,可能存在
,可能存在![]()
B.水样中一定存在![]() 、
、![]() 、
、![]()
C.BC段曲线所表示的离子方程式为![]()
D.水样中一定存在![]() ,且
,且![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列依据热化学方程式得出的结论正确的是
2C(s) +O2(g) =2CO (g) △H2则△H1<△H2
A.已知2SO2(g)+O2![]() 2SO3(g) 为放热反应,则SO2的能量一定高于SO3的能量
2SO3(g) 为放热反应,则SO2的能量一定高于SO3的能量
B.已知C(石墨,s)==C(金刚石,s)△H>0,则金刚石比石墨稳定
C.已知H+(aq)+OH-(aq)=H2O(1)△H=-57.3kJ/mol,则任何酸碱中和反应的热效应均为57.3 kJ
D.已知2C(s) +2O2(g) =2 CO2(g)△H1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol·L-1的三种酸(HA、HB和HD)溶液,滴定的曲线如图所示,下列判断错误的是( )
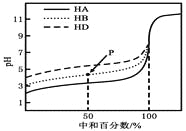
A. 三种酸的电离常数关系:KHA>KHB>KHD
B. 滴定至P点时,溶液中:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-)
C. pH=7时,三种溶液中:c(A-)=c(B-)=c(D-)
D. 当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)=c(OH-)-c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电石浆是氯碱工业中的一种废弃物,其大致组成如表所示:
成分 | CaO | SiO2 | Al2O3 | Fe2O3 | MgO | CaS | 其它不溶性的物质 |
质量分数/% | 65~66 | 3.5~5.0 | 1.5~3.5 | 0.2~0.8 | 0.2~1.1 | 1.0~1.8 | 23~26 |
用电石浆可生产无水CaCl2,某化工厂设计了以下工艺流程:
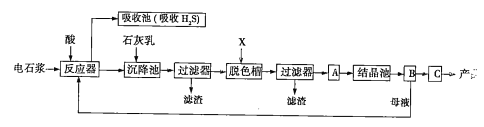
已知氯化钙晶体的化学式是CaCl2·6H2O;H2S是一种酸性气体,且具有还原性。
(1)反应器中加入的酸应选用______________。
(2)脱色槽中应加入的物质X是__________;设备A的作用是__________;设备B的名称为__________;设备C的作用是_______________。
(3)为了满足环保要求,需将废气H2S通入吸收池,下列物质中最适合作为吸收剂的是_______(填序号)。反应的化学方程式为____________________________。
A.水 B.浓硫酸 C.石灰乳 D.硝酸
(4)将设备B中产生的母液重新引入反应器的目的是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2RO3是一种二元酸,常温下用1L1mol·L-1Na2RO3溶液吸收RO2气体,溶液的pH随RO2气体的物质的量的变化如图所示。下列说法正确的是
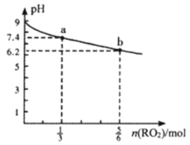
A.a点溶液中2c(Na+)=3c(RO32-)
B.向b点溶液中加水可使溶液的pH由6.2升高到7.4
C.常温下,NaHRO3溶液中c(HRO3-)>c(RO32-)>c(H2RO3)
D.当吸收RO2的溶液呈中性时,c(Na+)=c(RO32-)+c(HRO3-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应 C(s)+H2O(g)![]() CO(g)+H2(g)在一个可变容积的密闭容器中进行,下列条件的改变 对其反应速率几乎无影响的是( )
CO(g)+H2(g)在一个可变容积的密闭容器中进行,下列条件的改变 对其反应速率几乎无影响的是( )
①增加碳的量且表面积保持不变 ②加热③保持体积不变,充入 He,使体系压强增大 ④保持压强不变,充入 He,使容器体积变大
A.②④B.②③C.①④D.①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于苯的说法正确的是( )
A.苯的分子式为C6H6,它不能使酸性KMnO4溶液褪色,属于饱和烃
B.从苯的凯库勒式( )看,78g苯中含有碳碳双键数为3NA
)看,78g苯中含有碳碳双键数为3NA
C.在催化剂作用下,苯与液溴反应生成溴苯,发生了加成反应
D.苯分子为平面正六边形结构,6个碳原子之间的化学键完全相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室在50~60℃下制备硝基苯的反应装置如图所示。下列有关说法错误的是( )
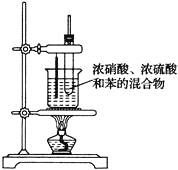
A.长玻璃导管的作用是冷凝回流、平衡压强
B.加入试剂的顺序:先加浓硝酸,再加浓硫酸,冷却后加入苯
C.将反应后的液体倒入烧杯中,加水
D.为了除去在硝基苯中的酸性物质,需要水洗、碱洗,然后再水洗
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com