
下列有关实验基本操作的说法错误的是 ( )。
A.存放浓硝酸时,使用带玻璃塞的棕色玻璃瓶
B.酸碱中和滴定时,若未用待测液润洗锥形瓶,对测定结果无影响
C.用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗上口倒出
D.将Mg(OH)2浊液直接倒入已装好滤纸的漏斗中过滤,洗涤并收集沉淀
 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源:2014年高一下学期化学必修2 1-1-2 元素的性质与原子结构练习卷(解析版) 题型:选择题
甲、乙、丙三种溶液中各有一种X-(X-为Cl-、Br-或I-),向甲中加入淀粉溶液和氯水,溶液变为橙色,再加丙溶液,颜色无明显变化,则甲、乙、丙中依次含有( )。
A.Br-、I-、Cl-B.Br-、Cl-、I- C.I-、Br-、Cl-D.Cl-、I-、Br-
查看答案和解析>>
科目:高中化学 来源:2014年江苏省南通市业水平测试(必修)化学试卷(解析版) 题型:选择题
实验室从海带中提取碘的操作过程中,仪器选用不正确的是
选项ABCD
操作称取3 g左右的剪碎了的干海带灼烧干海带碎片至完全变成灰烬过滤煮沸后的海带灰与水的混合液 用四氯化碳从氧化后的海带灰浸取液中提取碘
选用
仪器



查看答案和解析>>
科目:高中化学 来源:2014年化学高考题型专练四 氧化还原反应的规律与应用练习卷(解析版) 题型:选择题
锰酸钾可用于油脂、纤维、皮革的漂白等,其可由KOH、KClO3和MnO2经共熔制备,反应原理为6KOH+KClO3+3MnO2 KCl+3K2MnO4+3H2O。下列有关说法中正确的是 ( )。
KCl+3K2MnO4+3H2O。下列有关说法中正确的是 ( )。
A.KOH和KCl中均含有共价键
B.MnO2在反应中被还原
C.K2MnO4的氧化性大于KClO3
D.该反应中,每生成3 mol K2MnO4转移的电子数为6×6.02×1023
查看答案和解析>>
科目:高中化学 来源:2014年化学高考题型专练十六 基本理论综合应用题练习卷(解析版) 题型:填空题
多晶硅是太阳能光伏产业的重要原材料。
(1)由石英砂可制取粗硅,其相关反应的热化学方程式如下:
SiO2(s)+C(s)=SiO(g)+CO(g) ΔH=a kJ·mol-1
2SiO(g)=Si(s)+SiO2(s) ΔH=b kJ·mol-1
①反应SiO2(s)+2C(s)=Si(s)+2CO(g)的ΔH=________ kJ·mol-1(用含a、b的代数式表示)。
②SiO是反应过程中的中间产物。隔绝空气时,SiO与NaOH溶液反应(产物之一是硅酸钠)的化学方程式为________________________________。
(2)粗硅提纯常见方法之一是先将粗硅与HCl制得SiHCl3,经提纯后再用H2还原:
SiHCl3(g)+H2(g) Si(s)+3HCl(g)。
Si(s)+3HCl(g)。
不同温度及不同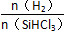 时,反应物X的平衡转化率关系如图所示。
时,反应物X的平衡转化率关系如图所示。
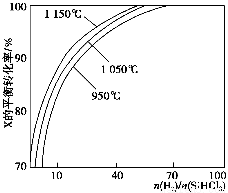
①X是________(填“H2”或“SiHCl3”)。
②上述反应的平衡常数K(1 150 ℃)________K(950 ℃)(填“>”、“<”或“=”)。
(3)SiH4(硅烷)法生产高纯多晶硅是非常优异的方法。
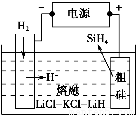
①用粗硅作原料,熔融盐电解法制取硅烷原理如图所示,电解时阳极的电极反应式为_________________________________________。
②硅基太阳电池需用N、Si两种元素组成的化合物Y作钝化材料,它可由SiH4与NH3混合气体进行气相沉积得到,已知Y中Si的质量分数为60%,Y的化学式为________。
查看答案和解析>>
科目:高中化学 来源:2014年化学高考题型专练十五 常见仪器的使用及实验基本操作练习卷(解析版) 题型:选择题
完成下列实验所选择的装置或仪器(夹持装置已略去)正确的是 ( )。
选项实验装置或仪器
A分离乙酸乙酯中混有的乙酸
B用已知浓度NaOH滴定未知浓度盐酸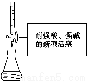
C从KI和I2的固体混合物中回收I2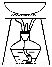
D配制100 mL 0.100 0 mol·L-1 NaOH溶液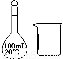
查看答案和解析>>
科目:高中化学 来源:2014年化学高考题型专练十二 常见无机物的性质及其综合应用练习卷(解析版) 题型:选择题
某同学向一支空试管中按一定的顺序分别加入下列四种物质(一种物质只加一次):①KI溶液
②淀粉溶液 ③NaOH溶液 ④新制氯水。发现溶液颜色按如下顺序变化:无色→棕黄色→蓝色→无色。依据溶液颜色的变化判断加入以上物质的顺序是 ( )。
A.①→②→③→④ B.①→④→②→③
C.②→④→①→③ D.①→②→④→③
查看答案和解析>>
科目:高中化学 来源:2014年化学高考题型专练十一 元素的单质及其化合物的性质与转化练习卷(解析版) 题型:选择题
下表各组物质之间通过一步反应不可以实现如图所示的转化关系的是( )。

选项XYZ箭头上所标数字的反应条件
ACaOCa(OH)2CaCO3①常温遇水
BAlCl3NaAlO2Al(OH)3②通入CO2
CFe2O3FeCl3Fe(OH)3④加入盐酸
DCl2Ca(ClO)2HClO③加浓盐酸
查看答案和解析>>
科目:高中化学 来源:2014年化学高考题型专练二 化学常用计量的理解和综合应用练习卷(解析版) 题型:选择题
阿伏加德常数约为6.02×1023 mol,下列说法中正确的是 ( )。
A.4.2 g丙烯(CH3CH===CH2)和乙烯的混合物中所含的碳原子数为0.3×6.02×1023
B.4.48 L N2O与CO2的混合气体所含电子数为0.2×22×6.02×1023
C.1 mol HCl和NH3的混合气体所含分子数为6.02×1023
D.100 mL 1 mol·L-1醋酸溶液中CH3COO-数目为0.1×6.02×1023
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com