
| A、①②③⑤⑦ | B、①②④ |
| C、③⑤⑦ | D、④⑥⑧ |
 ,为正四面体结构,但是金刚石为原子晶体,不存在分子,故错误;
,为正四面体结构,但是金刚石为原子晶体,不存在分子,故错误; ,为正四面体结构,故正确;
,为正四面体结构,故正确; ,二氧化硅晶体中存在四面体结构单元,每个硅原子能构成四个共价键,每个氧原子能形成2个共价键,Si处于中心,O处于4个顶角,但是二氧化硅晶体为原子晶体,不存在分子,故错误;
,二氧化硅晶体中存在四面体结构单元,每个硅原子能构成四个共价键,每个氧原子能形成2个共价键,Si处于中心,O处于4个顶角,但是二氧化硅晶体为原子晶体,不存在分子,故错误;

科目:高中化学 来源: 题型:
A、 制取干燥的氨气 |
B、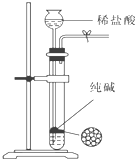 可用于制取少量纯净的CO2气体 |
C、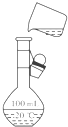 将溶液定容到100mL |
D、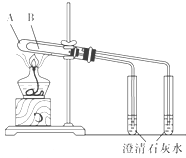 可用于比较碳酸钠和碳酸氢钠的热稳定性,大试管A中装碳酸钠固体,小试管B中装碳酸氢钠固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用量筒量取所需的盐酸时俯视刻度线 |
| B、定容时,仰视刻度线 |
| C、用量筒量取所需浓盐酸注入盛有适量蒸馏水的烧杯后,再分别用少量蒸馏水洗涤玻璃棒、量筒2-3次,洗涤液注入25 0 mL容量瓶中 |
| D、定容后倒转容量瓶几次,发现凹液面最低点低于刻度线,再补几滴水到刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、灯光明暗程度不变 |
| B、灯光变暗 |
| C、灯光变亮 |
| D、灯光明暗程度变化不明显 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、18g D2O中含有质子的数目为NA |
| B、0.1molCl2完全反应,转移的电子数一定为0.2NA |
| C、室温下,46 g NO2和N2O4的混合气体中含有氮原子数为NA |
| D、1 L 1mol?L-1的Na2CO3溶液中,阴离子总数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、进入煤矿井时,用火把照明 |
| B、用点燃的火柴在液化气钢瓶口检验是否漏气 |
| C、实验桌上的酒精灯倾倒了燃烧起来,马上用湿抹布扑灭 |
| D、实验时,将水倒入浓硫酸中配制稀硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol任何气体的体积都约是22.4 L |
| B、常温下,28 g氮气所含的原子数目为NA |
| C、在标准状况下,1mol任何物质所占的体积都约为22.4 L?mol-1 |
| D、醋酸的摩尔质量(单位为g?mol-1)与NA个醋酸分子的质量(单位为g)在数值上相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com