
| A.加入BaCl2溶液有白色沉淀产生,再加盐酸,沉淀不消失,原溶液一定有SO42— |
| B.滴入KMnO4酸性溶液,紫红色褪去,证明CH2=CHCH2CHO中一定有碳碳不饱和键 |
| C.某无色气体能使湿润的红色石蕊试纸变蓝,该气体的水溶液一定显碱性 |
| D.加入稀盐酸,产生无色并能使澄清石灰水变浑浊的气体,原溶液一定有CO32—或SO32— |
 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源:不详 题型:实验题
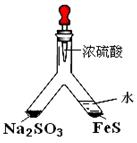
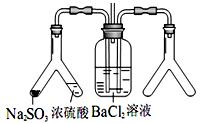
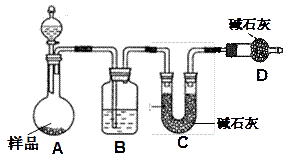
 验目的:探究 SO2与BaCl2反应产生沉淀的条件。二氧化硫通入氯化钡溶液并不产生沉淀,而通入另一种气体后可以产生白色沉淀。则右侧 Y型管中应放置的药品是____________和___________(必要时可以加热),该沉淀的化学式为________________。
验目的:探究 SO2与BaCl2反应产生沉淀的条件。二氧化硫通入氯化钡溶液并不产生沉淀,而通入另一种气体后可以产生白色沉淀。则右侧 Y型管中应放置的药品是____________和___________(必要时可以加热),该沉淀的化学式为________________。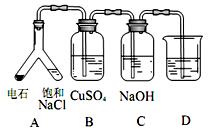
 证电石气的主要成分,D中盛放______________。
证电石气的主要成分,D中盛放______________。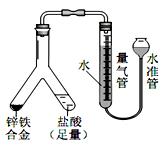
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
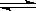 H++ClO-,为了探究HClO的漂白性,甲同学设计了如下的实验。
H++ClO-,为了探究HClO的漂白性,甲同学设计了如下的实验。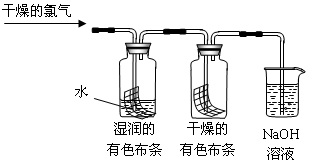
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| | 实验步骤 | 实验现象 |
| Ⅰ | 将打磨过的铝片(过量)放入一定浓度的CuCl2溶液中。充分反应后,过滤。 | 产生气泡,析出疏松的红色固体,溶液逐渐变为无色。 |
| Ⅱ | 滤液中加入少量的NaOH溶液。 | 有白色沉淀产生。 |
| Ⅲ | 将所得红色固体用蒸馏水洗涤后,加热烘干。 | 少量红色固体变黑 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.取Na2CO3溶液,发现取量过多,为了不浪费,又把过量的试剂倒回试剂瓶中。 |
| B.将剩余的金属钠放回原盛放金属钠的试剂瓶中。 |
| C.用蒸发方法使NaCl 从溶液中析出时,应将蒸发皿中NaCl 溶液全部蒸干才停止加热。 |
| D.用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.中和反应反应热的测定实验中,用温度计测完盐酸的温度后,直接继续测量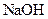 溶液的温度 溶液的温度 |
| B.中和反应反应热的测定实验中,将环形玻璃搅拌棒换成环形铁丝搅拌棒,不影响反应热的测定 |
C.用50ml酸式滴定管可准确量取25.00ml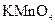 溶液 溶液 |
| D.用PH试纸测定溶液的PH时,需先用蒸馏水润湿试纸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| B.用100mL 量筒量取5.20mL 盐酸 |
| C.用托盘天平称取25.20g NaCl固体 |
| D.用100mL 容量瓶配制125mL 0.1mol·L-1盐酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com