
关于下图的说法正确的是
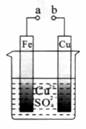
A.构成原电池时Cu是负极
B.构成电解池时Cu是阴极
C.构成电解池时质量增重的极是阴极
D.电池工作时溶液中的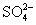 一定移向Cu极
一定移向Cu极
科目:高中化学 来源: 题型:
水溶液中能大量共存的一组离子是
A.Ba2+、Na+、Cl-、OH- B.Fe2+、H+、SO42-、NO3-
C.Na+、Mg2+、Cl-、CO32- D.K+、Fe3+、NO3-、SCN-
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下硝酸铵受热分解的未配平化学方程式为NH4NO3—HNO3+N2+H2O,在反应中被氧化与被还原的氮原子数之比为
A.5∶3 B.5∶4 C.1∶1 D.3∶5
查看答案和解析>>
科目:高中化学 来源: 题型:
镁铝合金5.1 g溶于300 mL 2 mol·L-1盐酸中,标准状况下放出气体体积为5.6 L,向反应后的溶液中加入500 mL NaOH溶液充分反应,最终产生白色沉淀。下列有关说法不正确的是
A.5.1 g镁铝合金中含有镁、铝的质量分别为2.4 g、2.7 g
B.溶解5.1 g镁铝合金时,剩余盐酸的物质的量为0.1 mol
C.生成白色沉淀的最大质量为13.6 g
D.若白色沉淀只有Mg(OH)2,该NaOH溶液的物质的量浓度至少为1.2 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
早期发现的一种天然二十面体准晶颗粒由 Al、Cu、Fe 三种金属元素组成。回答下列问题:
(1) 准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过 方法区分晶体、准晶体和非晶体。
(2) 基态 Fe原子有 个未成对电子,Fe3+的电子排布式为 。可用硫氰化钾检验 Fe3+,形成配合物的配离子可表示为 。
(3) 新制备的 Cu(OH) 2 可将乙醛(CH3CHO)氧化为乙酸,而自身还原成 Cu2O,乙醛中碳原子的杂化轨道类型为 ,1mol 乙醛分子中含有的 键的数目为 , 乙酸的沸点明显高于乙醛,其主要原因是 。Cu2O 为半导体材料,在其立方晶胞内部有 4 个氧原子,其余氧原子位于面心和顶点,则该晶胞中有 个铜原子。
键的数目为 , 乙酸的沸点明显高于乙醛,其主要原因是 。Cu2O 为半导体材料,在其立方晶胞内部有 4 个氧原子,其余氧原子位于面心和顶点,则该晶胞中有 个铜原子。
(4) Al 单质为面心立方晶体,其晶胞边长 a=0.405nm,晶胞中铝原子的配位数为 。
列式表示 Al 单质的密度 g·cm-3(不必计算出结果)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下图中,a、b、c、d、e为元素周期表中前四周期的一部分元素,下列有关叙述正确的是( )
A.元素b位于ⅥA族,有+6、-2两种常见化合价
B.五种元素中,元素e的性质最稳定
C.原子半径有d>c>b
D.元素e参与形成的化合物可以作为一种半导体材料
| a | |||
| b | |||
| c | d | ||
| e |
查看答案和解析>>
科目:高中化学 来源: 题型:
原子序数依次增大的短周期元素A、B、C、D、E、F,其中 A、B的阴离子与C、D的阳离子的电子排布式均为ls22s22p6,A原子核外有2个未成对电子,C单质可与热水反应但不能与冷水反应;E、F原子在基态时填充电子的轨道有9个,且E原子核外有3个未成对电子,F能形成与A相同价态的阴离子,且A离子半径小于F离子。回答:
(1)B元素的名称为 。
(2)A与F可形成两种中学化学常见的化合物,其分子式分别为 和 ;分子空间构型分别为 。
(3)请写出基态原子E的价电子排布式
(4)上述六种元素按电负性从大到小的排列是 (写元素符号表示)。
(5)C、D、E、F元素第一电离能从小到大的排列是 (写元素符号);
(6)A、B、C、D四种元素的简单离子按半径由小到大的顺序为(用离子符号表示)__________________________。
(7)C与A形成的化合物属于 晶体,此化合物和NaCl固体相比较熔点的高低关系为
(用化学式表示大小关系),原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com