
【题目】将下列物质的溶液在蒸发皿中加热蒸干并灼烧,可得到该物质的固体的是( )
A.MgCl2
B.NH4Cl
C.Na2CO3
D.KMnO4
科目:高中化学 来源: 题型:
【题目】一定温度下,在三个体积约为1.0L的恒容密闭容器中发生反应:2CH3OH(g)═CH3OCH3(g)+H2O(g)
下列说法正确的是( )
容器 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
I | 387 | 0.20 | 0.080 | 0.080 |
Ⅱ | 387 | 0.40 | ||
Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
A.该反应的正方应为吸热反应
B.达到平衡时,容器I中的CH3OH体积分数比容器Ⅱ中的小
C.容器I中反应达到平衡所需时间比容器Ⅲ中的长
D.若起始时向容器I中充入CH3OH 0.1mol、CH3OCH30.15mol和H2O 0.10mol,则反应将向正反应方向进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨化法是合成硫酰氯(SO2Cl2)的常用方法,实验室合成的酰氯的反应和实验装置如下所示:SO2(g)+Cl2(g) ![]() SO2Cl2(1) ΔH=-97.3KJ/mol。
SO2Cl2(1) ΔH=-97.3KJ/mol。

已知: 一般条件下,硫酰氯为无色气体,熔点为-541℃,沸点为69.1℃,在潮湿空气中会“发烟”;100℃以上开始分解,生成二氧化硫和氧气,长期放置会分解。
请回答下列问题:
(1)装置甲中,70%的硫酸体现的性质为_________。
(2)仪器己中盛放的试剂主要用于排气,该试剂最合适的是______(填名称);实验时,从仪器己中放出该试剂的操作方法是_________。
(3)①装置庚中的药品最合适的是________(填字母);
a.五氧化二磷 b. 碱石灰 c.无水氯化钙 d.硅胶
②装置丙的冷凝管中出水口是_______(填标号)
(4)活性炭的作用是____;若缺少装置乙和丁(均盛放浓硫酸),潮湿的氯气和二氧化硫发生反应的化学方程式是________。
(5)为提高本实验的硫酰氯的产率,在实验操作中还需要注意的有______。
a.控制气流速度,宜慢不宜快
b.保证装置的气密性良好
c.先向装置丙中通入一种气体,排出空气后再通入另一种气体
d.先通气体,再通冷凝水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用0.0500molL﹣1H2C2O4(二元弱酸)溶液滴定25.00mL0.1000molL﹣1NaOH溶液所得滴定曲线如图.下列说法正确的是( ) 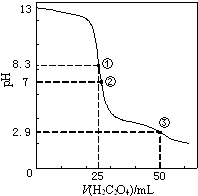
A.点①所示溶液中:c(H+)+c(H2C2O4)+c(HC2O4﹣)=c(OH﹣)
B.点②所示溶液中:c(HC2O4﹣)+2c(C2O42﹣)=c(Na+)+c(H+)
C.点③所示溶液中:c(Na+)>c(HC2O4﹣)>c(H2C2O4)>c(C2O42﹣)
D.滴定过程中可能出现:c(Na+)>c(C2O42﹣)=c(HC2O4﹣)>c(H+)>c(OH﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,回答下列有关问题: 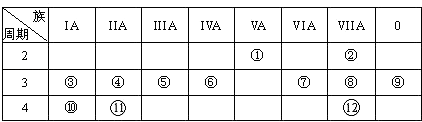
(1)写出下列元素符号:① , ⑥ , ⑦ .
(2)画出原子的结构示意图:④ , ⑧ .
(3)在①~12元素中,金属性最强的元素是 , 非金属性最强的元素是 , 最不活泼的元素是 . (均填元素符号)
(4)元素⑦与元素⑧相比,非金属性较强的是(用元素符号表示),下列表述中能证明这一事实的是 .
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(5)第三周期中原子半径最大的元素是(填序号),跟它同周期原子半径最小的元素是(填序号),它们可以形成(填离子或共价)化合物,用电子式表示其形成过程如下: .
(6)已知某元素原子最外层电子数是其次外层电子数的2倍,该元素可以与⑧形成一种AB4型的化合物,请用电子式表示其形成过程: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X,Y,Z,R,M是元素周期表中原子序数依次增大的五种短周期元素,其相关信息如下表:
元素 | 相关信息 |
X | X的一种核素的原子核中没有中子 |
Y | Y原子的核外电子占据4个原子轨道 |
Z | Z的气态氢化物能使湿润的红色石蕊试纸变蓝 |
R | R是地壳中含量最高的元素 |
M | M的单质与冷水剧烈反应,生成的强碱中含有电子数相同的阴阳离子 |
(1)Y,Z,R的第一电离能从大到小的顺序是(填元素符号)
(2)Z,R的最简单氢化物中稳定性强的是 , 沸点高的是(填化学式)
(3)甲是由上述3种元素组成的常见化合物,常温下pH=3的甲溶液中由水电离c(H+)=10﹣3mol/L,则甲的化学式是 .
(4)直线型分子Y2Z2中所有原子都达到8电子稳定结构,则分子中σ键与π键的个数之比是 .
(5)常温下0.58gY4H10完全燃烧放出29kJ的热量,请写出Y4H10燃烧热的热化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数为x的元素E在周期表中位于A,B,C,D四种元素中间(如图所示),则A,B,C,D四种元素的原子序数之和不可能是(镧系、锕系、O族元素除外)( ) 
A.4x
B.4x+6
C.4x+10
D.4x+14
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学方程式中,不能用H++OH-=H2O表示的是
A. 2NaOH+H2SO4 =Na2SO4+2H2O B. Ba(OH)2+2HCl=BaCl2+2H2O
C. Cu(OH)2+2HNO3=Cu(NO3)2+2H2O D. KOH+HCl=KCl+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是重要的化工原料,用CO2催化加氢可制取乙烯:2CO2(g)+6H2(g)![]() C2H4(g)+4H2O(g) △H<0
C2H4(g)+4H2O(g) △H<0
(1)若该反应体系的能量随反应过程变化关系如图所示,则该反应的△H=_______kJ/mol (用含a、b的式子表示)


(2)向1L容密闭容器中通入1 mol CO2和nmol H2,在一定条件下发生上述反应,测得CO2的转化率a(CO2)与反应温度、投料比X[![]() ]的关系如图所示。
]的关系如图所示。
①X1_______X2(填“>”“<”或“=”,下同),平衡常数Ka____Kb____Kc。
②若B点时X=3,则平衡常数Kb=__________(代入数据列出算式即可)。
③下列措施能同时满足增大反应速率和提髙CO2转化率的是______________。
a.升高温度 b.加入催化剂 c.增大投料比X d.增加压强
e.将产物从反应体系中分离出来
(3)乙烯也可作为制备甲酸的基础工业原料,常温时,HCOOH的电离平衡常数Ka=1.8×l0-4mol·L-1,pH=12的HCOONa和含少量NaOH混合溶液中。
①书写HCOONa的水解离子反应方程式_________________。
②该溶液中离子浓度关系:  =_________mol·L-1
=_________mol·L-1
③若0. lmol/L的HCOONa溶液中加入等体积的0.09mol/LHCOOH,配制了pH=6.8的溶液,则该溶液中微粒浓度由小到大的顺序为________________。(不考虑水分子)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com