
【题目】分子中所有原子不可能共平面的是( )
A. 苯 B. 乙炔 C. 乙烯 D. 甲烷
科目:高中化学 来源: 题型:
【题目】铝用途广泛,用铝土矿(主要成分为Al2O3nH2O、少量SiO2和Fe2O3)制取Al有如下途径: 
(1)滤液A加过量NaOH离子方程式表示为
(2)灼烧时盛放药品的仪器名称是 .
(3)步骤Ⅳ中发生反应的化学方程式是 .
(4)步骤Ⅲ中生成固体C的离子反应方程式为 .
(5)取滤液B 100mL,加入1molL﹣1盐酸200mL,沉淀量达到最大且质量为11.7g.则滤液B中c(AlO ![]() )= , c(Na+)6molL﹣1(填“>”、“=”或“<”).
)= , c(Na+)6molL﹣1(填“>”、“=”或“<”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于能量变化的说法正确的是
A. 冰融化成水放出热量
B. 金属与酸反应吸收能量
C. 生成物的总能量一定低于反应物的总能量
D. 化学键的断裂和形成是化学反应中能量变化的主要原因
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合金是指两种或两种以上的金属(或金属与非金属)熔合而成的具有金属特性的物质。分析下表中的数据,不能形成合金的是
Na | Cu | Al | Fe | |
熔点/℃ | 97.8 | 1083 | 660 | 1535 |
沸点/℃ | 883 | 2567 | 2467 | 2750 |
A.Cu和Al B.Fe和Cu C.Cu和Na D.Al和Na
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有①乙酸乙酯和碳酸钠溶液②甲醇和乙醇③溴化钠和溴水三组混合物,分离它们的正确方法依次是( )
A. 分液 蒸馏 萃取 B. 蒸馏 萃取 分液
C. 分液 萃取 蒸馏 D. 萃取 蒸馏 分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、某学生用0.2000 mol·L-1的标准NaOH溶液滴定未知浓度盐酸,其操作可分为如下几步:
①用蒸馏水洗涤碱式滴定管,并注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④量取20.00mL待测液注入用待测液润洗过的锥形瓶中,并加入3滴甲基橙溶液
⑤用标准液滴定至终点,记下滴定管液面读数

请回答:
(1)以上步骤有错误的是(填编号)________。
(2)用标准NaOH溶液滴定时,应将标准NaOH溶液注入______中。(从图中选填“甲”或“乙”)
(3)滴定时,左手控制滴定管,右手摇动锥形瓶,眼睛注视_______________。
(4)判断到达滴定终点的现象是:锥形瓶中溶液_________________________。
(5)下列操作会引起实验结果偏大的是:______(填编号)
A.滴定终点时,有一滴标准液悬挂在滴定管尖嘴处
B.观察计数时,滴定前俯视,滴定后仰视
C.锥形瓶先用蒸馏水洗涤后,未用待测液润洗
D.用酸式滴定管量取液体时,释放液体前滴定管前端有气泡,之后消失
E.滴定时振荡锥形瓶有溶液飞溅出去
F.配制标准NaOH溶液定容时仰视观察刻度线
II、某课外活动小组为了测定某(CuCl22H2O)样品的纯度,设计了如下方案:
称取1.0 g样品溶解于适量水中,向其中加入含AgNO3 2.38 g的AgNO3溶液(溶液中除Cl-外,不含其他与Ag+反应生成沉淀的离子),Cl-即被全部沉淀。然后用含Fe3+的溶液作指示剂,用0.2 mol·L-1的KSCN标准溶液滴定剩余的AgNO3,使剩余的Ag+以AgSCN白色沉淀的形式析出,以测定样品的纯度。
请回答下列问题:
(6)判断滴定达到终点的现象是___________________。
(7)在终点到达之前的滴定过程中,两种沉淀表面会吸附部分Ag+,需不断剧烈摇动锥形瓶,否则会使n(Cl-)的测定结果_____________(选填“偏高”、“偏低”或“无影响”)。
(8)若到达滴定终点时,用去KSCN标准溶液20.00mL,求此样品的纯度__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸异戊酯是组成蜜蜂信息素的成分之一,实验室制备乙酸异戊酯的反应装置示意图和有关数据如下:
![]()
相对分子质量 | 密度/(g·cm-3) | 沸点/℃ | 水中溶解度 | |
异戊醇 | 88 | 0.8123 | 131 | 微溶 |
乙 酸 | 60 | 1.0492 | 118 | 溶 |
乙酸异戊酯 | 130 | 0.8670 | 142 | 难溶 |
实验步骤:在A中加入4.4 g的异戊醇,6.0 g的乙酸、数滴浓硫酸和2~3片碎瓷片,开始缓慢加热A,回流50分钟,反应液冷却至室温后,倒入分液漏斗中,分别用少量水,饱和碳酸氢钠溶液和水洗涤,分液出来的产物加入少量无水硫酸镁固体,静置片刻,过滤除去硫酸镁固体,进行蒸馏纯化,收集140~143 ℃馏分,得乙酸异戊酯3.9 g。回答下列问题:
(1)装置B的名称是:_____________________。
(2)在洗涤操作中,第一次水洗的主要目的是:_________________________;
第二次水洗的主要目的是:__________________________________________。
(3)在洗涤、分液操作中,应充分振荡,然后静置,待分层后________(填标号),
A.直接将乙酸异戊酯从分液漏斗上口倒出
B.直接将乙酸异戊酯从分液漏斗下口放出
C.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
D.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口放出
(4)本实验中加入过量乙酸的目的是:___________________________。
(5)实验中加入少量无水硫酸镁的目的是:_________________________________。
(6)在蒸馏操作中,仪器选择及安装都正确的是:_____________(填标号)。
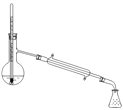

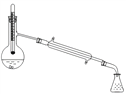
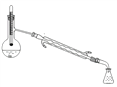
a b c d
(7)本实验的产率是:_________。
A.30 % B.40% C.50% D.60%
(8)在进行蒸馏操作时,若从130 ℃开始收集馏分,产率偏_________(填“高”或者“低”)。原因是___________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A.FeCl2溶液中通入Cl2:Fe2++Cl2= Fe3++2Cl-
B.澄清石灰水与少量小苏打溶液混合:Ca2++OH-+HCO3-= CaCO3↓+H2O
C.FeS固体放入稀硝酸溶液中:FeS+2H+= Fe2++H2S↑
D.AlCl3溶液中加入过量氨水:Al3++4OH-=AlO2-+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com