
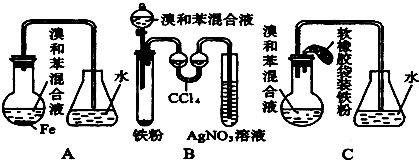
 ,
, ;
;

科目:高中化学 来源: 题型:阅读理解

| Fe |
| Fe |
查看答案和解析>>
科目:高中化学 来源: 题型:
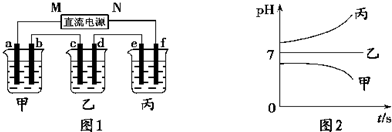
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:学习周报 化学 人教课标高二版(选修4) 2009-2010学年 第8期 总第164期 人教课标版(选修4) 题型:058
有
A、B、C三种电解质溶液分别装在三个烧杯中,插有石墨电极,并按如图所示安装装置,在电路中连接密闭开关K后,测得各支路电流强度IⅠ≈IⅡ(其中IⅡ略小).若撤去B,测得IA回答下列问题:
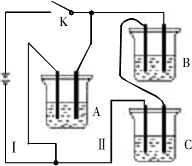
(1)通过实验,请你推断A、B、C三种溶液溶质的化学式分别为:A:________,B:________,C:________.
(2)若向C溶液中滴入酚酞呈红色,则C是________.
(3)已知:H2O![]() H++OH-,根据上述实验,请你判断,若将A、B、C分别等体积进行两两混合,能使H2O的电离程度最大的组合为________(填“AB”、“BC”或“AC”).试用离子方程式解释其原因________.
H++OH-,根据上述实验,请你判断,若将A、B、C分别等体积进行两两混合,能使H2O的电离程度最大的组合为________(填“AB”、“BC”或“AC”).试用离子方程式解释其原因________.
查看答案和解析>>
科目:高中化学 来源:模拟题 题型:实验题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com